 Tp N 3 -Étude de la variation de la tension superficielle en fonction
Tp N 3 -Étude de la variation de la tension superficielle en fonction
dans ce cas on observera une dépression capillaire. La loi de Jurin donnera une hauteur négative. 2. Manipulation. Le matériel
 Chapitre V : Tension superficielle et capillarité - V-1 Tension
Chapitre V : Tension superficielle et capillarité - V-1 Tension
La résultante F de ces tensions équilibre maintenant le poids P du liquide manquant. Si l'angle θ dépasse 90o la loi de Jurin donne h négatif. On parle alors
 Chapitre 3 Phénomènes de surfaces
Chapitre 3 Phénomènes de surfaces
✓ θ > 90° : hmin; Le liquide ne mouille pas le solide la loi de Jurin donne la valeur de h tension superficielle d'un alcool gras. Si cet anneau est en ...
 Chapitre 3 : Phénomènes de surfaces
Chapitre 3 : Phénomènes de surfaces
(Loi de Laplace). Le poids de la colonne de liquide dans le tube P= mg= π R² ρ g h est équilibré par la force de tension superficielle
 (1) Chapitre 3 : Phénomènes de surface 1. Phénomènes de surface
(1) Chapitre 3 : Phénomènes de surface 1. Phénomènes de surface
Mesure de la tension superficielle. ➢ Méthode capillaire : est basée sur la loi de Jurin. C-à-d : en appliquant la loi de Jurin on déduit une valeur de σ
 LES PHENOMENES DE SURFACE Tension superficielle - Capillarité
LES PHENOMENES DE SURFACE Tension superficielle - Capillarité
Loi Tension-Pression dans les structures élastiques de l'organisme 1. Stalagmométrie de Quincke. (Compte gouttes) : Loi de Tate. 2. Capillarité ( Loi de jurin).
 Chapitre 4 : Tension superficielle
Chapitre 4 : Tension superficielle
L'huile monte dans les tubes jusqu'à une hauteur. (soulignée en rouge) d'autant plus grande que le rayon est pe- tit : c'est la loi de Jurin. On observe
 Examen
Examen
Jan 30 2016 de la tension superficielle d'un liquide ? Expliquer. *Selon la ... La tension superficielle du mercure : par application de la loi de Jurin :.
 Chapitre 9 - Tension superficielle
Chapitre 9 - Tension superficielle
Équation sur les forces. On peut aussi obtenir la loi de Jurin en écrivant l'équilibre des forces en l'occurrence le poids de la colonne de fluide = 2ℎ
 LABORATOIRE DE PHYSIQUE TRAVAUX PRATIQUES DE
LABORATOIRE DE PHYSIQUE TRAVAUX PRATIQUES DE
Cet effet de surface ou de tension superficielle Vérification expérimentale de la loi de Jurin et calcul du coefficient de la tension superficielle du liquide ...
 LES PHENOMENES DE SURFACE Tension superficielle - Capillarité
LES PHENOMENES DE SURFACE Tension superficielle - Capillarité
?= Tension superficielle. ? S minimum ( Ex : bulle goutte …) Tension superficielle du liquide ... Capillarité - Loi de. Jurin. Phénomènes de surface.
 Tp N 3 -Étude de la variation de la tension superficielle en fonction
Tp N 3 -Étude de la variation de la tension superficielle en fonction
dans ce cas on observera une dépression capillaire. La loi de Jurin donnera une hauteur négative. 2. Manipulation. Le matériel
 Untitled
Untitled
Vérifier la loi de Jurin et calculer le coefficient de tension superficielle (ou tension superficielle). II DESCRIPTION: Cet appareil comprend :.
 La tension superficielle
La tension superficielle
que l'on appelle Loi de Jurin. R : rayon intérieur du tube ?: masse volumique du liquide
 TD : Tension Superficielle
TD : Tension Superficielle
On veut déterminer le coefficient de tension superficielle ? de l'éthanol. que la hauteur d'ascension capillaire est donnée par la loi de Jurin :.
 Olympiades de physique 2012
Olympiades de physique 2012
phénomènes naturels qui semblent défier les lois de Interprétation : La force de tension superficielle s'exerce et retient ... b. loi de Jurin.
 Loi de JURIN
Loi de JURIN
avec A tension superficielle du liquide ? sa masse volumique et g l'accélération de la pesanteur. BULLETIN DE L'UNION DES PHYSICIENS.
 Cours sur le module M3 : Tension superficielle et capillarité
Cours sur le module M3 : Tension superficielle et capillarité
Figure 1 – Expériences simples sur la tension superficielle La loi de Jurin donne la hauteur à laquelle un liquide monte dans un tube capillaire.
 Examen
Examen
30 janv. 2016 *Selon la loi de Laplace la surpression à l'intérieur d'une ... La tension superficielle du mercure : par application de la loi de Jurin :.
 Avec son air vibrant lorgue résonne !
Avec son air vibrant lorgue résonne !
ascension capillaire (Loi de Jurin). 3°) Expérience n°7 : Mesure du coefficient de tension superficielle de l'éthanol par décroissance de l'ascension
 [PDF] Loi de JURIN
[PDF] Loi de JURIN
avec A tension superficielle du liquide ? sa masse volumique et g l'accélération de la pesanteur BULLETIN DE L'UNION DES PHYSICIENS
 [PDF] loi de jurin
[PDF] loi de jurin
Vérifier la loi de Jurin et calculer le coefficient de tension superficielle (ou tension superficielle) II DESCRIPTION: Cet appareil comprend :
 [PDF] Chapitre V : Tension superficielle et capillarité
[PDF] Chapitre V : Tension superficielle et capillarité
En appliquant la loi de Jurin on déduit une valeur de ? de la mesure de la dénivellation h et de la connaissance des autres paramètres On installe sur une
 [PDF] Tension superficielle (PC*) - Olivier GRANIER
[PDF] Tension superficielle (PC*) - Olivier GRANIER
On peut retrouver la loi de Jurin en effectuant un bilan des forces : La force de tension superficielle qui agit sur tout le tour du ménisque compense le poids
 [PDF] Chapitre 4 : Tension superficielle
[PDF] Chapitre 4 : Tension superficielle
On appelle tension superficielle la force (par unitée de longueur) qui tire sur l'interface tangentiellement à la surface et de manière à réduire son aire La
 [PDF] Tension superficielle - LPENS
[PDF] Tension superficielle - LPENS
Il est donc cohérent que la tension superficielle associée aux forces de On peut aussi obtenir la loi de Jurin en écrivant l'équilibre des forces
 [PDF] LES PHENOMENES DE SURFACE Tension superficielle - Capillarité
[PDF] LES PHENOMENES DE SURFACE Tension superficielle - Capillarité
?= Tension superficielle ? S minimum ( Ex : bulle goutte ) Tension superficielle du liquide Capillarité - Loi de Jurin Phénomènes de surface
 [PDF] Chapitre tension superficielle
[PDF] Chapitre tension superficielle
Définition : La tension superficielle est un phénomène d'augmentation de l'énergie à la surface d'un fluide LA LOI DE JURIN OU DE LA CAPILLARITE
 [PDF] Cours de BTS BAT et TP - Module M3 : Tension superficielle
[PDF] Cours de BTS BAT et TP - Module M3 : Tension superficielle
La loi de Jurin donne la hauteur à laquelle un liquide monte dans un tube capillaire Cette loi a été énoncée en 1717 par le médecin anglais James Jurin h = 2
 [PDF] Chapitre 3 : Phénomènes de surfaces
[PDF] Chapitre 3 : Phénomènes de surfaces
La tension superficielle est une propriété des liquides qui permet de maintenir en équilibre leur surface libre [7] Au sein d'un liquide au repos chaque
Comment calcul la tension superficielle ?
Eau80°C 62 Huile d'olive 20°C 32 Comment expliquer la tension superficielle ?
La tension superficielle est la force de traction agissant sur un élément de surface situé dans un plan tangent à la surface et qui s'oppose à la dilatation de celle?ci. Ce coefficient est homogène au quotient d'une force par une longueur.Pourquoi le savon diminue la tension superficielle ?
Quand tu ajoutes du savon, le savon va séparer les molécules d'eau les unes des autres. Comme les molécules d'eau se séparent, le mur devient alors beaucoup moins résistant et donc l'aiguille coule.- Le phénomène de tension superficielle provient de l'existence des forces intermoléculaires. Une molécule de surface ayant moins de voisines qu'une molécule profonde, il faut rompre des liaisons, donc fournir du travail, pour amener une molécule profonde à la surface, c'est-à-dire pour augmenter la surface libre.
 BTS Bat et TP Cours sur le module M3 : Tension superficielle et capillarité
BTS Bat et TP Cours sur le module M3 : Tension superficielle et capillarité Notions et contenusCompétences exigibles
Tension superficielle et capillarité.Mettre en évidence expérimentalement les phénomènes de capillarité.Etudier les phénomènes de capillarité
sur les matériaux poreux.1 La tension superficielle des fluides
1.1 Quelques expériences sur la tension superficielleFigure1 - Expériences simples sur la tension superficielle
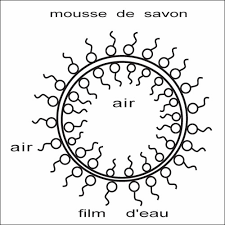
L"eau fa itu nb ourreletsur la pièce de monnaie. T outse passe comme si la surface libre formait une sorte de peau élastique qui retenait l"eau; Le trom boneflotte sur l"eau alors que l amasse v olumiquedu métal e stsup érieureà celle de l"eau, ce qui viole le principe d"Archimède (voir cours M2), ceci est dû à cette sorte de peau élastique à la surface de l"eau qui agit un peu comme un trampoline et retient les objets légers (certains insectes aquatiques du typeGerris lacustrisen profitent pour marcher sur l"eau); La bulle de sa vonminimise sa surface et te ndle fil c ommeun arc à caus ede la tension superficielle; La bulle de sa vonp euttirer une p etitebarre et la m ettreen mouv ement,comme un petit ressort qui se contracte, grâce à la tension superficielle; La bulle de sa vonprend une forme très sp écialep ourminimiser sa surface, on a l"im- pression de voir la molécule de méthane CH4avec le carbone au centre du tétraèdre et
les 4 hydrogènes au sommet de ce dernier.1.2 Quelques notions sur la tension superficielleFigure2 - Interactions entre molécules à la surface libre du liquide
Contrairement aux gaz, les liquides n"occupent pas tout le volume qui leur est offert lorsqu"ilssont contenus dans un récipient. Les liquides possèdent ainsi une ou des surfaces libres. Dans le
cas des gaz, les molécules n"interagissent que par chocs, les forces de cohésion entre molécules
étant inexistantes. En revanche, pour les liquides, ce sont les forces de cohésion d"origine élec-
tromagnétique qui permettent aux molécules de rester voisines. Les molécules se situant à la
surface libre ne possèdent pas autant de proches voisines que leurs homologues situés au seindu liquide. La figure 2 illustre la situation des molécules situées en surface (les flèches indiquent
le sens des interactions subies par chaque molécule).1E. H.
BTS Bat et TP Cours sur le module M3 : Tension superficielle et capillaritéLes molécules situées en surface du liquide sont ainsi attirées vers ce dernier. Le travail élé-
mentaire qu"il faut fournir pour accroître la surface libre du fluide de dS est proportionnel à
une quantité appeléecoefficient de tension superficiellenotée (N.m1) avec un travailélémentaire du type : dW =
dS. Ainsi, le liquide tend-il à minimiser sa surface pour minimi- ser son énergie (c"est pour cela qu"en apesanteur,l"eau prend la forme d"une sphèredans unecapsule spatiale). Cette dernière dépend de la température. Voici quelques valeurs :Liquide à 20°CEauEau savonneuseHydrocarburesGlycérineToluène
(N.m1)0,0730,060 à 0,0500,015 à 0,0310,0650,028 Remarque 1: la tension superficielle intervient également dans la forme de l"interface entre deux liquides non miscibles.Remarque 2: la valeur de la tension superficielle d"un fluide est liée à celle de la chaleur latente
de vaporisation. En effet, l"énergie nécessaire pour amener une molécule du fluide à la surface
sert à rompre environ 50 % (ce n"est qu"une approximation grossière) des forces de cohésion.
Dans le cas de la vaporisation d"une molécule du fluide, il faut rompre toutes les forces de cohésion ce qui nécessite environ le double d"énergie.1.3 Fluide mouillant
Du fait de l"existence de la tension superficielle, les liquides ont une propension plus ou moinsimportante à s"étaler sur un support solide. Cet effet peut être quantifié en mesurant l"angle
de contactouangle de mouillagenoté:Figure3 - Mouillage du solide par le liquide Le fluide mouille parfaitement la paroi si= 0°. Si le fluide est parfaitement non mouillant alors := 180°. Donnons quelques valeurs :InterfaceEau-verreÉthanol-verreEau-paraffineAngle de contact0°0°107°
La dissolution de molécules peut modifier la tension superficielle d"un liquide. Les tensioactifs (lessives, détergents...) permettent ainsi de l"eau de mieux mouiller certaines surfaces commecelle des plastiques et fibres synthétiques.Figure4 - Action d"un détergent sur la tension superficielle et le mouillage d"une surface
2E. H.
BTS Bat et TP Cours sur le module M3 : Tension superficielle et capillarité Notons enfin que la mouillabilité d"une surface dépend de nombreux facteurs (température,hygrométrie...). Il est ainsi déconseillé de peindre un jour de pluie, sous peine que la peinture
ne mouille pas la surface.1.4 Forme des ménisques
La forme des ménisques est une manifestation de la tension superficielle des fluides. Si le fluide
mouille la paroi du récipient (< 90°) alors le ménisque est concave (cas des solutions aqueuses
contenues dans du verre). Si le fluide mouille mal (> 90°) les parois du récipient, alors leménisque est convexe. Voici deux exemples :Figure5 - Ménisque concave (eau) et ménisque convexe (mercure)
1.5 Loi de Laplace ou pression de Laplace
Il faut bien noter que ce qui précède estcontraire à la relation fondamentale de l"hy- drostatiquedu module M2 qui dit que la surface libre d"un liquide estparfaitement plane et horizontale(tous les points à lamême pression, en l"occurence, la pression atmosphérique, devraient être à lamême altitude). On lève ce paradoxe en distinguant soigneusement pour un point A sur une surface non plane, A dans la phase liquide A liquideet le même point A mais dans la phase gaz A gaz.À cause de la tension superficielle, la pression est toujours un peu plusforte à l"intérieur de la voûte(côté concave du ménisque)et un peu plus faible à l"extérieur de
cette même voûte(côté convexe du ménisque). Par exemple pour les deux ménisques eau /air et mercure / air, on a : p(A eau) < p(Aair) et p(Aair) = patmdonc p(Aeau) < patm p(A mercure) > p(Aair) et p(Aair) = patmdonc p(Amercure) > patm Dans le cas particulier d"une goutte sphérique de rayon r, laloi de Laplacedit que cette différence de pression estproportionnelleaucoefficient de tension superficielle et inversement proportionnelleaurayonde courbure r :p 2p1=2 rp1< p2est lapression du côtéextérieur (convexe) en pascals (Pa);p
2> p1est lapression du côtéintérieur (concave) en pascals (Pa);r est lerayonde la goutte en mètre (m).la pression différentielle p
2- p1est lapression de Laplaceen pascals (Pa).Par contre, lorsqu"on est loin de l"interface solide/liquide et que la surface est plane (rayon
infini), la pression différentielle (de Laplace) est nulle. p2- p1= 0 carlimr!12
r = 0et p2=p1. p(A liquide)= p(Aair) = p(A) = patm Lorsque lasurface libredu liquide estplane, il n"y a plus lieu de distinguer les deux phases pour un point à l"interface etla relation fondamentale de l"hydrostatique(RFH)s"ap- pliquecar la tension superficielle, même non nulle, n"a plus d"influence.3E. H.
BTS Bat et TP Cours sur le module M3 : Tension superficielle et capillarité1.6 Ascension capillaire, loi de Jurin
Figure6 - Ascension capillaire pour l"eau et pour le mercure La loi de Jurin donne la hauteur à laquelle un liquide monte dans un tube capillaire. Cette loi a été énoncée en 1717 par le médecin anglais James Jurin.h=2: :cos()r::gh est lahauteurdu liquide dans le tube capillaire en mètres (m);est latension superficielledu liquide en newton par mètre (N.m1);est l"angle de contactentre le liquide et la paroi du tube;est lamasse volumiquedu liquide en kilogrammes par mètre cube (kg.m3);r est lerayon du tubeen mètres (m);g est l"accélération de la pesanteurterrestre, g = 9,81 m.s2.Plus le tube est fin, plus l"eau monte haut à l"intérieur. Cette montée de l"eau ne nécessite pas
d"énergie externe vu qu"elle provient de l"eau elle-même à cause de sa tension superficielle (la
surface agit comme un ressort). On remarque que pour le mercure, c"est exactement l"inverse,il descend dans le tube capillaire car l"angle de contactest supérieur à 90°et son cosinus est
négatif, ce qui donne un h négatif, ce qui signifie une descente du liquide.2 Le phénomène de capillarité
2.1 Ascension capillaire dans les matériaux poreux
L"ascension capillaire désigne la montée d"un liquide dans un solide poreux. Lorsque la taillecaractéristique des alvéoles est tres petite, alors les forces capillaires (dues à la tension superfi-
cielle) peuvent devenir du même ordre de grandeur que la force de pesanteur (le poids). Dans cecas, si le fluide mouille partiellement le solide l"entourant, il peut vaincre les forces de pesanteur
et ainsi s"élever en altitude. La hauteur d"ascension est d"autant plus importante que le diamètre
des porosités est petit, elle est proportionnelle au coefficient de tension superficielle du liquide
(N.m1). C"est par capillarité que le café monte dans un sucre ou que les éponges, le sopalin
et le papier filtre (fibres de cellulose) absorbent l"eau. C"est encore la capillarité qui permet à
la cire chaude fondue de monter dans la mèche de la bougie pour alimenter en permanence laflamme en combustible. Elle explique également le principe des marqueurs pour tableaux blanc.Figure7 - Ascension capillaire dans un matériau poreux
4E. H.
BTS Bat et TP Cours sur le module M3 : Tension superficielle et capillarité2.2 Le phénomène de capillarité (humidité ascensionnelle) dans le
BTPFigure8 - Le phénomène de capillairité dans le BTP L"humidité ascensionnelle fait partie despathologies du bâtiment les plus destructrices.D"origine souterraine, elle engendre desdégâts visibles et invisibles, qui se répercutent sur
lasanté des habitants. Il est essentiel d"identifier clairement les causes, pour appliquer labonne thérapie. Elle n"épargne aucun matériau, de structure ou décoratif. Les dégradations se
produisentà l"intérieurcommeà l"extérieurdes habitations. Les effets visuels des remontées
de sol peuvent se confondre avec d"autres problèmes d"humidité. Seule uneexpertise objectiveest en mesure d"identifier le mal à sa source et de préconiser les moyens d"action appropriés.Figure9 - Quelques méthodes de traitement des remontées capillaires
En matière de lutte contre l"humidité ascensionnelle, il n"y a pas de panacée mais un éventail de
solutions adaptables au cas par cas. Les travaux cosmétiques sont à éviter en toute circonstance,
sous peine d"aggraver la situation. Pour permettre l"étanchéité de la maison chaque méthode
d"assèchement a ses contraintes. L"intervention sur la maçonnerie (coupure à la scie circulaire
de l"enduit) n"est jamais anodine et les effets de certains matériaux ou produits font débat.Unebarrière étanchestoppe les remontées d"humidité mais ne protège pas les parois enterrées.
Là où l"eau est en excès, on pallie le problème enrepoussant des soubassements. Il existe
pour cela différents systèmes qui imposent tous decreuser une tranchée jusqu"à la semelle
des fondations. Ledrainagea pour fonction derecueillir les eaux souterraines et de les évacueravant qu"ellesn"atteignent les fondations. Sa mise en oeuvre obéit à des règles précises. Lecuvelageestl"ultime
recours pour les caves et sous-sols humides: le cuvelage peut être extérieur ou intérieur. Car il
est des circonstances où le drainage s"avère insuffisant, voire contrindiqué. Notamment, lorsque
des locaux enterrés subissent la pression d"une nappe phréatique ou des crues ponctuelles.Remarques :
-Les produits hydrofugesont pour fonction dediminuer ou arrêter l"absorption d"eau par capillaritédans les matériaux poreux. Il existe deux types d"hydrofuges : les hydro- fuges de masse et les hydrofuges de surface. -Les adjuvants béton(entraîneurs d"air, superplastifiants...) contiennent des molécules qui agissent sur la tension superficielle (surfactants, tensio-actifs). Plus la tension super- ficielle est abaissée, plus il est facile d"obtenir desbulles(d"air ou d"eau)de faibles diamètres.5E. H.
quotesdbs_dbs31.pdfusesText_37[PDF] le role de la tension superficielle
[PDF] mesure de la tension superficielle
[PDF] tp tension superficielle
[PDF] role de l'éthanol dans la saponification
[PDF] concordance des temps espagnol tableau
[PDF] concordancia de tiempos verbales en español
[PDF] concordancia de los tiempos en español
[PDF] concordancia de los tiempos ejercicios
[PDF] passé composé imparfait plus que parfait exercices pdf
[PDF] concordance des temps tableau
[PDF] exercices sur la concordance des temps en français pdf
[PDF] concordat sur les entreprises de sécurité test de capacité
[PDF] le concordat définition
[PDF] concordat 1801 definition
