 Chapitre 3 Conductimétrie
Chapitre 3 Conductimétrie
Un dosage par étalonnage conductimétrique permet la détermination d'une concentration Cx d'un soluté ionique en solution aqueuse à partir d'une droite d'
 Fiche 4 : Titrage par suivi conductimétrique
Fiche 4 : Titrage par suivi conductimétrique
- La conductivité d'une solution étant liée à la concentration ionique il faut que l'ajout de solution titrante soit petit devant le volume de solution à
 Quelques notions de conductimétrie
Quelques notions de conductimétrie
(? : conductivité de l'électrolyte en C - Relation entre la conductivité et la mobilité des ions ... et conductivité molaire ionique de l'ion.
 Formule de Kubo: Conductivité électrique
Formule de Kubo: Conductivité électrique
Formule de Kubo: Conductivité électrique. Système d'électrons libres dans un champ électromagnétique : Opérateur courant : dans la jauge de London (Coulomb)
 Dosage des ions cuivre et détermination de la formule de la
Dosage des ions cuivre et détermination de la formule de la
Le comportement de la solution lors de l'ajout de soude est suivi par pH-métrie et conductimétrie. 2. Dosage des ions cuivre(II) dans la solution de sulfate de
 Diffusion quantique et conductivité dans les systèmes apériodiques
Diffusion quantique et conductivité dans les systèmes apériodiques
20 jan. 2003 I.C Lien entre conductivité et diffusion quantique . ... Pour calculer la conductivité on utilise la formule d'Einstein (I.37)
 Conductance et conductivité
Conductance et conductivité
La mesure de la conductivité d'une solution de chlorure de potassium + + ? de concentration C 1-1- Ecrire la formule de chaque solution.
 Techniques danalyse quantitative La conductimétrie
Techniques danalyse quantitative La conductimétrie
La conductimétrie est une méthode d'analyse physique qui est basée sur la mesure de la conductivité d'une solution. La conductivité ?.
 Guide de la mesure de conductivité
Guide de la mesure de conductivité
Cette relation entre la concentration en ions et la capacité de conduire le courant électrique fait de la conductivité une grandeur intéressante à mesurer dans
 Calcul du pH à laide de la mesure de la conductivité cationique
Calcul du pH à laide de la mesure de la conductivité cationique
conductivité est bien connue. La formule finale donne un lien direct entre le logarithme de Cond1 Cond2 et le pH d'une solution d'ammoniac équivalente :.
 [PDF] Chapitre 3 Conductimétrie
[PDF] Chapitre 3 Conductimétrie
Un dosage par étalonnage conductimétrique permet la détermination d'une concentration Cx d'un soluté ionique en solution aqueuse à partir d'une droite d'
 [PDF] Chapitre 4: Conductimétrie
[PDF] Chapitre 4: Conductimétrie
Une cellule de conductimétrie (ci-contre) est constituée de deux plaques (les électrodes) identiques et parallèles reliées à un générateur de tension
 [PDF] Conductance et conductivité - AlloSchool
[PDF] Conductance et conductivité - AlloSchool
1 2- On mesure une conductance = 796 10?6 pour une solution électrolytique Calculer la conductivité en précisant clairement l'unité utilisée
 [PDF] ex08conductimetriepdf
[PDF] ex08conductimetriepdf
1) Donner la formule de la solution 2) Exprimer la conductivité de la solution en fonction des concentrations effectives des ions et de leur
 [PDF] Conductivité Théorie et Pratique - IGZ Instruments
[PDF] Conductivité Théorie et Pratique - IGZ Instruments
Le thème abordé est la mesure de la conductivité c'est-à-dire la capacité d'une solution à transporter un courant électrique Des mesures fiables et exactes
 [PDF] Travaux dirigés : Conductance et Conductivité
[PDF] Travaux dirigés : Conductance et Conductivité
Une cellule conductimétrique est constituée de deux électrodes de surface S nitrate donc un ion nitrate doit porter une charge –e et sa formule est NO3
 [PDF] Quelques notions de conductimétrie - Nicole Cortial
[PDF] Quelques notions de conductimétrie - Nicole Cortial
Remarque : On constate alors que la mobilité de l'ion dépend de l'ion (charge et « taille ») mais aussi du milieu ( )? dans lequel il évolue
 [PDF] Techniques danalyse quantitative La conductimétrie
[PDF] Techniques danalyse quantitative La conductimétrie
18 sept 2016 · Le conductimètre mesure donc la conductance G de la cellule (ou sa résistance R) dont le milieu conducteur est la solution située entre les
 [PDF] Fiche 4 : Titrage par suivi conductimétrique
[PDF] Fiche 4 : Titrage par suivi conductimétrique
Le conductimètre indique la valeur la conductivité ? de la solution (en TP3a : Dosage conductimétrique: acide chlorhydrique par hydroxyde de sodium
 [PDF] Dosage conductimétrique - univ-biskradz
[PDF] Dosage conductimétrique - univ-biskradz
étapes inhérentes `a un dosage par conductimétrie Cependant avant d'exposer la par- 1mol/m3 = 10?3 mol/L et retrouve ainsi la formule :
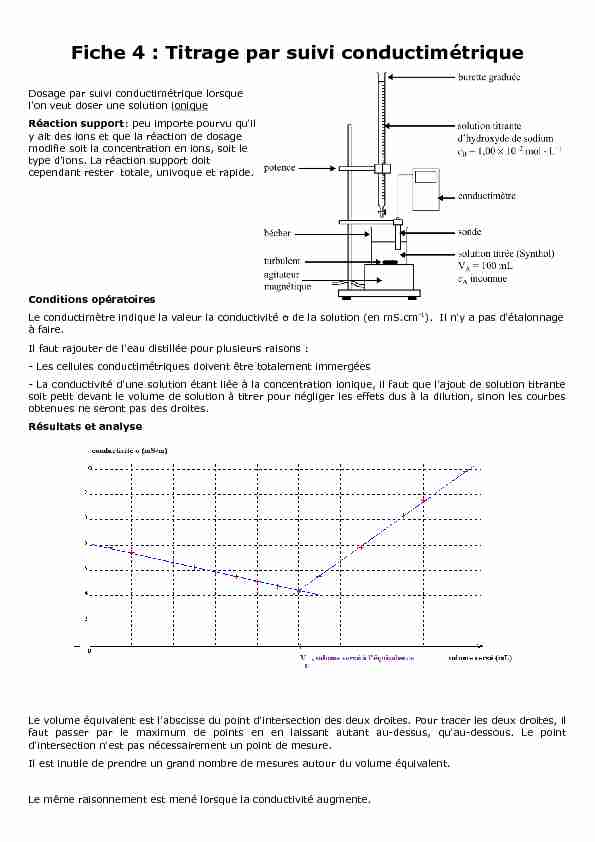
Fiche 4 : Titrage par suivi conductimétrique
Dosage par suivi conductimétrique lorsque
l'on veut doser une solution ioniqueRéaction support: peu importe pourvu qu'il
y ait des ions et que la réaction de dosage modifie soit la concentration en ions, soit le type d'ions. La réaction support doit cependant rester totale, univoque et rapide.Conditions opératoires
Le conductimètre indique la valeur la conductivité σ de la solution (en mS.cm-1). Il n'y a pas d'étalonnage
à faire.
Il faut rajouter de l'eau distillée pour plusieurs raisons : - Les cellules conductimétriques doivent être totalement immergées- La conductivité d'une solution étant liée à la concentration ionique, il faut que l'ajout de solution titrante
soit petit devant le volume de solution à titrer pour négliger les effets dus à la dilution, sinon les courbes
obtenues ne seront pas des droites.Résultats et analyse
Le volume équivalent est l'abscisse du point d'intersection des deux droites. Pour tracer les deux droites, il
faut passer par le maximum de points en en laissant autant au-dessus, qu'au-dessous. Le point d'intersection n'est pas nécessairement un point de mesure. Il est inutile de prendre un grand nombre de mesures autour du volume équivalent. Le même raisonnement est mené lorsque la conductivité augmente. TP3a : Dosage conductimétrique: acide chlorhydrique par hydroxyde de sodium Solution à titrer : acide chlorhydrique : VA = 10 mL CA = 0,25 mol.L-1Solution titrante : soude CB= 0,2 mol.L-1
Indicateur coloré : BBT (non obligatoire)
VE=12,5 mL
réaction support du dosage : HO-(aq)+H3O+(aq)→2H2O(l)Réflexions sur la pente de chaque droite.
Lorsque la conductivité diminue, cela veut dire que : soit il y a moins d'ions dans la solutionssoit qu'un des ions est remplacé par un ion dont la conductivité molaire ionique est plus faible.
Ici :Au début du dosage, les ions H30+ présents dans la solution réagissent avec chaque ion HO- introduit.
Leur concentration diminue donc. En ajoutant une goutte de soude, on ajout des ions hydroxyde quiréagissent avec les ions oxonium présents, mais aussi des ions sodium qui contribuent à la conductivité de
la solution.Tout se passe comme si, chaque ion oxonium était remplacé par ion sodium. La conductivité molaire
ionique des ions H30+ étant 7 fois plus élevée que celle des ions sodium Na+, la conducivité de la solution
baisse.Un fois l'équivalence passée, les ions apportés par la solution titrante participent à la conductivité de la
solution. Celle-ci augmente donc. ionsH30+ Cl-HO-Na+σTP3b : Dosage conductimétrique: vinaigre
Solution à titrer : vinaigre blanc commercial dilué 10 fois VA = 20 mLSolution titrante : soude CB= 0,2 mol.L-1
indicateur coloré : phénolphtaléine (non obligatoire)Volume équivalent : VE= 13,3 mL
Réaction support du dosage :
Réflexions sur la pente de chaque droite.
La réaction du dosage montre qu'à chaque goutte de soude ajoutée, des ionsCH3COO- sont produits. Sont
également ajoutés des ions sodium
Na+. La
conductivité augmente. La droite associéeσ=f(V)a
une pente positive Une fois l'équivalence passée, chaque goutte de soude ajoutée apporte des ionsHO-et des ions sodium. La
conductivité des ionsHO-étant bien plus élevée que
celle des ionsCH3COO-, la conductivité augmente
davantage. La droite associée sur le graphique a une pente plus élevée que celle de la droite avant l'équivalence :Attention : les valeurs indiquées ne correspondent pas à l'expérience faite en TP. Seules l'allure des
courbes est fidèle. ionsCH3COO-HO-Na+σquotesdbs_dbs29.pdfusesText_35[PDF] conductivité de l'eau potable
[PDF] facteur de correction température conductivité
[PDF] influence de la température sur la conductivité de l'eau
[PDF] conversion conductivité salinité
[PDF] conversion ms/cm en g/l
[PDF] conductivité en fonction de la température
[PDF] la conductivité d'une solution
[PDF] mesure de conductivité d'une solution
[PDF] relation conductivité température
[PDF] facteur de correction conductivité
[PDF] conductivité eaux usées domestiques
[PDF] cours conductivité électrique pdf
[PDF] résistivité cuivre ohm mm2 m
[PDF] résistivité cable aluminium
