 1. Mélanges homogènes et hétérogènes (liquide / liquide) 2
1. Mélanges homogènes et hétérogènes (liquide / liquide) 2
Si deux liquides sont non-miscibles alors le mélange est hétérogène. 2. Mélanges homogènes et hétérogènes (solide / eau). Problème : est-ce que tout se
 Chapitre 6 : Mélange
Chapitre 6 : Mélange
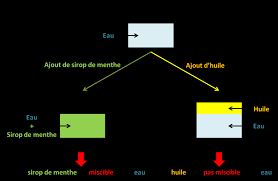
Figure A6.1 : Exemple de mélange liquide-liquide homogène et hétérogène. Page 3. Cours de physique-chimie.
 Mélanges et solutions en cycle 3 (CM1) Éléments de contexte
Mélanges et solutions en cycle 3 (CM1) Éléments de contexte
Mélange homogène/hétérogène. S2 Mélanges homogènes et hétérogènes. (solide On peut peser un bécher vide et un bécher contenant du sel par exemple pour se.
 LES MÉLANGES Eléments de contexte Explorer le monde Explorer
LES MÉLANGES Eléments de contexte Explorer le monde Explorer
mélange d'eau et de sirop par exemple l'eau prend la couleur du sirop alors que ... (mélange hétérogène) & eau + lait (mélange homogène). Bien montrer les ...
 Untitled
Untitled
Classe les mélanges suivants selon qu'ils forment un mélange homogène ou hétérogène. Acier. Eau de piscine. Lau. Jus d'orange avec pulpe.
 dfun mélange homogène
dfun mélange homogène
Exemple : le lirnonène une espèce
 Partie 1 :1. Mélanges homogènes et hétérogènes : liquide/liquide - à
Partie 1 :1. Mélanges homogènes et hétérogènes : liquide/liquide - à
Exemple de trace écrite pour la classe : Certains liquides (comme l'eau et le sirop le jus de fruits et l'eau ) se mélangent : ils sont miscibles. Si après
 Les mélanges
Les mélanges
Les mélanges peuvent être homogènes ou hétérogènes. A Les espèces chimiques. Une espèce chimique est représentée par une unique formule chimique et correspond à
 Mélanges et solutions 1) Les mélanges homogènes et hétérogènes
Mélanges et solutions 1) Les mélanges homogènes et hétérogènes
Si deux liquides sont non-miscibles alors le mélange est hétérogène. Exemples : eau + huile
 Dossier pédagogique Dossier pédagogique
Dossier pédagogique Dossier pédagogique
Le mélange est dit homogène si l'on n'y distingue pas les différentes substances. Sinon il est dit hétérogène. Un mélange qui est homogène à l'œil peut
 1. Mélanges homogènes et hétérogènes (liquide / liquide) 2
1. Mélanges homogènes et hétérogènes (liquide / liquide) 2
Si deux liquides sont non-miscibles alors le mélange est hétérogène. 2. Mélanges homogènes et hétérogènes (solide / eau). Problème : est-ce que tout se mélange
 Les mélanges
Les mélanges
Exemple. Un mélange d'eau et de sucre est homogène : il est impossible de différencier ses constituants à l'œil nu. Définition. Mélange hétérogène.
 CM1-CM2
CM1-CM2
Exemples de mélanges liquides hétérogènes : eau + huile gasoil (pétrole). – Exemples de mélange solide + liquide homogènes : eau. + sel
 dfun mélange homogène
dfun mélange homogène
Exemple : lorsqu'on prépare du thé les arômes et les colorants des feuilles Définir un mélange homogène et un mélange hétérogène (faire des phrases).
 Module 3 Les mélanges et les solutions Temps suggéré: 25 heures
Module 3 Les mélanges et les solutions Temps suggéré: 25 heures
exemples : le pain est un mélange de levure de sucre
 MELANGE ET CORPS PURS bis 18112018
MELANGE ET CORPS PURS bis 18112018
Distinguer mélange homogène et mélange hétérogène Exemple dans le mélange « eau + huile » les constituants sont l'eau et l'huile.
 Présentation PowerPoint
Présentation PowerPoint
Comment passer d'un mélange hétérogène à un mélange homogène? Eau du robinet Par exemple de l'eau pure contient uniquement de l'eau. Eau pure ...
 SCIENCES ET TECHNOLOGIE
SCIENCES ET TECHNOLOGIE
Quelques propriétés de la matière solide ou liquide (par exemple les termes de « mélange hétérogène » et de « mélange homogène » dans une stratégie.
 1. Définir « mélange homogène » et donner trois exemples. Un
1. Définir « mélange homogène » et donner trois exemples. Un
Un mélange hétérogène est un mélange où on distingue à l'œil nu les constituants. Exemple : eau + huile – coca – eau + terre. 2. Donne la définition. Miscible
 Substances pures Mélanges homogènes et mélanges hétérogènes
Substances pures Mélanges homogènes et mélanges hétérogènes
Donnez-moi d'autres exemples! Page 8. Composés: substance pure formée d'au moins deux éléments différents
 [PDF] 1 Mélanges homogènes et hétérogènes (liquide / liquide)
[PDF] 1 Mélanges homogènes et hétérogènes (liquide / liquide)
Si deux liquides sont miscibles alors le mélange est homogène Si deux liquides sont non-miscibles alors le mélange est hétérogène 2 Mélanges homogènes et
 [PDF] Les mélanges ??????? - AlloSchool
[PDF] Les mélanges ??????? - AlloSchool
Un mélange homogène est un mélange dont on ne peut distinguer à l'œil nu les différents constituants Exemples : eau de robinet limonades farine et sucre
 [PDF] élanges homogènes et M :1 1 Leçon n° mélanges hétérogènes
[PDF] élanges homogènes et M :1 1 Leçon n° mélanges hétérogènes
Un mélange peut être : de deux liquides comme l'eau et l'huile d'un liquide et solide comme l'eau et le sable d'un liquide et d'un gaz comme une limonade
 [PDF] Exercices sur les mélanges - Le site de la classe
[PDF] Exercices sur les mélanges - Le site de la classe
Distinguer un mélange homogène d'un mélange hétérogène 1 Un jus de fruit contient des particules (pulpe de fruit) en suspension et visibles à l'œil nu Ce
 [PDF] S2-mÉlanges-et-solutions+CM1pdf - Squarespace
[PDF] S2-mÉlanges-et-solutions+CM1pdf - Squarespace
Quelques exemples de mélanges de ma0ères : • le verre est un mélange homogène d'espèces solides qui ont été?mélangées et chauffées : silice (principal
 [PDF] dfun mélange homogène
[PDF] dfun mélange homogène
Exemple : lorsqu'on prépare du thé les arômes et les colorants des feuilles Définir un mélange homogène et un mélange hétérogène (faire des phrases)
 [PDF] Mélanges et solutions - Fondation LAMAP
[PDF] Mélanges et solutions - Fondation LAMAP
Lorsqu'on parle d'un ensemble hétérogène (eau boueuse fumée) on emploie toujours le terme mélange Dans le cas d'un ensemble homogène solide liquide ou
 [PDF] 1 Matière corps purs et mélanges
[PDF] 1 Matière corps purs et mélanges
Voici quelques exemples de mélanges Indique pour chaque mélange s'il s'agit d'un mélange hétérogène ou homogène ainsi que le nom de ce type de mélange !
 [PDF] les mélanges - PCCL
[PDF] les mélanges - PCCL
Mélange hétérogène : on peut distinguer les différents constituants à l'œil nu Exemple : dans l'orangina on voit la pulpe Mélange homogène : on ne
 [PDF] Les mélanges - Editions Ellipses
[PDF] Les mélanges - Editions Ellipses
Un mélange est hétérogène s'il est possible de distinguer ses différents constituants à l'œil nu ? Exemple Un mélange d'eau et d'huile est hétérogène : on
Quels sont les mélange homogène et hétérogène ?
Un mélange hétérogène est un mélange dont on peut distinguer à l'œil nu au moins deux constituants. Un mélange homogène est un mélange dont on ne peut pas distinguer à l'œil nu les différents constituants. Le mélange d'un solide avec de l'eau est également soit homogène, soit hétérogène.Quelle sont les mélange hétérogène ?
Un mélange hétérogène est un mélange dans lequel on peut distinguer plusieurs composants à l'œil nu ou au microscope. Les mélanges hétérogènes présentent les caractéristiques suivantes : Ils ont plus d'une phase visible. Ces phases sont généralement gazeuses, liquides ou solides.Comment savoir si un mélange est homogène ou hétérogène ?
Si, après avoir agité un mélange de deux liquides, ceux-ci restent distincts, on dit qu'ils sont non miscibles. Si deux liquides sont miscibles alors le mélange est homogène. Si deux liquides sont non-miscibles alors le mélange est hétérogène.- Nous obtenons un mélange homogène. Observations : Le café en poudre ne se dissout pas dans l'eau, cette poudre n'est pas soluble dans l'eau. Nous obtenons un mélange hétérogène. Un mélange est une substance (liquide, solide ou gazeuse) qui contient au moins deux constituants.

Ministère de l'éducation nationale
Académie de Louga : Niveau : 4
ème
Etablissement :
Prénom et NOM
DOMAINE : CHIMIE
CHAPITRE : MELANGES ET CORPS PURS
LEÇON : MELANGES ET CORPS PURS
DUREE : Durée : 6 heures
COMPÉTENCE(S) DE BASES :
§ Utiliser les acquis du cours (mélanges, méthodes de séparation) pour purifier de l'eau prélevée du milieu environnant.§ Utiliser les acquis du cours (mélanges, méthodes de séparation) pour séparer et purifier les
constituants d'un échantillon de matière du milieu environnant dans des cas simples. § Utiliser les acquis du cours (mélanges et corps purs) dans la protection de l'environnement (analyse de la composition de l'air pour déterminer les % en oxygène ; en gaz carbonique....)OBJECTIFS SPÉCIFIQUES :
Ø Distinguer mélange homogène et mélange hétérogène Ø Réaliser quelques méthodes de séparation Ø Caractériser l'eau par ses constantes physiques. Ø Distinguer corps pur simple et corps pur composéØ Donner quelques exemples de mélanges
Ø Distinguer mélange et corps pur simple
LISTING DES PRÉ REQUIS :
Les états de la matière
Le cycle de l'eau
PRÉSENTATION DE LA SITUATION D'APPRENTISSAGE :
ACTIVITÉS PRÉPARATOIRES :
Faire rechercher par les élèves des informations sur : - le traitement de l'eau, - le cycle de l'eau.DEROULEMENT
Résultats attendus (explicitation des OS) :
RESSOURCES PEDAGOGIQUES (MATERIEL/ SUPPORTS/ PRODUITS) : - GU et GP - SP ; livre de sciences physiques USAID- Matériel pour réaliser la décantation, la filtration, la distillation, l'électrolyse, synthèse de l'eau et
l'analyse de l'air. - Produits : eau naturelle et autres types de mélanges.Organisation de la classe: classe entière
DEROULEMENT
I- NOTION DE MELANGE
1- Exemples
Considérons les béchers suivants numérotés de 1 à 4.Eau boueuse
Eau + huile
Eau + sel
Eau + lait
Tous ces béchers contiennent des mélanges.
2- Définition
Un mélange est un ensemble constitué de plusieurs substances. Chaque partie du mélange est appelé constituant. Exemple dans le mélange " eau + huile » les constituants sont l'eau et l'huileII- LES TYPES DE MELANGES
1- Mélange homogène
Un mélange homogène est un mélange dans lequel, il est impossible de distinguer ses différents
constituants à l'oeil nu.Exemples : Eau + sel ; Eau + lait.
2- Mélange hétérogène
Un mélange hétérogène est un mélange dans lequel on peut distinguer au moins deux de ses
constituants à l'oeil nu.Exemples : Eau boueuse ; Eau + huile.
Remarque :
• L'eau et huile ne se méla ngent pas : on dit qu'ell es ne sont pas miscibles. Des gouttes d'huile restent dans l'eau. Le mélange eau + huile forme une émulsion. • L'eau boueuse forme une suspe nsion (particul es soli des en suspension). III- METHODES DE SEPARATION DES CONSTITUANTS D'UN MELANGE1- La décantation
La décantation est un procédé qui consiste à laisser reposer un liquide trouble afin que les
particules solides lourdes se déposent au fond puis à faire un transvasement lent.Eau boueuse salée
particules lourdes2- La filtration
C'est l'opération qui consiste à faire passer un liquide à travers un filtre afin de retenir les
particules légères qu'elle pourrait contenir. Conclusion : L'eau filtrée ou le filtrat ne contient plus de particules en suspension : c'est un mélange homogène.3-La distillation
Pour séparer les constituants d'un mélange homogène liquide, on utilise la distillation - ExpérienceOn chauffe de l'eau salée dans un ballon à fond plat muni d'un tube à dégagement relie à un
réfrigérant. Portées à l'ébullition les vapeurs qui s'y dégagent sont refroidies à l'aide d'un
courant d'eau. Les vapeurs se condensent pour donner de fines gouttelettes d'eau que nouspourrons recueillir dans un autre récipient. A la fin de la distillation, il ne restera dans le ballon
que du sel et on obtient dans l'autre un liquide clair et limpide appelé eau distillée ou distillat
La distillation
Réfrigérant
Distillat
Ballon
Eau salée
Chauffage
Définition : la distillation consiste à faire bouillir le mélange liquide et à condenser ses vapeurs
en les refroidissant : c'est une évaporation suivie d'une condensationEau pure : répétons la distillation avec cette même eau distillée. Celle-ci reste identique à elle
même et il ne restera rien dans le ballon chauffée Donc l'eau distillée ne renferme pas de solides dissoutes, elle est incolore, inodore, et sans saveur : c'est de l'eau pure4-Autres méthodes de séparation
Il existe d'autres méthodes physiques de séparation : le triage, le tamisage, la distillation fractionnée, la congélation fractionnée, le tri magnétique, la centrifugation .........II -NOTIONS DE CORPS PURS
1- Définition
Un corps purs est une substance qu'il est impossible de séparer en d'autres corps par des procèdes de séparation tels que la décantation, la filtration ou la distillationEx : l'eau distillée est un corps pur
2- constantes physiques
Un corps pur est caractérisé par des constantes physiques qui sont : Ø la masse volumique ρ (ro) : c'est le rapport de la masse m du corps par son volume v. (Eau 1g/cm3 fer 7,8 or 19,3 air 1,3kg/m3 cuivre8900kg/m3.)
Ø la température de fusion : c'est la température à partir de laquelle le corps commence à
fondre. (Eau 0° fer 1535 or 1664)Ø la température d'ébullition : c'est la température à partir de laquelle le corps commence
à bouillir. (Eau 100° fer 2750 or 2304)Constantes de l'eau pure
Ø L'eau pure boue à 100° C. Cette t° reste fixe pendant toute la durée de l'ébullition
Ø L'eau pure se solidifie (fond) à 0°.Cette t° reste fixe pendant toute la durée de la
congélation (fusion) Ø La masse volumique de l'eau pure est fixe et vaut 1g/cm3 = 1kg/dm3Distinction entre mélanges et corps pur
Pour un corps pur les constantes physiques (masses volumique, températures de changementd'état .........) sont fixes alors qu'elles sont variables pour un mélange puisqu'elles dépendent
de ses constituants. Ex : la masse volumique de l'eau salée dépend de la quantité de sel dissoute1. Compléter le texte suivant
Lorsqu'on introduit des feuilles de biss ap dans l'eau : on obtie nt a lors un mélange dit.............. . Pour séparer plus tard les feuilles du jus de bissap, on pratique la ................ .
Les feuilles sont retenues par le ............... qui laisse passer le jus appelé ........... et qui est
un mélange ............ .2. Remplir par le mot qui convient
2V 1H 2H 1V 4H 5HHORIZONTALEMENT VERTICALEMENT
1H : méla nge dans lequel, on ne peut pas
distinguer les constituants2H : vaporisation suivie de liquéfaction
3H : procédé de séparation des constituants
d'un mé lange hétérogène liquide-solide en suspension4H : procédé consistant à laisser un mélange
hétérogène se reposer pour sépa rer les constituants5H : particules arrêtées par une paroi poreuse
1V : paroi poreuse
2V : mélange dans lequel on peut distinguer
les constituants 3Hquotesdbs_dbs29.pdfusesText_35[PDF] mers et océans : un monde maritimisé cours
[PDF] mers et océans un monde maritimisé 4eme
[PDF] mers et océans un monde maritimisé carte
[PDF] météorologie et climatologie 5ème svt
[PDF] difference entre climatologie et meteorologie
[PDF] différence entre climat et météo 5eme
[PDF] devoir nombre premier 3eme
[PDF] test maths nombres relatifs
[PDF] devoir pile premiere s
[PDF] devoir physique chimie 1ere s oxydoréduction
[PDF] exercices oxydoréduction 1ère s pdf
[PDF] exercice parallélogramme 6ème
[PDF] kidimath 5ème
[PDF] contrôle aire et périmètre 6ème pdf
