 TP Chimie n° 3
TP Chimie n° 3
- Savoir calculer la concentration molaire la masse volumique et le facteur de dilution de la solution obtenue. 2 Présentation. On dispose d'une solution mère
 Comment préparer une solution de chlore à 05 % (haute
Comment préparer une solution de chlore à 05 % (haute
Ne PAS mettre de solution de chlore dans la bouche ou les yeux. Comment préparer une solution de chlore à 05 % (haute concentration) à partir d'eau de javel.
 Réalisation de dilutions sur lanalyseur de biochimie IDEXX Catalyst
Réalisation de dilutions sur lanalyseur de biochimie IDEXX Catalyst
Quand effectuer une dilution. Vous devez effectuer des dilutions uniquement lorsqu'une valeur de test se situe hors de l'intervalle de valeurs mesurables ou
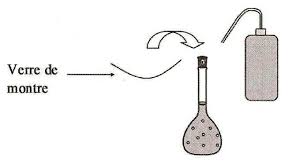 TP-Préparation dune solution de concentration donnée par dilution.
TP-Préparation dune solution de concentration donnée par dilution.
Réaliser une dilution consiste à diminuer la concentration molaire d'une solution en Alors comment faire ? ° A partir du matériel disponible proposer une ...
 FICHE TECHNIQUE Numération des cellules sanguines
FICHE TECHNIQUE Numération des cellules sanguines
- Pipettes réglables / tube pour dilution du sang. - Mélangeur pour les échantillons de sang. - Microscope avec oculaire 10x et objectif 50x ou 60x sans
 Limite de linéarité Importance de la dilution
Limite de linéarité Importance de la dilution
Celle-ci se fait à l'aide du matériel adéquat (pipettes calibrées) et de la solution appropriée (sérum physiologique eau distillée
 Protocole pour réaliser une dilution
Protocole pour réaliser une dilution
Protocole pour réaliser une dilution. Etape 1 : Mettre la solution mère dans un bécher. A l'aide d'une pipette jaugée de Vpipette mL munie d'un dispositif d
 Solvants solutés et règles de dilution
Solvants solutés et règles de dilution
Administration sur une durée précise ou en continu nécessite une dilution en perfusion ou seringue. M'arrêter quand j'ai un doute et de faire vérifier ...
 Comment préparer une solution de chlore à 005 % (faible
Comment préparer une solution de chlore à 005 % (faible
Comment préparer une solution de chlore à 005 % (faible concentration). Assurez-vous de porter l'EPI complémentaire. RA. Mélangez bien pendant 10 secondes
 Protocole de dilution
Protocole de dilution
L'analyseur de biochimie Catalyst Dx* permet de réaliser des dilutions automatisées (il mélange l'échantillon et le diluant pour vous) et des dilutions
 Protocole pour réaliser une dilution
Protocole pour réaliser une dilution
Protocole pour réaliser une dilution. Etape 1 : Mettre la solution mère dans un bécher. A l'aide d'une pipette jaugée de Vpipette mL munie.
 TP-Préparation dune solution de concentration donnée par dilution.
TP-Préparation dune solution de concentration donnée par dilution.
Objectifs : -Connaître le principe d'une dilution Réaliser une dilution consiste à diminuer la concentration molaire d'une ... Alors comment faire ?
 Pousse Seringue Électrique : Reconstitution administration Des
Pousse Seringue Électrique : Reconstitution administration Des
Ampoule de 150 mg/3 ml on va passer une dose de charge de 300 mg en 30 min
 TP Chimie n° 3
TP Chimie n° 3
- Savoir calculer la concentration molaire la masse volumique et le facteur de dilution de la solution obtenue. 2 Présentation. On dispose d'une solution mère
 Solvants solutés et règles de dilution
Solvants solutés et règles de dilution
Indication : véhicule pour la dilution et la reconstitution de médicaments injectables X = 175 mL MAIS ma seringue la plus petite fait 2 mL et est.
 Table pour la dilution de lalcool (Table de Gay-Lussac) appelée
Table pour la dilution de lalcool (Table de Gay-Lussac) appelée
Table pour la dilution de l'alcool (Table de Gay-Lussac) appelée aussi Table de mouillage de l'alcool. Concentration initiale.
 Protocole de dilution
Protocole de dilution
L'analyseur de biochimie Catalyst Dx* permet de réaliser des dilutions automatisées (il mélange l'échantillon et le diluant pour vous) et des dilutions
 Santé-TP n°7 : Préparation dune solution. Dilution
Santé-TP n°7 : Préparation dune solution. Dilution
concentration massique : cm1 = 5
 Réalisation de dilutions sur lanalyseur de biochimie IDEXX Catalyst
Réalisation de dilutions sur lanalyseur de biochimie IDEXX Catalyst
Quand effectuer une dilution. Vous devez effectuer des dilutions uniquement lorsqu'une valeur de test se situe hors de l'intervalle de valeurs mesurables ou
 TDCalculsdoses pediatriquesCORRIGES
TDCalculsdoses pediatriquesCORRIGES
Comment effectuez vous la dilution ? Que faut-il faire pour que Justin reçoive l'intégralité de son traitement ? Corrigé :.
 Comment réaliser des dilutions en série: 9 étapes
Comment réaliser des dilutions en série: 9 étapes
On réalise par dilution différentes solutions de concentration connues de la solution mère On mesure la grandeur (absorbance ou conductivité) On trace la droite de la grandeur en fonction de la concentration On mesure la grandeur pour notre solution inconnue
 Searches related to comment faire une dilution PDF
Searches related to comment faire une dilution PDF
Préparer des solutions par dilution d’une solution 1 But detravail - Savoir utiliser et connaître le matériel adapté à une dilution - Savoir calculer la concentration molaire la masse volumique et le facteur de dilution de la solution obtenue 2 Présentation
Vue d’ensemble
La dilution est le processus qui permet de réaliser une solution moins concentrée à partir d’une solution plus concentrée. Il existe de nombreuses raisons pour lesquelles on pourrait vouloir réaliser une dilution, elles peuvent aller des plus occasionnelles aux plus sérieuses. Par exemple, les biochimistes diluent des solutions à partir de leur forme concentrée pour créer de nouvelles solutions qu’ils vont utiliser dans leurs expérimentations, alors que, dans un tout autre registre, les barmans diluent souvent les alcools forts avec des boissons non alcoolisées ou des jus de fruits pour faire de savoureux cocktails. La formule pour calculer une dilution est C
Diluer précisément les concentrés grâce à l’équation de dilution
Déterminez ce que vous savez et ce que vous ignorez. Faire une dilution en chimie revient la plupart du temps prendre une petite quantité d’une solution dont vous connaissez la concentration, puis à y ajouter une certaine quantité d’un liquide neutre (comme l’eau) pour faire une nouvelle solution avec un volume plus grand, mais une concentration plus faible. On réalise souvent cela dans les labos de chimie, car, dans un souci d’efficacité, les réactifs sont souvent stockés sous de très fortes concentrations qui seront ensuite diluées pour être utilisées dans les expérimentations. Habituellement, dans les situations du quotidien, vous connaitrez la concentration de votre solution de base ainsi que la concentration et le volume que vous voulez dans la deuxième solution, mais pas le volume de la première solution dont vous aurez besoin ici.
Comment calculer la dilution d'une solution ?
La formule est alors : Cfinale = Cinitiale/D, avec Cfinale représentant la concentration terminale de la solution diluée, Cinitiale, la concentration de la solution mère et D, le ratio de la dilution déterminé à l'avance .
Quels sont les objectifs d’une dilution ?
Objectifs : -Connaître le principe d’une dilution -Réaliser des dilutions successives. ajoutant de l’eau (le solvant). ¤ La solution initiale utilisée est appelée la solution mère. Le volume prélevé de la solution mère sera notéViet sa concentration molaire Ci. ¤La solution finale préparée est appelée la solution fille.
Comment préparer une solution de concentration donnée par dilution ?
TP-Préparation d'une solution de concentration donnée par dilution. Objectifs : -Connaître le principe d’une dilution -Réaliser des dilutions successives. ajoutant de l’eau (le solvant). ¤ La solution initiale utilisée est appelée la solution mère. Le volume prélevé de la solution mère sera notéViet sa concentration molaire Ci.
Comment faire une dilution en chimie ?
Faire une dilution en chimie revient la plupart du temps prendre une petite quantité d’une solution dont vous connaissez la concentration, puis à y ajouter une certaine quantité d’un liquide neutre (comme l’eau) pour faire une nouvelle solution avec un volume plus grand, mais une concentration plus faible.
UNIVERSITÉ MENTOURI 1 INSTITU DES SCIENCES VÉTÉRINAIRE DÉPARTEMENT PRÉCLINIC CHIMIE 2018-2019 TP Chimie n° 3 Préparer des solutions par dilution d'une solution. 1 But
travail- Savoir utiliser et connaître le matériel adapté à une dilution. - Savoir calculer la concentration molaire, la masse volumique et le facteur de dilution de la solution obtenue. 2 Prés ntation On dispose d'une solution mère, de concentration connue, à partir de laque lle on prépare une solution fille, moins concentrée. Diluer une solution aqueuse consiste, en lui ajoutant de l'eau distillée, à obtenir une solution moins concentrée. Diluer 10 fois une solution revient à diviser sa concentration par 10, la diluer 100 fois revient à diviser sa concentration par 100. On parle aussi de dilution au dixième, au centième.10 et 100 représente le facteur de dilution. 2.1 Utilisation
'un propip tt (poir'aspiration)Fixer la propipette à la pipette (du côté opposé à la poire). Appuyer sur l'emplacement A et presser sur la poire pour la vider. Une pression sur l'emplacement S permet d'aspirer le liquide. Une pression sur l'emplacement E permet de laisser couler le liquide.
UNIVERSITÉ MENTOURI 1 INSTITU DES SCIENCES VÉTÉRINAIRE DÉPARTEMENT PRÉCLINIC CHIMIE 2018-2019 2.2 Protocol xpérim ntalpourlapréparation
'un solutionpar ilution 3 Matéri l tProuitsMatériel Produits - Béchers - Fiole jaugée de 100 mL - Pipette jaugée de 10 mL ou 20 mL - Pissette d'eau distillée - Alcool à brûler - Eau de Dakin 4 Parti théoriqu • Solution mère Sm : concentration massique Cm • Solution fille à préparer Sf : concentration massique Cf , volume Vf. Il faut d'abord calculer le volume Vm de solution mère à prélever auquel on ajoute de l'eau jusqu'au volume Vf. Lorsqu'on dilue une solution la masse de soluté présent ne change pas • La masse du soluté dans le prélèvement d'un volume Vm de la solution mère est Cm x Vm. • La masse du soluté dans la solution fille sera égale à Cf x Vf • Pour diluer, on ne rajoute que de l'eau à la solution mère, donc la masse de soluté est la même dans la solution mère et la solution fille. On a donc la relation: Cm x Vm = Cf x Vf
UNIVERSITÉ MENTOURI 1 INSTITU DES SCIENCES VÉTÉRINAIRE DÉPARTEMENT PRÉCLINIC CHIMIE 2018-2019 Cm x Vm → masse de soluté dans le prélèvement de solution mère Cf x Vf → masse de soluté dans la solution fille • Le volume Vm de la solution mère à prélever est donc tel que: Vm = Cf x Vf / Cm • Cm et Cf sont exprimés dans la même unité, par exemple en gramme par litre (g.L-1) • Facteur de dilution : F = Cm / Cf = Vf / Vm. 5 Activités5.1 Dilution
'unliqui1- Mesurer la masse m2 d'une fiole jaugée de 100 mL vide. 2- Prélever V1 =10,0 mL d'alcool à brûler commercial avec une pipette jaugée munie de sa propipette. 3- Les introduire dans la fiole jaugée de 100 mL. 4- Ajouter de l'eau distillée aux 2⁄3, homogénéiser, puis ajuster au trait de jauge avec une pissette d'eau distillée. 5- Boucher et agiter doucement pour homogénéiser. On obtient la solution 2. 6- Mesurer la masse m1 de la fiole pleine. Les pesées 7- Déterminer la valeur de la masse volumique de la solution 2
UNIVERSITÉ MENTOURI 1 INSTITU DES SCIENCES VÉTÉRINAIRE DÉPARTEMENT PRÉCLINIC CHIMIE 2018-2019 5.2 Dilution
'un solutionmèr La liqueur de Dakin (ou ea u de Dakin) es t un liqui de antiseptique (bactéricide, fongicide, virucide) utilisé pour le lavage des plaies et des muqueuses, de couleur rose et à l'odeur d'eau de Javel. Elle est composée d'un mélange d'espèces chimiques dont seul le permanganate de potassium (formule KMnO4) est coloré en violet. 1- Vous avez une solution mère S0 de permanganate de potassium de concentration massique Cm = 0,4 g/L en permanganate de potassium. 2- À partir de cette solution mère, vous préparerez 2 solutions fille de concentrations massiques Cm données dans le tableau ci-dessous, chacune de volume Vf = 100,0 mL. Pour les préparer, il faudra introduire un volume Vm de la s olution mère et on complète à 100,0 mL avec de l'eau distillée. Cm = 0,4 g/L , Vf = 100,0 m Solutions filles S1 S2 Cf (g/L) 8 x 10-2 4 x 10-2 Volume Vm de la solution mère à prélever (mL) Facteur de dilution
quotesdbs_dbs5.pdfusesText_9[PDF] tableau de mouillage des alcools pour 1 litre dalcool
[PDF] dilemmes impossible
[PDF] contraction de volume eau alcool
[PDF] exercice spectre ir
[PDF] dilemmes jeu
[PDF] organiser sa classe maternelle
[PDF] vocabulaire voilier
[PDF] quizz égalité homme femme
[PDF] tableau spectre rmn carbone 13
[PDF] table rmn proton
[PDF] activités égalité filles garçons
[PDF] pdf table de déplacement chimique en rmn h
[PDF] jeux de femme et homme dans le lit
[PDF] jeux homme contre femme
