 Kit pGLO de Transgénèse Bactérienne
Kit pGLO de Transgénèse Bactérienne
Le cation Ca2+ de la solution de transformation (50 mM CaCl2 pH 6
 Transformation bactérienne
Transformation bactérienne
Cette bactérie est rendue compétente (capacité à incorporer de l'ADN) par un traitement au CaCl2. Les bactéries compétentes sont d'abord gardées sur la glace ce
 4 : La transformation
4 : La transformation
Cette bactérie est rendue compétente (capacité à incorporer de l'ADN) par un traitement au CaCl2. Les bactéries compétentes sont d'abord gardées sur glace
 TRANSFECTION - Création dun OGM procaryote Comparaison de
TRANSFECTION - Création dun OGM procaryote Comparaison de
Avant sa transformation la bactérie est rendue compétente; c'est à dire que Etaler 100 µL pour le tube traité par la technique au CaCl2 et étaler 100 ou 10 µL ...
 KIT DETPTRANSFORMATIONGENETIQUE
KIT DETPTRANSFORMATIONGENETIQUE
transformation bactérienne en utilisant la bactérie E.Coli et de l'ADN suspension les cellules bactériennes dans la solution CaCl2 en tourbillonnant.
 Initiation aux techniques de biologie moléculaire appliquées à la
Initiation aux techniques de biologie moléculaire appliquées à la
permet la conservation à - 80'C de ces bactéries réparties en aliquots de ZOO pl. 3.5- Transformation. Le mélange de ligation vecteur-insert est ajouté à ZOO pl
 Chapitre III: les transferts génétique 2- La Transformation et la
Chapitre III: les transferts génétique 2- La Transformation et la
nom de transformation à ce changement de bactéries non virulentes en bactéries virulentes CaCl2 qui rend la membrane cellulaire plus perméable au DNA. 4 ...
 Etude des premières étapes de la transformation naturelle chez
Etude des premières étapes de la transformation naturelle chez
5 déc. 2017 pylori lors de l'infection. (Falush et al. 2001). Chez les bactéries
 Couplage de rapporteurs génétiques et dune molécule active pour l
Couplage de rapporteurs génétiques et dune molécule active pour l
CaCl2 les agents chélatants comme l'EDTA et le Dequest 2006
 Compréhension des mécanismes physiologiques et génétiques
Compréhension des mécanismes physiologiques et génétiques
26 févr. 2016 M17 agar 6% supplémentée de CaCl2 10 mM et de glucose à 0
 Kit pGLO de Transgénèse Bactérienne
Kit pGLO de Transgénèse Bactérienne
Le cation Ca2+ de la solution de transformation (50 mM CaCl2 pH 6
 Transformation bactérienne
Transformation bactérienne
Cette bactérie est rendue compétente (capacité à incorporer de l'ADN) par un traitement au CaCl2. Les bactéries compétentes sont d'abord gardées sur la glace ce
 TRANSFECTION - Création dun OGM procaryote Comparaison de
TRANSFECTION - Création dun OGM procaryote Comparaison de
Avant sa transformation la bactérie est rendue compétente; Remettre le culot en suspension dans 10 mL de chlorure de calcium stérile (CaCl2) à 75 mmol.
 Transformation bactérienne avec un plasmide contenant un gène de
Transformation bactérienne avec un plasmide contenant un gène de
Ensuite nous allons vous expliquer la transformation bactérienne. Comment transformer une bactérie avec un plasmide? ... CaCl2 01M. Choc thermique.
 hotes de clonage - Génie Génétique
hotes de clonage - Génie Génétique
Exemple : si le vecteur est un plasmide la cellule hôte est une bactérie. La cellule LA TRANSFORMATION BACTÉRIENNE ... (par CaCl2 par exemple) pour.
 KIT DETPTRANSFORMATIONGENETIQUE
KIT DETPTRANSFORMATIONGENETIQUE
transformation bactérienne en utilisant la bactérie E.Coli et de l'ADN plasmidique. A suspension les cellules bactériennes dans la solution CaCl2 en ...
 Ce document est le fruit dun long travail approuvé par le jury de
Ce document est le fruit dun long travail approuvé par le jury de
La transformation bactérienne est possible lorsque des fragments d'ADN sont libérés par la lyse d'une cellule et sont captés par une cellule réceptrice avant
 4 : La transformation
4 : La transformation
Cette bactérie est rendue compétente (capacité à incorporer de l'ADN) par un traitement au CaCl2. Les bactéries compétentes sont.
 4-Matériels et méthodes.
4-Matériels et méthodes.
ce plasmide inactive le gène lacZ la bactérie est alors incapable de produire de la MgSO4 1M ; 20 ml de glucose 20% ; 1 ml de CaCl2 0
 Rôles du calcium et des transports ioniques de lépithélium des
Rôles du calcium et des transports ioniques de lépithélium des
22 mai 2009 Effets de la bactérie Pseudomonas aeruginosa sur les cellules ... Manipulation en solution Krebs (NaCl 140 mM KCl 5 mM
 Transformation of Escherichia coli Made Competent by Calcium
Transformation of Escherichia coli Made Competent by Calcium
transformation is frequently used to clone and amplify a fragment of a gene a whole gene or an entire DNA library Transformation of cells with DNA is an invaluable technique that provides scientists with a w ay to introduce and manipulate genes Theory Since E coli is not naturally transformable the ability to take up DNA or
 5 Transformation bactérienne
5 Transformation bactérienne
Introduction Dans l'expérience proposée nous allons transformer Escherichia coli Cette bactérie est rendue compétente (capacité à incorporer de l'ADN) par un traitement au CaCl2 Les bactéries compétentes sont d'abord gardées sur la glace ce qui fige les membranes L'ADN ajouté se fixe sur les bactéries
Introduction
Competent cells are bacterial cells that can accept extra-chromosomal DNA or plasmids (naked DNA) from the environment. The generation of competent cells may occur by two methods: natural competence and artificial competence. Natural competence is the genetic ability of a bacterium to receive environmental DNA under natural or in vitro conditions. ...
Principle
As DNA is a highly hydrophilic molecule, normally it cannot pass through the cell membrane of bacteria. Hence, in order to make bacteria capable of internalizing the genetic material, they must be made competent to take up the DNA. This can be achieved by making small holes in bacterial cells by suspending them in a solution containing a high conce...
Natural Competence
Bacteria are able to take up DNA from their environment by three ways; conjugation, transformation, and transduction. In transformation, the DNA is directly entered into the cell. Uptake of transforming DNA requires the recipient cells to be in a specialized physiological state called competent state. Natural competence was first discovered by Fred...
Artificial Competence and Transformation
Artificial competence is not encoded in the cell’s genes. Instead, it is a laboratory procedure by which cells are made permeable to DNA, with conditions that do not normally occur in nature. This procedure is comparatively easy and simple, and can be used in the genetic engineering of bacteria but in general transformation efficiency is low. Metho...
Reagents Required and Their Role Luria-Bertani Broth
Luria-Bertani (LB) broth is a rich medium that permits fast growth and good growth yields for many species including E. coli. It is the most commonly used medium in microbiology and molecular biology studies for E. coli cell cultures. Easy preparation, fast growth of most E. coli strains, ready availability and simple compositions contribute to the...
Does storing cells in CaCl2 increase transformation efficiency?
Holding cells in CaCl2 at 4°C will, in fact, increase transformation efficiency although this declines with more than 24 h storage. Long periods of storage can be achieved by freezing the competent cells. The revival step is necessary both to allow the plasmid establishment and to allow expression of the resistance genes.
What is CaCl2 treatment?
It is one of the most reliable techniques of transformation; however, for different bacterial species and strains, owing to the differences in their surface properties, certain conditions need to be adjusted and optimized accordingly. CaCl2 treatment ensures the competency of bacterial cells for the uptake of foreign DNA.
What is Escherichia coli plasmid transformation with deoxyribonucleic acid?
Transformation of Escherichia coli with plasmid deoxyribonucleic acid: calcium-induced binding of deoxyribonucleic acid to whole cells and to isolated membrane fractions. J. Bacteriol. 145, 780–787. Yoshida, N., and Sato, M. (2009). Plasmid uptake by bacteria: a comparison of methods and efficiencies. Appl. Microbiol.
What is the most effective chemical treatment for bacterial transformation?
This chapter focuses on bacterial transformation using CaCl2 as the most effective chemical treatment to bring about transformation.
Laboratoire de biologie 4OS
Transformation bactérienne
La transgenèse est l'addition d'un ou de plusieurs gènes étrangers dans une cellule. Lenouveau gène introduit est appelé transgène qui peut, s'il est exprimé, conférer de nouvelles
caractéristiques à la cellule. La transformation de bactéries fut décrite la première fois par Griffith
en 1928, puis plus tard par Avery qui démontra que l'ADN était le "principe transformante" capable
de rendre des souches de Streptococcus pneumoniae virulentes.Thèmes: tra nsgenèse, bioluminescence, sélection de bactéries, résistances aux antibiotiques,
β-lactamase, formation de colonies sur boîtes de pétri.Introduction
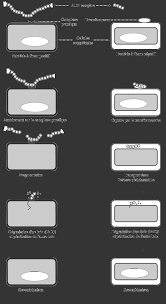
Dans l'expérience proposée, nous allons transformer Escherichia coli. Cette bactérie estrendue compétente (capacité à incorporer de l'ADN) par un traitement au CaCl2. Les bactéries
compétentes sont d'abord gardées sur la glace ce qui fige les membranes. L'ADN ajouté se fixe sur
les bactéries. Un passage à 42°C restaure la fluidité des membranes permettant l'incorporation de
l'ADN. Les bactéries sont ensuite cultivées une trentaine de minutes afin de permettre l'expression
du gène de résistance nouvellement incorporé. Enfin ces bactéries son étalées sur un milieu sélectif
(permettant la croissance des cellules qui ont incorporé l'ADN). L'ADN utilisé est n plasmide. Il
s'agit d'éléments extra-chromosomiques circulaires capables de se répliquer (de 1 à 100 copies) dans
la bactérie et d'être transmis dans les cellules filles lors de divisions cellulaires. Dans la nature, les
plasmides peuvent être échangés entre différentes espèces de bactéries. Ces plasmides peuvent
disséminer ainsi de nouvelles caractéristiques tels que des résistances aux antibiotiques, à des
métaux-lourd, ou encore de rendre les bactéries virulentes.Les plasmide lux117
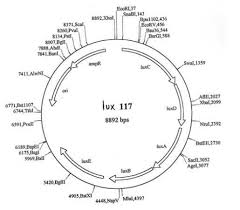
Pour cette expérience nous allons utiliser le plasmide lux117 (voir figure). Celui-ci contientune origine de réplication (ori), un gène de résistance à l'antibiotique ampiciline (ampR) ainsi que
l'opéron lux, (un opéron est une unité de transcription) provenant de la bactérie Vibrio harveyi. Cet
opéron contient 5 gènes, luxA à luxE. Ils codent pour les protéines impliquées dans la réaction de
bioluminescence. Le gène ampR code pour une enzyme (la β-lactamase) capable d'inactiver lesantibiotiques de la famille des pénicillines en clivant une liaison du noyau β-lactamase (voir
figure). Seules les bactéries possédant le gène ampR sont capables de croître sur un milieu
contenant de l'ampicilline (antibiotique de la famille des pénicillines)Carte de restriction du plasmide lux117.
La taille de ce plasmide est de 8892 paires de bases. Les sites de restriction et leurs localisations (en paires de bases) sur le plasmide sont indiqués. Ce plasmide contient une origine de réplication (ori), un gène de résistance à l'ampicilline (ampR) et l'opéron lux, codant pour les deux sous-unités de la luciférase (luxA et luxB) et pour les enzymes impliquées dans la production de cofacte urs néce ssair es à la réaction de bioluminescence (luxC, luxD et luxE). Clivage du noyau β-lactamase de la pénicilline par la β-lactamaseLa bioluminescence
La luci férase bactérienne est une enzy me contenant 2 sous-unités (α e t β) codées
respectivement par les gènes luxA et luxB. Les gènes luxC, luxD et luxE codent pour de protéines
impliquées dans la conversion d'acides gras en une longue chaîne d'aldéhyde nécessaire à la
réaction de luminescen ce . L a bi oluminescence est observée dans des milliers d' espè cesd'organismes vivants tels que bacté ries , protozoaires, cham pignons, annélides, cni dai res,
mollusques, insectes et poisons. Le rôle de la bioluminescence varie suivant ces organismes, On note 4 fonctions principales: l'éclairage, l'appât, la protection et la communication. Historiquement, la bioluminescence est un phénomène connu depuis l'antiquité. Aristote(348 - 322 av JC) parlait déjà de lumière émise par des poissons morts et de moisissures. À partir
de 1600 diverses recherches permirent d'établir que cette réaction mettait en jeu une enzyme (la
luciférase), un substrat oxydable (la luciférine) ainsi que l'oxygène. Les enzymes et substrats utilisés
pour les réactions de bioluminescence sont extrêmement variés d'un organisme à l'autre. Chez les
bactéries, la luciférase catalyse l'oxydation de la riboflavine mononucléotide réduite (FMNH2) et
une longue chaîne d'aldéhyde (R-CHO), générant une flavine oxydée (FMN), un acide gras (R-
COOH), de l'eau (H2O) et de la lumière (490 - 500 nm). La réaction est la suivante: R-CHO + FMNH2 + O2 FMN + R-COOH + H2O +L'expérience
1) préparation des cellules compétentes:
Le protocole présenté ici est simplifié mais permet néanmoins d'obtenir une efficacité de
transformation suffisante pour l'expérience proposée. Il est important que les élèves puissent se
rendre compte de toutes les étapes nécessaires au déroulement de l'expérience. Si toutefois, pour
des raisons techniques, il ne vous est pas possible de préparer des cellules compétentes nous pouvons vous en fournir.• Prendre une culture d'une nuit de bactéries Escherichia coli (DH5α). Diluer cette culture 100
fois dans 40 ml de milieu LB dans un Erlenmeyer de 250 ml. Agiter vigoureusement à 37°C .• Après environ 3 heures, vérifier la densité optique de la culture. Quand la densité optique
(OD600) est entre 0.5 et 0.6, mettre l'Erlenmeyer contenant les bactéries dans la glace.• Prélever 1.5 ml de culture et les transférer dans 1 tube Eppendorf 1.5 ml. Marquer ce tube
avec un +. Prélever 1.5 ml dans un autre tube Eppendorf. Marquer ce tube avec un -. L'ADN sera mis dans le tube marqué +. Le tube marqué - servira de contrôle.• Centrifuger les tubes Eppendorf 30 secondes à vitesse maximale pour faire tomber les cellules.
• Jeter le surnageant.• Ajouter 1 ml de CaCl2 0.05M froid sur le culot et le resuspendre en utilisant la pipette P1000.
Attention, il faut pipeter doucement et éviter d'aspirer les cellules dans la pipette elle-même.
• Centrifuger les tubes comme avant. Jeter le surnageant et resuspendre le culot de cellules dans
100 μl de CaCl2 0.05M froid.
• Les bactéries sont gardées sur la glace et sont maintenant prêtes à l'emploi ("compétentes"
pour la transformation). • Il est important que les solutions et les tubes soient gardés sur glace.2) la transformation:
• Ajouter 8 μl d'ADN dans le tube marqué +. • Mettre le tube marqué + et le tube marqué - sur la glace pendant 15 minutes. • Incuber les tubes deux minutes à 42°C (choc thermique) • Replacer les tubes dans la glace pendant 5 minutes.• Ajouter 1 ml de LB et incuber la suspension à 37°C pendant 30 minutes (pour l'expression de
la résistance à l'ampicilline). • Déposer et étaler: • 0.1 ml du tube + sur une boîte LA + Amp • 0.1 ml du tube + sur une boîte LA • 0.1 ml du tube - sur une boîte LA+ Amp, • 0.1 ml du tube - sur une boîte LA • Centrifuger le reste de la suspension 30 secondes à vitesse maximale pour faire tomber les cellules. • Enlever 0.7 ml de surnageant et le jeter. • Resuspendre le culot avec le reste (~ 0.1 ml) du surnageant • Déposer et étaler ces 0.1 ml sur une boite LA+Amp.• Mettre les boîtes à 37°C pendant 24 h. Les boîtes peuvent ensuite être gardées au frigo (4°C) et
incubées la nuit à 37°C avant de les observer en classe.Attention: Marquer les boîtes sur le fond (et non sur le couvercle) avec votre nom, le numéro de
l'expérience et le numéro du tube. Mettre les boîtes à l'envers dans l'étuve à 37°C.
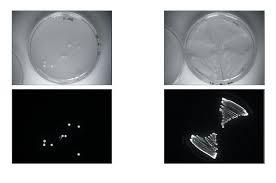
3) Résultats:
• Regarder le nombre de colonies obtenues sur chacune des boîtes et discuter des résultats
• Observer les boîtes à l'obscurité et discuter de l'expérience:Voici des exemples de ce que l'on peut observer:
Matériel:
• Pipettes p20 et embouts stériles • Pipettes p200 et embouts stériles • Pipettes p1000 et embouts stériles • Pipettes pasteur pour étalement • Bechers pour ethanol • Microcentrifugeuse • Bain-Marie 37°C • Bain-Marie 42°C • Tubes à réaction (Eppendorf 1.5ml) • Ethanol pour étalement • H2O stérile • plasmide lux117 • 2 Boîtes de Petri LA • 2 Boîtes de Petri LA+Amp • 0.5M CaCl2 (solution 10x, à diluer dans de l'H2O stérile) • Bec bunsen • Spectrophotomètre (en option) • Cuvettes (en option)Cette expérience a été initialement mise en place par C. Béguin et M. Goldschmidt-Clermont
quotesdbs_dbs11.pdfusesText_17[PDF] transformer les subordonnées relatives en adjectifs
[PDF] complément de phrase
[PDF] iso 26000
[PDF] principe équateur
[PDF] subordonnée relative exemple
[PDF] l'appel de la foret jack london
[PDF] قانون العقار في المغرب 2017
[PDF] avis de deces
[PDF] la relative déterminative et explicative pdf
[PDF] les pronoms relatifs et leurs fonctions
[PDF] fonction du pronom relatif dont
[PDF] didactique de l'oral et de l'écrit
[PDF] les difficultés de loral chez les apprenants marocains
[PDF] influence du surréalisme
