 Mesure de la teneur en alcool
Mesure de la teneur en alcool
Ce qui cor- respondrait au titre alcoométrique volumique probable (degré potentiel) de ce moût si la fermentation alcoolique n'avait pas commencé. Cependant il
 Table de correspondance* des différentes échelles de mesure de la
Table de correspondance* des différentes échelles de mesure de la
Titre Alcoométrique Potentiel en fonction du rendement en alcool. (sucres pour 1% vol.d'alcool). Degré. Brix. Densité. Degré. Oechslé. Degré.
 Alcool : connaître ses limites : guide pratique dévaluation de sa
Alcool : connaître ses limites : guide pratique dévaluation de sa
même si vous ne devenez jamais dépendant à l'alcool. Vous pouvez mesurer facilement votre consommation d'alcool en ... comment et pourquoi le faire.
 Détermination du degré alcoolique dun vin 4pts
Détermination du degré alcoolique dun vin 4pts
Le degré alcoolique d'un vin est le pourcentage volumique d'alcool mesuré à une Cet exemple montre que le degré du vin augmente avec la température.
 Détermination de la date des vendange
Détermination de la date des vendange
Il est utilisé pour la mesure de la teneur en sucre des jus de raisin. La valeur approximative de leur degré alcoolique est lue directement sur l'instrument
 Maîtrise de la teneur en alcool des vins
Maîtrise de la teneur en alcool des vins
par un degré alcoolique trop élevé (12 à 14 voire 15 % vol.) Cet examen comprend la mesure de l'aptitude à la multiplication végétative des tests de.
 Lalcool dans le corps – effets et élimination
Lalcool dans le corps – effets et élimination
Un outil pédagogique destiné aux enseignant-e-s du degré secondaire partie de l'alcool au fur et à mesure. En moyenne le ... comment se manifestent.
 Lanalyse du vin
Lanalyse du vin
2. DÉTERMINATION DU DEGRÉ ALCOOLIQUE PAR ARÉOMÉTRIE. Le degré alcoolique légal est le pourcentage volumique d'alcool mesuré à une température de 20°C.
 La fabrication maîtrisée des hydromels
La fabrication maîtrisée des hydromels
Il permet de mesurer l'acidité gustative des liquides. Les levures utilisées déterminent le degré d'alcool final maximal de l'hydromel.
 Caractère combustible dun stockage de bouteilles de vin DRA 31
Caractère combustible dun stockage de bouteilles de vin DRA 31
6 janv. 2005 3.2.2 Combustibilité du vin selon le degré d'alcool. ... L'inflammabilité définie par la mesure du point d'éclair du liquide
 [PDF] Mesure de la teneur en alcool
[PDF] Mesure de la teneur en alcool
DIFFÉRENCE ENTRE DEGRÉ POTENTIEL DEGRÉ ACQUIS ET DEGRÉ TOTAL 285 4 INTÉRÉT ET LIMITE DE LA MESURE DU TAV PAR ÉBULLIOMÉTRIE 286
 [PDF] Détermination du degré alcoolique dun vin 4pts
[PDF] Détermination du degré alcoolique dun vin 4pts
A 21°C l'alcoomètre indiquera une valeur supérieure à 12° Il faut donc ajouter 019 au degré indiqué sur l'étiquette A 21°C l'alcoomètre indiquerait 12
 [PDF] Titre alcoométrique volumique - OIV
[PDF] Titre alcoométrique volumique - OIV
La masse volumique "?" exprimée en kilogrammes par mètre cube (kg/m³) d'un mélange d'alcool éthylique et d'eau à la température t exprimée en degrés Celsius
 [PDF] Détermination du titre alcoométrique volumique réel par densimétrie
[PDF] Détermination du titre alcoométrique volumique réel par densimétrie
Le titre alcoométrique des boissons spiritueuses peut être mesuré par densimétrie sur balance hydrostatique suivant le principe d'Archimède selon
 Mesure de la teneur en alcool - PDF Free Download - DocPlayerfr
Mesure de la teneur en alcool - PDF Free Download - DocPlayerfr
«degré hecto» ; en conséquence le prix du vin est proportionnel à son taux d alcool : ainsi dans une catégorie de vin donnée plus le vin est alcoolisé
 Séparation et identification despèces chimiques : Comment mesure
Séparation et identification despèces chimiques : Comment mesure
23 déc 2008 · Comment mesure-t-on le degré en alcool du vin ? Utilisation et principe de fonctionnement d'un densimètre ou aréomètre d'Antoine Baumé
 Degré dalcool - Wikipédia
Degré dalcool - Wikipédia
Un hydromètre ou densimètre directement gradué en degrés d'alcool est plongé dans le liquide La mesure lue est corrigée en fonction de la température du
 [PDF] Table de correspondance* des différentes échelles de mesure de la
[PDF] Table de correspondance* des différentes échelles de mesure de la
Titre Alcoométrique Potentiel en fonction du rendement en alcool (sucres pour 1 vol d'alcool) Degré Brix Densité Degré Oechslé Degré
 [PDF] Maîtrise de la teneur en alcool des vins
[PDF] Maîtrise de la teneur en alcool des vins
Le vin est analysé pour les paramètres suivants : degré alcoolique SO2 libre et total sucres résiduels acidité totale et pour les rouges IPT et intensité
Comment se mesure le degré d'alcool ?
Un hydromètre ou densimètre directement gradué en degrés d'alcool est plongé dans le liquide. La mesure lue est corrigée en fonction de la température du liquide. Les tables de densité et de correction selon la température ont été établies expérimentalement par Gay-Lussac.Comment mesurer le degré d'alcool sans appareil ?
Instructions
1Mesurez environ une tasse de moût (ou de bière finie).2Remplissez le tube de l'hydromètre jusqu'à environ 5 cm du haut.3Insérez l'hydromètre. 4Regardez où le liquide croise les marques de l'hydromètre. 5Enregistrez la lecture de la gravité. 6Ajustez la mesure de gravité en fonction de la température.- Alcoomètre: Avec un alcoomètre on peut mesurer tous les mélanges contenant de l'alcool et de l'eau.La profondeur de la plonge de l'alcoomètre dépend du poids spécifique du mélange. Vous pouvez utiliser l'alcoomètre dans tous les distillat (eau-de-vie, Whisky, Vodka, Cognac, etc.)
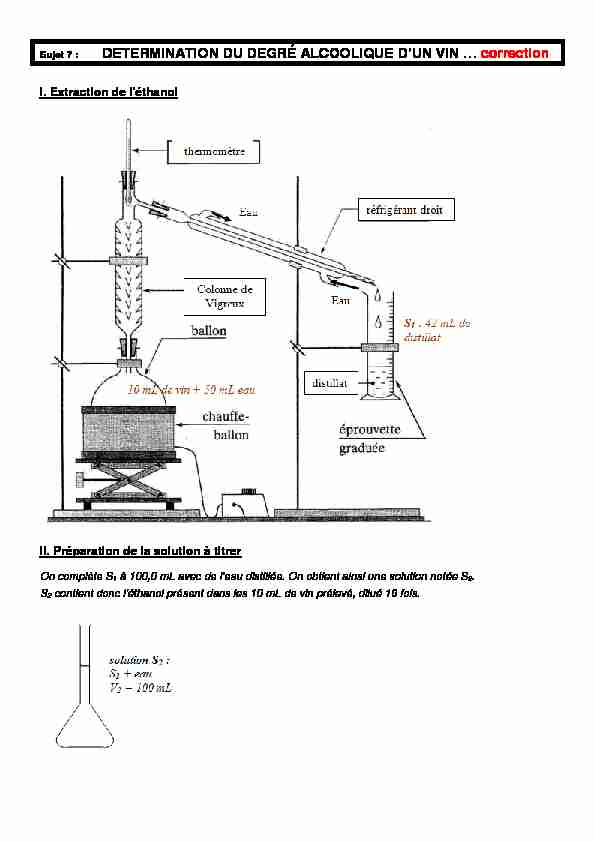 Sujet 7 : DETERMINATION DU DEGRÉ ALCOOLIQUE D'UN VIN ... correction
Sujet 7 : DETERMINATION DU DEGRÉ ALCOOLIQUE D'UN VIN ... correction I. Extraction de l'éthanol
II. Préparation de la solution à titrer
On complète S
1 à 100,0 mL avec de l'eau distillée. On obtient ainsi une solution notée S 2 S 2 contient donc l'éthanol présent dans les 10 mL de vin prélevé, dilué 10 fois. III. Réaction entre l'éthanol et le dichromate de potassiumIII.1. La solution S
3 possède une coloration verdâtre en raison de la présence des ions Cr 3+ qui se sont formés au cours de la transformation.III.2. L'éthanol est une espèce chimique volatile, des vapeurs d'éthanol peuvent se répandre dans le
laboratoire. Or ces vapeurs sont facilement inflammables, même à température ambiante. Les ions dichromate sont cancérigènes, il faut éviter leu r contact.Ce réactif n'est plus utilisé en lycée,
mais encore utilisé dans les alcootests.L'acide éthanoïque qui se forme est irritant pour les voies respiratoires, en bouchant l'erlenmeyer on évite
de respirer des vapeurs.III.3.
équation chimiqu
e 2 Cr 2 O 7 2- + 16 H 3 O + 3 CH 3 -CH 2OH = 4 Cr
3+ + 27 H 2O + 3 CH
3 COOHÉtat du
systèmeAvancemen
t (mol)Quantités de matière (mol)
État initial x = 0 C
1 .V 1 beaucoup n 00 beaucoup 0
En cours de
transformation x C 1 .V 1 - 2x beaucoup n 0 - 3x 4x beaucoup 3xÉtat final x
final n(Cr 2 O 7 2- restant beaucoup n 0 - 3x final 0 4x final 3 4 n 0 beaucoup 3x final = n 0 Cr 2 O 72-est en excès donc l'éthanol est le réactif limitant, il est totalement consommé. On a n 0 - 3x final = 0 donc x final 3 0 n ; on a alors n(Cr 2 O 72-
restant = C 1 .V 1 - 2x final = C 1 .V 1 3 2 n 0
IV DOSAGE DE L'EXCES DU DICHROMATE DE POTASSIUM.
IV.1.équation chimique Cr
2 O 72-+ 14 H 3 O + 6 Fe 2+ = 2 Cr 3+ + 21 H 2
O + 6 Fe
3État du
systèmeAvancemen
t (mol)Quantités de matière (mol)
État initial x = 0
n(Cr 2 O 7 2- restant = C 1 V 1 32n 0 beaucoup C 2 .V 2
0 beaucoup 0
En cours de
transformation x C 1 V 1 3 2 n 0 x beaucoup C2 .V 26x 2x beaucoup 6x
État final x
final0 beaucoup 0 beaucoup
Solution S
3 V 0 = 10,0 mL de solution S 2 V 1 = 20,0 mL de (2K +(aq) + Cr 2 O72-(aq)
) C 11,00.10
-1 mol.L -1 + 10 mL d'acide sulfurique concentré Lorsque l'équivalence est atteinte les réactifs sont totalement consommés.Pour les ions dichromate : C
1quotesdbs_dbs33.pdfusesText_39[PDF] détermination du degré alcoolique d'un vin correction
[PDF] compte rendu dosage de l'acidité d'un vinaigre
[PDF] tp dosage d'un vinaigre
[PDF] tp chimie dosage de l'acidité d'un vinaigre
[PDF] calculer le degré d'acidité du vinaigre étudié
[PDF] dosage de l'acidité du vinaigre commercial
[PDF] combien de verre d'alcool peut on boire pour conduire
[PDF] nombre de verre autorisé pour conduire
[PDF] a partir de quelle quantite d alcool est on alcoolique
[PDF] sortes de rhum
[PDF] rhum pdf
[PDF] pays producteur de rhum
[PDF] quel est le meilleur rhum du monde
[PDF] different type de rhume
