 Construction du diagramme binaire isobare eau-propan-1-ol
Construction du diagramme binaire isobare eau-propan-1-ol
This article introduces some practical work whose goal is to draw the temperature-composition phase diagram of water-propanol. The values obtained make it
 TP : Diagramme binaire
TP : Diagramme binaire
Nous allons dans ce TP
 Binaire eau/propan-1-ol
Binaire eau/propan-1-ol
m eau (g). 20 19 16 12 8 6 4 2 1 05 0 m propanol (g) 0 1 4 8 12 14 16 18 19 19
 SYSTEMES BINAIRES A LEQUILIBRE LIQUIDE / VAPEUR
SYSTEMES BINAIRES A LEQUILIBRE LIQUIDE / VAPEUR
1-C LES DIAGRAMMES BINAIRES DE L'EQUILIBRE LIQ / VAP EN Voici le diagramme binaire isobare sous 1 bar du mélange eau / 2- méthyl propan-1 ol en xol .
 Compte-rendu TP1 Mélange binaire : diagramme de phases isobare
Compte-rendu TP1 Mélange binaire : diagramme de phases isobare
24 nov. 2014 Pour pouvoir tracer le diagramme binaire eau-propanol nous avons mesuré l'indice de réfraction de différents mélanges de compositions connues.
 Diagrammes Binaires: Equilibres Liquide - Vapeur
Diagrammes Binaires: Equilibres Liquide - Vapeur
Le mélange de composition xz est appelé azéotrope. Il bout et se condense à la température fixe Tz comme un corps pur. binaire isobare eau-propanol.
 Cet ouvrage fait partie de la collection « Classe prépa » une
Cet ouvrage fait partie de la collection « Classe prépa » une
Diagramme d'équilibre isotherme liquide-vapeur d'un mélange binaire idéal ... 1 ωHCl. –. --------------------mH2O. = = mHCl. 036. 1 0
 DS 2 – 10 octobre 2015 Diagrammes binaires liquide-vapeur
DS 2 – 10 octobre 2015 Diagrammes binaires liquide-vapeur
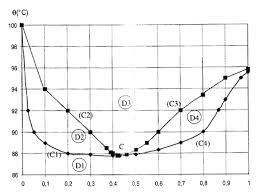
On donne ci-dessous le diagramme de phases du mélange binaire eau-propan-1-ol à pression atmosphérique constante. = 1013 . Il indique la température en.
 Compressibilites de leau et du benzene dans tout le domaine de
Compressibilites de leau et du benzene dans tout le domaine de
selon le cas le melange binaire eau + 2-propanol (W + P) ou 2- propanol + diagramme de phase et de type eau dans l'huile dans la rtgion riche en B
 Azéotrope
Azéotrope
1. Diagramme isotherme : Le diagramme isobare de deux liquides a l'allure Diagramme binaire eau-propanol. On donne en fonction de la fraction molaire ...
 Construction du diagramme binaire isobare eau-propan-1-ol
Construction du diagramme binaire isobare eau-propan-1-ol
Diagramme binaire distillation
 TP : Diagramme binaire
TP : Diagramme binaire
Nous allons dans ce TP
 E binaires
E binaires
A et B constituent un binaire liquide-vapeur idéal ; à une température T 3) Tracer le diagramme isotherme d'équilibre des mélanges eau-propanol à 25°C.
 Mélanges et transformations Diagrammes binaires liquide-vapeur
Mélanges et transformations Diagrammes binaires liquide-vapeur
L'eau (1) et le pentan-1-ol (2) forment un mélange non idéal. Le diagramme isobare du mélange binaire formé par le propan-2-ol C3H8O (noté (2)) et du ...
 Azéotrope
Azéotrope
2. Diagramme binaire eau-propanol. On donne en fonction de la fraction molaire en propanol dans le liquide x2
 DS 2 – 10 octobre 2015 Diagrammes binaires liquide-vapeur
DS 2 – 10 octobre 2015 Diagrammes binaires liquide-vapeur
1 – Epaisseur de zinc déposé sur une rondelle métallique (E3A 2015) On donne ci-dessous le diagramme de phases du mélange binaire eau-propan-1-ol à.
 Oraux CCINP-2019 Lépreuve orale de chimie se focalisera
Oraux CCINP-2019 Lépreuve orale de chimie se focalisera
B) Exercice : Différents diagrammes binaires eau-alcool 3) Donner l'allure du diagramme binaire isobare (1 bar) eau/propan-1-ol sachant que la miscibili ...
 Mélanges et transformations Diagrammes binaires liquide-vapeur
Mélanges et transformations Diagrammes binaires liquide-vapeur
L'eau (1) et le pentan-1-ol (2) forment un mélange non idéal. Le diagramme isobare du mélange binaire formé par le propan-2-ol C3H8O (noté (2)) et du ...
 Cet ouvrage fait partie de la collection « Classe prépa » une
Cet ouvrage fait partie de la collection « Classe prépa » une
3 - Diagramme d'équilibre isobare liquide-vapeur d'un mélange binaire . Construire le diagramme binaire eau – propan-1-ol et préciser la nature des.
 TD T5A Etude des équilibres liquide-vapeur des mélanges binaires
TD T5A Etude des équilibres liquide-vapeur des mélanges binaires
1/ D'après les courbes prévoir le type de mélange liquide que forment l'eau et le propan-1-ol. 2/ Tracer le diagramme binaire liquide-vapeur isobare de ce
 [PDF] Construction du diagramme binaire isobare eau-propan-1-ol
[PDF] Construction du diagramme binaire isobare eau-propan-1-ol
Dans cet article est proposé un TP simple qui permet d'obtenir le diagramme binaire liquide-vapeur isobare (à pression atmosphérique) entre l'eau et le propan-
 Diagrame Binaire Eau Propanol PDF Diagramme de phase - Scribd
Diagrame Binaire Eau Propanol PDF Diagramme de phase - Scribd
Cet article prsente un TP dont lobjet est la construction du diagramme binaire isobare eau-propanol Les valeurs obtenues permettent dtudier la distillation
 [PDF] TP : Diagramme binaire
[PDF] TP : Diagramme binaire
Nous allons dans ce TP tracer le diagramme binaire d'un mélange liquide eau-propanol Le propanol de formule CH3 ? CH2 ? CH2OH est un liquide de
 [PDF] Mélanges et transformations Diagrammes binaires liquide-vapeur
[PDF] Mélanges et transformations Diagrammes binaires liquide-vapeur
Le diagramme isobare du mélange binaire formé par le propan-2-ol C3H8O (noté (2)) et du 2-méthylpropan-1-ol C4H10O (noté (1)) est donné ci-dessous La
 [PDF] P1) Binaire liquide vapeur idéal
[PDF] P1) Binaire liquide vapeur idéal
3) Tracer le diagramme isotherme d'équilibre des mélanges eau-propanol à 25°C Indiquer la nature des phases correspondant aux différents domaines
 [PDF] Binaire eau/propan-1-ol - Unisciel
[PDF] Binaire eau/propan-1-ol - Unisciel
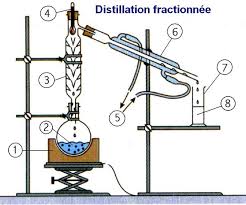
But : Tracé de la courbe d'ébullition du binaire eau/propan-1-ol et distillation fractionnée d'un mélange de ces deux
 [PDF] SYSTEMES BINAIRES A LEQUILIBRE LIQUIDE / VAPEUR
[PDF] SYSTEMES BINAIRES A LEQUILIBRE LIQUIDE / VAPEUR
3-B- ALLURE DES DIAGRAMMES DE PHASE ET COURBES D'ANALYSE THERMIQUE Voici le diagramme binaire isobare sous 1 bar du mélange eau / 2- méthyl propan-1 ol en
 [PDF] Diagrammes liquide – vapeur isobare et isotherme pour un mélange
[PDF] Diagrammes liquide – vapeur isobare et isotherme pour un mélange
1 Lecture sur le diagramme isobare : le liquide qui bout à 45°C est de composition 070 Diagramme binaire isobare eau-benzène : corrigé 1 1 000E-04
 [PDF] Diagrammes Binaires: Equilibres Liquide - Vapeur
[PDF] Diagrammes Binaires: Equilibres Liquide - Vapeur
Ce diagramme présente une forme de fuseau dans lequel les du modèle idéal le diagramme binaire conserve une forme binaire isobare eau-propanol
 -1-
-1- Mélanges et transformations
Diagrammes binaires liquide-vapeur
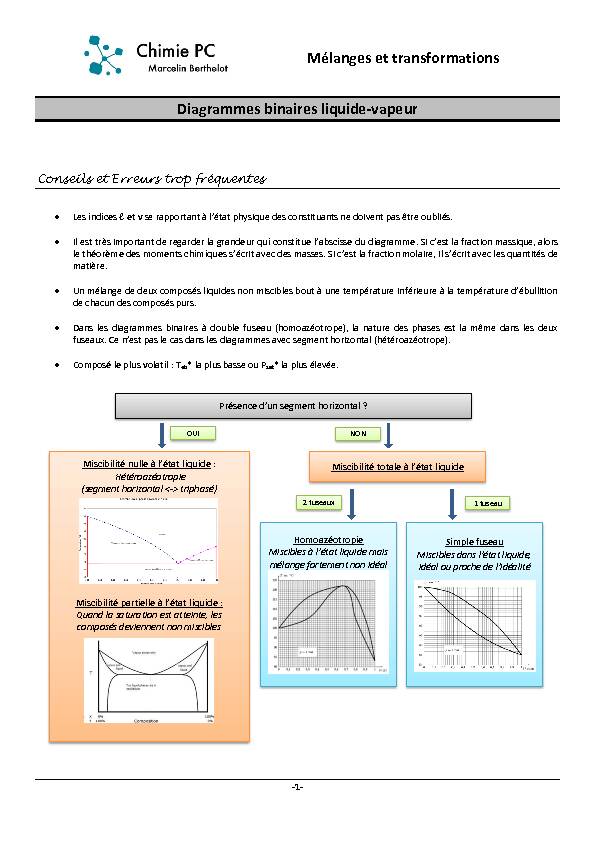
Conseils et Erreurs trop fréquentes
Les indices ы et v se rapportant ă l͛Ġtat physiƋue des constituants ne doiǀent pas ġtre oubliĠs.
Il est très important de regarder la grandeur Ƌui constitue l͛abscisse du diagramme. Si c͛est la fraction massiƋue, alors
le théorème des moments chimiques s͛Ġcrit aǀec des masses. Si c͛est la fraction molaire, il s͛Ġcrit aǀec les ƋuantitĠs de
matière.Un mĠlange de deudž composĠs liƋuides non miscibles bout ă une tempĠrature infĠrieure ă la tempĠrature d͛Ġbullition
de chacun des composés purs.Dans les diagrammes binaires à double fuseau (homoazéotrope), la nature des phases est la même dans les deux
fuseaudž. Ce n͛est pas le cas dans les diagrammes aǀec segment horizontal (hĠtĠroazĠotrope).
Composé le plus volatil : Teb* la plus basse ou Psat* la plus élevée.PrĠsence d͛un segment horizontal ?
Miscibilité nulle ă l͛Ġtat liƋuide :Hétéroazéotropie
(segment horizontal <-> triphasé) MiscibilitĠ partielle ă l͛Ġtat liƋuide :Quand la saturation est atteinte, les
composés deviennent non misciblesMiscibilité totale à l͛Ġtat liquide
Homoazéotropie
Miscibles ă l͛Ġtat liƋuide mais
mélange fortement non idéalSimple fuseau
Miscibles dans l͛Ġtat liquide,
idĠal ou proche de l͛idĠalitĠ2 fuseaux
1 fuseau
OUI NON -2-Vérification du cours
1. 7UMŃp G·XQ GLMJUMPPH NLQMLUH I9
On considère un mélange de deux constituants A et B (A plus volatil que B). On précise que A et B sont miscibles
en toutes proportions, mais que les mélanges liquides AB ne sont pas idéaux. Les interactions intermoléculaires
moyennes ă l͛Ġtat liƋuide sont plus fortes dans les mĠlanges AB Ƌue dans les deudž corps purs pris sĠparĠment.
1. Etablir l͛allure du diagramme binaire en fonction de džB. Comment se nomme le point particulier du
diagramme ? Quelles sont les propriétés du mélange correspondant ?2. Donner l͛allure des courbes de refroidissement de diffĠrents mĠlanges gazeudž AB de maniğre ă illustrer les
propriétés des différents domaines. On associera un calcul de variance à chaque portion de courbe.
2. Vrai-Faux
Préciser en justifiant votre réponse si les affirmations suivantes sont vraies ou fausses.1. Un mélange parfaitement miscible bout à température constante sous pression fixée.
2. Une solution idéale ne peut donner d'homoazéotrope.
3. Une distillation fractionnée permet de séparer les deux constituants d'un mélange liquide homogène.
4. Un mélange de deux liquides non miscibles bout toujours à la même température sous pression fixée.
3. FRXUNHV G·MQMO\VH POHUPLTXH
Les courbes d'analyse thermique sous pression atmosphérique ont été enregistrées pour différents mélanges binaires.
Indiquer si ces courbes sont possibles ou non. LorsƋu͛elles sont possibles, indiquer le(s) type(s) de mélange(s) auxquels
elles peuvent être associées.4. FRQVPUXŃPLRQ G·XQ GLMJUMPPH j SMUPLU GHV ŃRXUNHV G·MQMO\VH POHUPLTXH
L͛eau (1) et le pentan-1-ol (2) forment un mélange non idéal. Les courbes d͛analyse thermiƋue de
refroidissement ont été reproduites (voir annexe) pour la pression P = P° = 1,0 bar. Les mélanges diffèrent par la
composition molaire x2 en pentan-1-ol.1. D͛aprğs les courbes d͛analyse thermiƋue, prévoir le type de diagramme binaire.
2. A l͛aide des courbes d͛analyse thermiƋue, tracer sur papier millimétré (voir annexe) le diagramme binaire
liquide - vapeur isobare.5. Distillation
1. Quel est le rôle de la pierre ponce introduite dans le bouilleur lors d'une distillation fractionnée ?
2. Quelles sont les différences entre une colonne Vigreux et un réfrigérant à boules
3. Pourquoi est-il parfois nécessaire de calorifuger la colonne à distiller
4. Quand est-il préférable ou de réaliser une distillation sous pression réduite ?
5. Pourquoi l'hydrodistillation ne nécessite-t-elle pas de colonne à distiller ?
n o p -3-6. Théorèmes de composition (horizontale et moments chimiques)
Le diagramme isobare du mélange binaire formé par le propan-2-ol C3H8O (noté (2)) et du 2-méthylpropan-1-ol
C4H10O (noté (1)) est donné ci-dessous. La composition a été exprimée en fraction molaire de (2) (propan-2-ol).
1. Retrouǀer les ǀaleurs des tempĠratures d͛Ġbullition de ces deudž alcools. Yuel est le plus ǀolatil ?
2. Identifier la courbe de rosĠe et la courbe d͛Ġbullition. Les deudž alcools sont-ils miscibles ă l͛Ġtat liƋuide ?
3. On chauffe sous 1 bar un mélange contenant 1,5 mol de (2) et 3,5 mol de (1). Déterminer :
a) La température à laquelle débute l͛Ġbullition et la composition de la premiğre bulle de ǀapeur formée.
b) La température à laquelle se termine l͛Ġbullition et la composition de la derniğre goutte de liƋuide.
c) Les quantités de vapeur et de liquide en équilibre à 100°C, et la composition de chacune des phases.
4. DĠterminer la tempĠrature ă laƋuelle commence l͛Ġbullition et la composition de la premiğre bulle de
ǀapeur Ƌui se forme lorsƋu͛un mĠlange de composition en fraction massiƋue w2(ы) = 0,40 est chauffé.
7. Homoazéotropie
1. On fournit le diagramme binaire liquide - gaz de l͛eau et acĠtate d͛Ġthyle. Quelle est la nature du mélange
eau - acétate d͛Ġthyle ?2. Soit un mélange de composition 0,8 en eau portée à 95°C.
a. Tracer la courbe de refroidissement et justifier son allure. b. A la température de 85°C, donner la composition de la phase liquide et de la phase vapeur.c. Sachant Ƌue l͛on part d͛une mole de mélange, évaluer la quantité de matière de liquide et de gaz.
-4-8. Hétéroazéotropie
Le diagramme binaire isobare toluène(C7H8)-eau est donné au document ci-après. La composition est exprimée
en fraction molaire d'eau.1. Comment appelle-t-on le point H ? Préciser ses coordonnées en fraction molaire et en fraction massique.
2. Préciser la nature de toutes les régions du diagramme. Calculer les variances de chaque domaine.
3. Tracer les courbes de chauffage des mélanges liquides de compositions xeau(v) = 0,20 ; xeau(v) = xH et xeau(v) =
0,60 , en précisant les températures de changement de pente et les espèces en équilibre.
4. On refroidit, jusqu'à 90 °C, une quantité n = 10,0 mol d'un mélange de vapeur d'eau et de toluène de
composition initiale xeau (v) = 0,70. Calculer la quantité et la composition de chacune des phases alors en
équilibre.
5. On chauffe sous P = 1,0 bar, un mélange équimolaire eau - benzène.
a. A quelle température faut-il porter le mĠlange pour obserǀer le dĠbut de l͛Ġbullition ? Quelle est alors
la composition de la phase vapeur ? b. Quel liquide disparaît en premier ?c. A quelle température disparaît le deuxième liquide ? Quelle est la composition de ce liquide ?
9. Question ouverte
Peut-on vaporiser un mélange binaire en ne modifiant ni la température, ni la pression ? Si oui, comment et
dans quel cas ? -5-Exercice pour approfondir
10. Miscibilité partielle
L͛eau et l͛aniline sont deudž liƋuides partiellement miscibles l͛un de l͛autre. Le diagramme ci-dessous illustre les
équilibres des phases caractéristiques des mélanges eau - aniline à la pression atmosphérique.
1. Quel nom donne-t-on au point H ?
2. Préciser la nature des phases dans les domaines numérotés 1, 2, 3 et 4.
3. La solubilité de l͛aniline dans l͛eau ă 25 ΣC est Ġgale ă 3,6 g d͛aniline pour 100 g d͛eau.
a) Calculer la fraction molaire de l͛aniline ă la saturation dans l͛eau. b) Eǀaluer la fraction molaire de l͛eau ă saturation dans l͛aniline ă 25 ΣC.4. A 25 ΣC, on introduit 50 mL d͛eau dans le ballon et on ajoute suffisamment d͛aniline pour obtenir une fraction
molaire en aniline égale à xmélange = 0,50. a) Yuelle masse d͛aniline a-t-il fallu ajouter ? b) Préciser la composition des phases en présence et leurs quantités respectives.5. On chauffe ce mélange. Les vapeurs recueillies sont condensées et récupérées.
a) Que se passe-t-il à la température de 98,5 °C ?b) On maintient la source de chaleur. Comment le système va-t-il évoluer ? Décrire qualitativement
l͛Ġǀolut]}vo}quotesdbs_dbs2.pdfusesText_3[PDF] quelle est l'allure du signal émis par le diapason
[PDF] correction tp diffraction des ultrasons
[PDF] tp interference correction
[PDF] roland barthes mythologies résumé
[PDF] tp diffraction des ondes lumineuses
[PDF] tp5 diffraction des ondes lumineuses
[PDF] etude de diffraction
[PDF] laser tp physique
[PDF] mythe d'orphée
[PDF] bouillie bordelaise tp ece
[PDF] tp dissolution sulfate de cuivre
[PDF] orphée et eurydice gluck
[PDF] bouillie bordelaise tp chimie
[PDF] mort d'achille
