 LES ELEMENTS DU GROUPE 1 - LES METAUX ALCALINS -
LES ELEMENTS DU GROUPE 1 - LES METAUX ALCALINS -
1.87. 260. 170. 28.4. Bleu. B. Densité : les métaux alcalins ont des densités faibles : Li Na et K flottent sur l'eau. C. Rayon atomique et rayon ionique
 TP COURS de chimie n° 4 Etude des propriétés de leau et des
TP COURS de chimie n° 4 Etude des propriétés de leau et des
Présenter les propriétés de l'eau en tant que solvant. - Etudier les caractéristiques des métaux alcalins et alcalino-terreux.
 La classification périodique : alcalins et alcalinoterreux MT 22421
La classification périodique : alcalins et alcalinoterreux MT 22421
Les métaux alcalins sont peu denses. Durée : 52 sec. Séquence 3 : réaction avec l'eau. On place un petit morceau de lithium Li puis de sodium
 alcalins.pdf
alcalins.pdf
Nom : métaux alcalins (alcalin : de l'arabe al-qaly la soude). Réagit avec les oxydes acides pour donner des sels de sodium et de l'eau :.
 LES ELEMENTS DU GROUPE 2 - LES METAUX ALCALINO
LES ELEMENTS DU GROUPE 2 - LES METAUX ALCALINO
Comparable à celle des métaux alcalins leur réactivité ne permet pas Avec H2O : la réaction avec l'eau produit un hydroxyde et libère de l'hydrogène.
 ? ? ? ? ? ? ? ? ?
? ? ? ? ? ? ? ? ?
a) Réactivité des métaux alcalins avec l'eau. Dans le tableau périodique sélectionner un métal alcalin
 I. Les éléments du groupe IA
I. Les éléments du groupe IA
(9) Les valeurs de densité augmentent de haut en bas. (10) En réagissant avec le dioxygène les métaux alcalins forment un oxyde
 1-DECHETS CHIMIQUES GENERES PAR LES LABORATOIRES ET
1-DECHETS CHIMIQUES GENERES PAR LES LABORATOIRES ET
Produits susceptibles de réagir violemment au contact de l'eau en dégageant du dihydrogène qui peut s'enflammer (la réactivité des métaux alcalins avec l'eau
 T3 sept. 2014
T3 sept. 2014
3 sept. 2014 Les métaux alcalins et l'eau (déplacement simple). Les alcalins réagissent avec l'eau de façon exothermique pour.
 Untitled
Untitled
Les métaux alcalins peuvent-ils réagir sur l'eau ? IO. Quel caractère portent les oxydes et les hydroxydes des métaux alcalins ?
 [PDF] LES ELEMENTS DU GROUPE 1 - LES METAUX ALCALINS -
[PDF] LES ELEMENTS DU GROUPE 1 - LES METAUX ALCALINS -
Les métaux alcalins sont les éléments du 1er groupe du tableau périodique Ils forment un ensemble dont les propriétés sont particulièrement homogènes En
 [PDF] LES METAUX ALCALINO-TERREUX
[PDF] LES METAUX ALCALINO-TERREUX
Avec un potentiel d'ionisation plus élevée que ceux des métaux alcalins les métaux alcalino- terreux présentent une plus grande aptitude à s'hydrater et par
 [PDF] Les métaux
[PDF] Les métaux
On trouve les métaux alcalins et alcalino-terreux dans les minéraux et les eaux naturelles exemples : Métal Source naturelle Sodium sel de gemme NaCl eau
 [PDF] Alcalins et alcalino-terreux - F2School
[PDF] Alcalins et alcalino-terreux - F2School
Par électrolyse des hydroxydes alcalins ou des hydroxydes alcalino-terreux fondus on obtient les métaux et par électrolyse de la solution aqueuse c'est l'eau
 [PDF] TP COURS de chimie n° 4 Etude des propriétés de leau et des
[PDF] TP COURS de chimie n° 4 Etude des propriétés de leau et des
- Présenter les propriétés de l'eau en tant que solvant - Etudier les caractéristiques des métaux alcalins et alcalino-terreux - Etudier quelques équilibres
 [PDF] Section C CHIMIE; MÉTALLURGIE - WIPO
[PDF] Section C CHIMIE; MÉTALLURGIE - WIPO
Composés des métaux alcalins c à d du lithium du sodium du potassium du rubidium (production de gaz à l'eau ou de gaz de synthèse à partir
 Métal alcalin - Wikipédia
Métal alcalin - Wikipédia
Un métal alcalin est un élément chimique de la première colonne ( 1 groupe) du tableau Les métaux alcalins réagissent également avec l'eau pour former des
 [PDF] Chimie minérale systématique II Métaux et semi-métaux - UniNE
[PDF] Chimie minérale systématique II Métaux et semi-métaux - UniNE
Les métaux alcalins élémentaires réagissent directement avec de l'eau pour don- ner les hydroxydes et avec l'oxygène pour donner les composés oxygénés
 [PDF] La classification périodique : alcalins et alcalinoterreux MT 22421
[PDF] La classification périodique : alcalins et alcalinoterreux MT 22421
Les métaux alcalins sont peu denses Durée : 52 sec Séquence 3 : réaction avec l'eau On place un petit morceau de lithium Li puis de sodium
Quels sont les métaux alcalins ?
Les métaux alcalins – lithium, sodium, potassium, rubidium, césium et francium – constituent les éléments de la première colonne du tableau de classification périodique. Ils doivent leur nom à la propriété qu'ils ont de donner avec l'eau des bases fortes, ou « alcalis ».Quel est le rôle des métaux alcalins ?
Les métaux alcalins réagissent non seulement avec l'eau mais également avec les donneurs de protons comme les alcools et les phénols, l'ammoniac gazeux et les alcynes, ces derniers donnant lieu aux réactions les plus violentes.Quelles sont les propriétés des alcalins ?
Propriétés des alcalins
Ce sont des métaux. Ce sont des solides mous; ils peuvent se couper au couteau. Ils sont extrêmement réactifs. Pour cette raison, à l'état pur, on doit les conserver dans l'huile puisqu'ils réagissent fortement au contact de l'eau.- Si la plupart des métaux que nous connaissons dans la vie quotidienne ne réagissent pas ou peu avec l'eau, certains, tels que le lithium, le sodium, le potassium ou le calcium, réagissent violemment au contact de l'eau.
I. Tableau périodique des éléments
12I. Les éléments du groupe IA
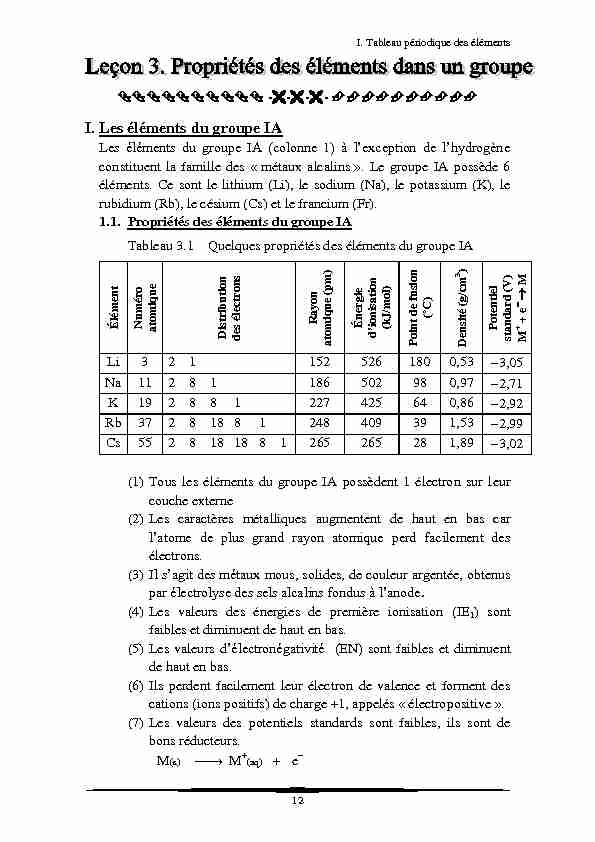
constituent la famille des " métaux alcalins ». Le groupe IA possède 6 éléments. Ce sont le lithium (Li), le sodium (Na), le potassium (K), le rubidium (Rb), le césium (Cs) et le francium (Fr).1.1. Propriétés des éléments du groupe IA
Tableau 3.1 Quelques propriétés des éléments du groupe IAÉlément
Numéro atomique
Distribution des électrons
Rayon atomique (pm)Énergie
(kJ/mol)Point de fusion
(°C)Densité (g/cm
3)Potentiel standard (V)
M + + e MLi 3 2 1 152 526 180 0,53 3,05
Na 11 2 8 1 186 502 98 0,97 2,71
K 19 2 8 8 1 227 425 64 0,86 2,92
Rb 37 2 8 18 8 1 248 409 39 1,53 2,99
Cs 55 2 8 18 18 8 1 265 265 28 1,89 3,02
(1) Tous les éléments du groupe IA possèdent 1 électron sur leur couche externe (2) Les caractères métalliques augmentent de haut en bas carélectrons.
(3) mous, solides, de couleur argentée, obtenus par (4) Les valeurs des énergies de première ionisation (IE1) sont faibles et diminuent de haut en bas. (5) Les valeurs dsont faibles et diminuent de haut en bas. (6) Ils perdent facilement leur électron de valence et forment des cations (ions positifs) de charge +1, appelés " électropositive ». (7) Les valeurs des potentiels standards sont faibles, ils sont de bons réducteurs. M(s) oM+(aq) + e
I. Tableau périodique des éléments
13 (8) Ils ont de hauts et tendent à diminuer de haut en bas. (9) Les valeurs de densité augmentent de haut en bas. (10) En réagissant avec le dioxygène, les métaux alcalins forment un oxy :4 Na + O2
o2 Na2O
oOH224 NaOH
4 K + O2
o 2 K2O oOH22 4 KOH (11) Les métaux alcalins réagissent violemment av donner des hydroxydes qui sont des bases et du dihydrogène.2 Na + 2 H2O
o2 NaOH + H2
2 K + 2 H2O
o2 KOH + H2
(12) Les composés des éléments du groupe IA sont tous solubles dan (13) Les composés des éléments du groupe IA ont des flammes de couleur différente après brûlage tels que : Li de couleur rouge, Na jaune, K violet1.2. Les avantages des éléments du groupe IA
(1) Entrant dans la composition des minéraux dont le corps a besoin. (2) Bon conducteur de chaleur et d'électricité ce qu'on applique à utiliser dans le réacteur nucléaire. (3) Utiliser comme réducteur pour préparer des éléments. (4) Utiliser dans la préparation du tétraéthyl-plomb qui est un composé organométallique de formule Pb(C2H5)4 liquide huileux qui a été très utilisé comme additif antidétonant dans les essences. Le tétraéthyl-plomb est obtenu par la réaction m. oII. Les éléments du groupe IIA
Les éléments du groupe IIA (colonne 2) constituent la famille des " métaux alcalino-terreux ». Le groupe IIA possède 6 éléments. Ces éléments sont le béryllium (Be), le magnésium (Mg), le calcium (Ca), le strontium (Sr), le baryum (Ba) et le radium (Ra).2.1. Propriétés des éléments du groupe IIA
Tableau 3.2 Quelques propriétés des éléments du groupe IIAI. Tableau périodique des éléments
14Élément
Numéro atomique
Distribution des
électrons
Rayon a
tomique (pm)Énergie
(kJ/mol)Point de fusion
(°C)Densité (g/cm
3)Potentiel standard
(V) M + + e M I IIBe 4 2 2 112 900 1760 1280 1,85 1,85
Mg 12 2 8 2 160 738 1450 649 1,74 2,36
Ca 20 2 8 8 2 197 590 1146 839 1,55 2,87
Sr 38 2 8 18 8 2 215 549 1064 770 2,60 2,89
Ba 56 2 8 18 18 8 2 222 503 965 714 3,50 2,90
Ra 88 2 8 18 32 18 8 2 - 509 979 700 5,00 2,92
(1) Tous les éléments du groupe IIA possèdent 2 électrons sur leur couche externe, les caractères métalliques augmentent de haut en bas. (2) électricité. (3) Préparation par électrolyse des composés des alcalino-terreux fondus. (4) Le rayon atomique augmente de haut en bas du groupe. (5) Les valeurs des énergies de première ionisation (IE1) diminuent de haut en bas. (6) Ils perdent facilement leurs deux électrons de valence et forment des cations (ions positifs) de charge +2. (7) bas. (8) Les valeurs des potentiels standards sont faibles comme les éléments du groupe IA, ils sont donc de bons réducteurs. M(s) oM2+(aq) + 2e
(9) Les points de fusion diminuent par numéro atomique croissant en descendant le long du groupe. (10) La densité augmente par numéro atomique croissant en descendant le long du groupe. (11) En réagissant avec le dioxygène, les métaux alcalino-terreux2 Mg + O2
o 2 MgO oOH222 Mg(OH)2
2 Ca + O2
o 2 CaO oOH222 Ca(OH)2
I. Tableau périodique des éléments
15 (12) Les métaux alcalino- donner des hydroxydes qui sont des bases et du dihydrogène (quoique celle-ci soit moin alcalins).Mg + 2 H2O
oMg(OH)2 + H2 au)
Ca + 2 H2O
oCa(OH)2 + H2 (avec lau chaude)
(13) La plupart des composés du groupe IIA sont solubles dans (14) Les composés des éléments du groupe IIA ont des flammes de couleur différente après brûlage tels que : Ca de couleur rouge-2.2. Les avantages des éléments du groupe IIA
(1) Utiliser comme réducteur dans certaines réactions. (2) terrestre. (3) La dolomite est une espèce minérale formée de carbonate de calcium et de magnésium de formule CaCO3.MgCO3. On la retrouve beaucoup dans les roches calcaires. (4) 2+ contrôle le pH de la terre, par conséquence de (5) Le calcium et le magnésium sont très largement présents dans tous organismes vivants connus, et y jouent un rôle vital. (6) 2] est employé en médecine dans certains dentifrices et pour traiter les aigreurs (7) Utiliser le mélange de Ba et Cu pour des composants du navire marine (8) Le magnésium est le composant dans certaines chlorophylles des plantes.III. Les éléments du groupe VIA
Les éléments du groupe VIA (colonne 16) constituent la famille des " chalcogènes ». Le groupe VIA possède 5 éléments. Ce sont polonium (Po) qui est une substance radioactive. Certains éléments de ce groupe se trouvent sous forme de corps simples tels que le dioxygène (O2) et le soufre (S8). On les trouveI. Tableau périodique des éléments
163.1. Propriétés des éléments du groupe VIA
Tableau 3.3 Quelques propriétés des éléments du groupe VIAÉlément
Numéro atomique
Distribution des électrons
Rayon atomique (pm)Énergie
(IE1) (kJ/mol)
EN (kJ/mol)Densité (g/cm
3)Point de fusion
(°C)Potentiel standard
: E 0 (V) M + + e MO 8 2 6 66 1320 3,44 1,15 219 +1,23
S 16 2 8 6 104 1006 2,58 2,07 113 0,48
Se 34 2 8 18 6 117 947 2,55 4,80 217 0,92
Te 52 2 8 18 18 6 137 876 2,10 6,24 450 0,95
Po 84 2 8 18 32 18 6 140 818 2,00 9,4 254
(1) La plupart des éléments du groupe VIA sont des non-métaux, ils possèdent 6 électrons sur leur couche externe. (2) Le rayon atomique augmente de haut en bas. (3) Les caractères métalliques augmentent ou les caractères non- métalliques diminuent de haut en bas. (4) Les valeurs des énergies de première ionisation (IE1) diminuent au fur et à mesure que le numéro atomique augmente (5) au fur et à mesure que le numéro atomique augmente en descendant le (6) Ils possèdent de plus grandes valeurs potentiels standards et diminuent de haut en bas, ils tendent à être des oxydants. (7) O2 ; Se et Te sont des (8) Les points de fusion augmentent au fur et à mesure que le groupe. (9) La densité augmente au fur et à mesure que le numéro (10) qui sont entre 2 et +6, par exemple soufre (S) dans H2S, S8, H2SO3, H2SO4 sont respectivement de 2, 0, +4 et +6.I. Tableau périodique des éléments
173.2. Les avantages des éléments du groupe VIA
(1) Pour les êtres vivants : ils sont des composants dans les lipides et les sucres. (2) Le dioxygène liquide est utilisé comme oxydant dans lesquotesdbs_dbs33.pdfusesText_39[PDF] famille d'objet definition
[PDF] milieu familial et reussite scolaire pdf
[PDF] influence des parents sur le parcours scolaire
[PDF] milieu familial et réussite scolaire
[PDF] les effets de l'éducation familiale sur la réussite scolaire
[PDF] montrer qu'une famille est génératrice
[PDF] texte d amour famille recomposée
[PDF] que signifie le cid
[PDF] texte mariage famille recomposee
[PDF] definition du mot cid
[PDF] étymologie du mot cid
[PDF] le cid signification du titre
[PDF] qui est le cid figaro
[PDF] origine du mot cid
