 Exercices de nomenclature organique Corrigés
Exercices de nomenclature organique Corrigés
5 substituants : 4 méthyle et 1 éthyle. Page 4. OS Chimie. Corrigé des exercices. - 4 -.
 NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
NOMENCLATURE EN CHIMIE ORGANIQUE. La nomenclature permet de : a) Trouver le nom d'une molécule connaissant la structure. b) Trouver la structure d'une
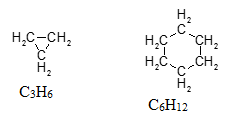 COURS ET EXERCICES DE CHIMIE ORGANIQUE 1
COURS ET EXERCICES DE CHIMIE ORGANIQUE 1
Le tableau ci- dessous nous montre la nomenclature des hydrocarbures saturés (alcanes) et celle des groupes alkyles dérivés. CHO. CO. COH. N. OR. C. C.
 Exercices Complémentaires
Exercices Complémentaires
Correction des exercices complémentaires. Chapitre 2: Nomenclature des composés organiques. 2.1 Exercice 2.1. CH. CH2. HO. CH2 OH. HC. CH. Cl. CH2. H3C. O CH3.
 Nomenclature organique: Exercices
Nomenclature organique: Exercices
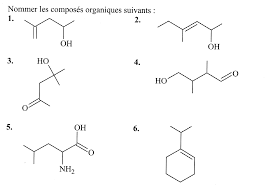
Page 1. Exercices 1ère. AdM. 1. Nomenclature organique: Exercices. 1 Ecrire les noms scientifiques : (1)
 Terminale générale - Structure en chimie organique - Exercices
Terminale générale - Structure en chimie organique - Exercices
Exercice 11 corrigé disponible. Indiquer en nomenclature chimique le nom des composés organiques suivants : 1. Acide tartrique. 2. Acide lactique. 3. Glycérol
 chimie organique
chimie organique
C'est pour- quoi cet ouvrage propose un cours concis mais complet des exercices et des QCM Nomenclature systématique. ❚ 1.1. Intérêt d'une nomenclature ...
 Exercices résolus - de chimie organique - Les cours de Paul Arnaud
Exercices résolus - de chimie organique - Les cours de Paul Arnaud
Ce chapitre couvre le chapitre 1 de la 19ème édition du cours de Chimie Organique de Exercice 1.1 Détermination de la formule brute d'un composé organique. L ...
 Chimie Générale Avancée II: Partie Organique Exercices - Séance n
Chimie Générale Avancée II: Partie Organique Exercices - Séance n
22 févr. 2019 Donner la nomenclature systématique des composés suivants. Exercice 2. Expliquer les faits suivants en vous aidant de diagramme d'orbitales pour ...
 Atomistique et Chimie Organique Cours et Exercices Corrigés
Atomistique et Chimie Organique Cours et Exercices Corrigés
chimie organique. Page 47. 4. Exercices et Corrections. 4.1. Exercice 01. On ... chimie organique. Page 53. 2.2. Nomenclature IUPAC (nomenclature systématique).
 Exercices de nomenclature organique Corrigés
Exercices de nomenclature organique Corrigés
OS Chimie. Corrigé des exercices. - 1 -. Exercices de nomenclature organique. Corrigés. 1. Dessinez la formule développée des molécules suivantes :.
 Exercices Complémentaires
Exercices Complémentaires
Exercices Complémentaires. Chapitre 2 : Nomenclature des composés organiques. 2.1 Exercice 2.1. Donner la formule développée des composés suivants :.
 Exercices de la nomenclature en chimie organique
Exercices de la nomenclature en chimie organique
Université frères Mentouri Constantine 1. TC SNV 1ére Année
 Terminale générale - Structure en chimie organique - Exercices
Terminale générale - Structure en chimie organique - Exercices
Indiquer le nom en nomenclature officielle de cette molécule. Exercice 3 – Polynésie Juin 2018. 4/5. Structure en chimie organique – Exercices. Physique
 chimie organique
chimie organique
chimie organique. UE1. Élise Marche. ParcourS. SanTÉ. & L.aS Nomenclature des autres molécules ... QCM et exercices.
 Chimie organique : Exercices – corrections
Chimie organique : Exercices – corrections
Chimie organique : Exercices – corrections. Exercice 1 Nommez les molécules ci-dessous. a) butane b) éthane c) propane d) heptane. Exercice 2 Nommez les
 Exercices résolus - de chimie organique - Les cours de Paul Arnaud
Exercices résolus - de chimie organique - Les cours de Paul Arnaud
Le but de la Chimie organique comme de la Chimie en général
 EXERCICES
EXERCICES
1e Spécialité Physique Chimie. CHAPITRE 6 1 Nomenclature groupes fonctionnels. Exercice 1. Exercice 2 ... Pour les quatre molécules organiques sui-.
 COURS ET EXERCICES DE CHIMIE ORGANIQUE 1
COURS ET EXERCICES DE CHIMIE ORGANIQUE 1
-La nomenclature des composés cycliques est toujours désignée par le nom de l'hydrocarbure suivi du suffixe carbaldéhyde (le –CHO est lié à un atome de carbone
 TD CH13 Les différentes familles de molécules organiques.
TD CH13 Les différentes familles de molécules organiques.
Première S CH13 Nomenclature des molécules organiques page 201. 9. Exercices chimie organique. Feuille. Première S. Alcanes alcènes
Fonction
organique Formule générale TerminaisonRègle de nomenclature Exemples
Alcool
olOn remplace le e final de l"alcane correspondant par ol précédé du numéro de position du groupe hydroxyde OH. OH a priorité pour la numérotation de chaîne.
Aldéhyde
R-CHO ...alOn remplace le e final de l"alcane
correspondant par al précédé .Ce groupement se trouve toujours
en bout de chaîne : pas de position à préciserCétone
...one On remplace le e final de l"alcane correspondant par one précédé du numéro de position du groupe carboxyle CO.CO a priorité pour la
numérotation de chaîne. Acide carboxyliq ue RCOOH ou RCO 2HAcide ... oïque
On remplace le e final de l"alcane
correspondant par oïque, le nom est précédé du mot acide.Ce groupement se trouve toujours
en bout de chaîne : pas de position à préciser.RCOOH a priorité pour la numérotation. EsterR1 - COO-R2
oate.. yle Partie1: R1-C On remplace le e final de l"alcane correspondant par oatePartie2 :
R2 On remplace le e
final de l"alcane correspondant par oyle.Associer les deux noms.
Amine R-NH2 ...
amine On ajoute au nom de l"alcane correspondant le motamine. Première S CH13 Nomenclature des molécules organiques page 201 2 Première S CH13 Nomenclature des molécules organiques page 201 3 Première S CH13 Nomenclature des molécules organiques page 201 4 Première S CH13 Nomenclature des molécules organiques page 201 5EXERCICES LES HYDROCARBURES
Exercice n° 1 :
Donner le nom des hydrocarbures suivants, indiquer pour chacun d"eux la famille d"hydrocarbure à laquelle il
appartient et vérifier si la formule brute du composé correspond bien à la formule générale de la famille.
C 2H5 a) CH3-CH2-CH3 b) CH3-CH-CH=CH2 c) CH3-CH=CH-C-CH2-CH3
CH3 CH3
C2H5 C2H5
d) CH3-CH-CH-CH2-CH3 e) CH3-CºC-CH-CH3 f) CH3-CH2-CH-CH-C-CH2-CH3
C2H5 CH3 CH3CH3CH3
Exercice n° 2 :
Donner la formule semi-développée des hydrocarbures dont les noms suivent : a) 2-méthylhex-3-ène b) 2,4-diméthylpentane c) 4,5-diéthyl-3-méthyloctane d) heptane e) 2-méthylpent-2-ène f) 2,2-diméthylbutane g) propène h) diméthylpropaneExercice n° 3 :
Donner la formule semi-développée des hydrocarbures dont les noms suivent : a) 3-méthylbut-1-yne b) 3-éthyl-2-méthylhex-3-ène c) 4-éthylhept-1-yned) 3-éthyl-2-méthylpentane e) 4,5-diméthylhex-2-yne f) 2-éthyl-3,4-diméthylpent-2-ène
Exercice n° 4 :
Donner le nom des hydrocarbures suivants :
CH3 C2H5 CH3 -CH2-CH2 C2H5
a) CH3-C=CH2-CH-CH3 b) CH3-CºC-CH- CH-CH3 c) CH3 -CH-CH -C-CH2-CH3
CH3 CH3 CH3 CH3
Exercice n° 5 :
Certains composés d"usage courant sont des hydrocarbures :1) L"acétylène est un gaz utilisé dans les chalumeaux oxyacétylènique qui comportent une bouteille d"acétylène
et une bouteille de dioxygène sous pression. a) Chercher l"autre nom et la formule de l"acétylène b) La flamme du chalumeau est bleue, écrire l"équation-bilan de la combustion correspondante.c) Quelle masse d"eau sera dégagée par la combustion de 0,5 L d"acétylène si on considère que sous pression
une mole d"acétylène occupe un volume de 10 L?2) Les liquides correcteurs portent la mention : sans trichloroéthane, contient du méthylcyclohexane
Donner la formule semi-developpée de ces molécules.3) Le gaz de ville contient du méthane. Lorsqu"il alimente une gazinière, un des deux feux qui n"a pas été nettoyé
depuis longtemps produit une flamme jaune alors que l"autre produit une flamme bleue. a) Expliquer la cause de la couleur jaune de la flamme pour le premier feu .b) Ecrire l"équation-bilan des deux combustions et calculer dans chaque cas le volume de dioxygène nécessaire
pour brûler 200 g de méthane. c) Première S CH13 Nomenclature des molécules organiques page 201 6Exercice n° 6 :
On réalise la combustion du butane en présence de dioxygène.1) Comment peut-on identifier visuellement le type de combustion ?
2) La combustion réalisée est une combustion complète.
a) Donner l"équation-bilan de cette réaction. b) Calculer la masse molaire du butane. c) Quelle est la masse d"eau obtenue à partir de 20 grammes de butane ? d) Quel volume de dioxygène est nécessaire à la combustion de 500 mL de butane ?Exercice n° 7 :Nommer un alcane
2. Nommer un alcène
CH3-CH2-CH2-CH3
CH3-CH-CH3
CH3CH3-CH2-CH-CH2-CH3
CH3CH3-CH-CH-CH2-CH2-CH3
CH3 C2H5
CH3-CH-CH2-CH-CH2-
CH 3 CH3 CH 3-C- CH 3 CH3 CH3-CH2-C---CH-CH2-CH2-CH3
CH3 C2H5
CH2=CH-CH2-CH3
CH2=C-CH3
CH3CH3-CH=CH-
CH3CH2=CH-CH2-CH2-CH3 CH2=CH-CH-CH3
CH3CH2=C-CH2-CH3
CH3CH3-CH=CH-CH2-CH3 CH3-C=CH-CH3
CH 3 Première S CH13 Nomenclature des molécules organiques page 201 73. Nommer un alcyne
4. Divers.
Exercice n° 8
1) Dans les molécules suivantes indiquer le nombre d"atomes de carbone tétravalents, tétragonaux, trigonaux,
digonaux. a) CH3-CH2-CH3 b) CH2=CH-CH3 c) CH3-C-CH2-CH3
d) CH3-CH-CH3 e) CH3-CH-C ºCH
2) Nommer les molécules a, b, d et e.
3) Déterminer leurs masses molaires moléculaires.
Exercice n°9 :
1) Ecrire la formule semi-développée des composés suivants :
a) heptane b) 2-méthylpent-2-ène c) 4-éthylhept-1-yne d) 2,2-diméthylbutane e) 3-éthyl-2-méthylpentane f) propène g) 4,5-diméthylhex-2-yne h) 3-éthyl-2-méthylhex-3-ène2) Indiquer leurs formules brutes et vérifier qu"elles correspondent à la formule générale du cours.
3) Représenter les molécules avec la convention de Cram.
OCH3 CH3
HCºC-CH2-CH3 CH3-CºC-CH3 HCºC-CH2-CH2-CH3HCºC-CH-CH3
CH3CH3-CºC-CH2-CH3
CH3 C2H5
CH3-CH2-CH--C-CH2-
CH 3CH3 CH3
CH2-CH=CH-C-CH2-CH3
CH3 CH3
CH2-CH2-CH2-C-CH=CH2
C2H5 CH3
CH3 CH3
CH2-CH2-CH2-C-CºCH
CH3CH3 CH3
CH2-CºC-C-CH2-CH3
C2H5 CH3
Première S CH13 Nomenclature des molécules organiques page 201 8Exercice n°10 :
1) Nommer les composés suivants :
a) CH3-C-CH3 b) CH3-CH2-CH=CH3 c) CH3-CH-CºCH2
2) Ecrire l"équation-bilan équilibrée de la réaction de combustion complète de chaque composé.
3) Calculer le volume de dioxygène produit par la combustion complète de 100 g de chaque composé.
4) Calculer la masse puis le volume d"eau ainsi produit.
5) Pour chaque molécule, rechercher la formule semi-développée d"un isomère et le nommer.
Exercice n°11 :
La combustion complète de 3,6g d"alcane produit 5,4g d"eau.1) Déterminer la formule brute et la masse molaire de cet alcane.
2) Donner les noms et les formules semi-développées des isomères de cet alcane.
DONNEES :
Volume molaire des gaz V
m=22,4L.mol-1Masse volumique de l"eau
r = 1000 g.L-1 CH3 CH3 C2H5 Première S CH13 Nomenclature des molécules organiques page 201 9 Exercices chimie organique Feuille Première SAlcanes, alcènes, alcynes
Exercice 1 Le craquage
Par craquage du cyclooctane C8H16, on obtient uniquement un composé non cyclique de formule C4H8.1. Ecrire l"équation chimique du craquage réalisé.
2. Donner tous les isomères de constitution du produit de craquage.
3. Parmi ces isomères, quels sont ceux qui présentent une isomérie Z/E ? Les dessiner en faisant apparaître
cette isomérie.Exercice 2 Test à l"eau de brome
Afin de déterminer la formule brute d"un alcène X, on mesure la quantité de dibrome consommée par réaction
d"addition. On observe que 2,1 g d"alcène décolorent complètement une solution contenant 8,0 g de dibrome.
1. Donner la formule générale d"un alcène.
2. Ecrire l"équation associée à la réaction d"addition.
3. La transformation a lieu dans des proportions stoechiométriques. En déduire la quantité de matière
d"alcène introduit, puis sa masse molaire.4. Donner la formule brute de X.
Données : M(Br
2)= 160.0 g.mol-1; M(C) = 12.0 g.mol-1; M(H)= 1.0 g.mol-1.
Exercice 3 Solvants chlorés
Le tableau ci dessous rassemble des données concernant quelques solvants chlorés.Solvant Formule
Température d"ébullition sous 1 bar
(°C) Production européenne en 1991 (t)Chlorométhane CH3Cl - 24 220 000
dichlorométhane CH2Cl2 40,1 234 000 trichlorométhane CHCl3 61 220 000 tétrachlorométhane CCl4 76 250 0001,1,2-trichloroéthylène Cl2C=CHCl 86,7 125 000
1,1,2,2-
tétrachloroéthylène Cl2C=CCl2 121,2 210 000
1,1,1-trichloroéthane H3C - CCl3 73,8 1980
Première S CH13 Nomenclature des molécules organiques page 201 101. Donner l"état physique des solvants du tableau à 25°C et sous 1 bar.
2. Le 1,1,2,2-tétrachloroéthylène peu être fabriqué par craquage d"un mélange de 1,1,2,2-tétrachloroéthane
Cl2HC - CHCl2 et de 1,1,1,2,2-pentachloroéthane Cl3C - CHCl2. Compléter les équations suivantes :
Cl2HC - CHCl2 --> Cl2C = CCl2 ......
Cl3C - CHCl2 --> Cl2C = CCl2 .......
3. Le chlorométhane CH
3Cl gazeux est synthétisé à 150 °C par action du chlorure d"hydrogène gazeux sur le
méthanol CH3OH gazeux, en présence d"alumine, qui sert de catalyseur. L"excès de chlorure d"hydrogène
est éliminé par passage dans une solution aqueuse d"hydroxyde de sodium. Le chlorométhane est ensuite
séché avec de l"acide sulfurique H2SO4, puis comprimé et liquéfié.
- Ecrire l"équation chimique de la transformation du méthanol en chlorométhane.- Par quel type de réaction de chlorure d"hydrogène en excès est-il éliminé ? Ecrire l"équation chimique de
cette transformation.- Calculer la quantité de matière de méthanol nécessaire à la production européenne de chlorométhane.
- Calculer en m3, le volume occupé par le chlorométhane formé s"il est stocké à 25°C, sous 1 bar.
Données : M (CH
3OH) = 32,0 g.mol-1.M (CH3Cl) = 50,5 g.mol-1.Volume molaire à 25°C sous 1 bar : Vm = 24,0
L.mol -1.Exercice 4
1. A partir de la formule brute C3H6O, combien peut-on construire de molécules ? On utilisera les règles de
l"octet et du duet pour déterminer les formules semi développées.2. Donner la géométrie autour de chaque atome de carbone.
Première S
Exercices chimie organique Feuille Première SCorrection exercice 1
C8H16 --> 2 C4H8. CH2=CH-CH
(CH3)2C=CH2 ; 2-méthylpropèneCorrection exercice 2
C nH2n. CnH2n + Br2 --> CnH2nBrQté matière Br2 : 8/ 160 = 0,05 mol donc 0,05 mol alcène de masse molaire 12 n + 2n = 14 n
Qté de matière (mol) = masse (g) / masse molaire (g/mol)0,05 = 2,1 / (14n) soit n = 3 C3H
Correction exercice 3
Gaz pour le chlorométhane ; liquide pour les autres à 25 °C sous 1 bar.Cl2HC - CHCl2 --> Cl2C = CCl2 + H2.
CH3OH + HCl --> CH3Cl + H2O
220 000 t = 2,2 1011 grammes
2,2 1011 / 35,5+12+3) = 4,36 109 mol
(12+4+16)* 4,36 109 =1,39 1011 g = 139 000 t volume chlorométhane (L) = Qté matière (mol) fois volume molaire (L/mol)4,36 109 *24 = 1,05 1011 L = 1,05 108 m
Correction exercice 4
CH3-CH2-CHO propanal ( aldehyde)
CH2=CH-CH2OH ; CHOH=CH
d"autres molécules :carbone tétragonal ( lié à 4 groupes d"atomes) :le carbone est au centre d"un tétraèdre et les quatre liaisons sont
dirigées vers les sommets du tétraèdrecarbone trigonal ( lié à 3 groupes d"atomes) : structure triangle plan ( angles proches de 120°)
Première S CH13 Nomenclature des molécules organiques page 201 Exercices chimie organique Feuille Première S CH2-CH3 but-1-ène ; CH3CH=CH-CH3 deux isomères Z et E du butBr2 ( dibromoalcane)
donc 0,05 mol alcène de masse molaire 12 n + 2n = 14 n Qté de matière (mol) = masse (g) / masse molaire (g/mol)H6 soit CH3-CH=CH2.(propène).
Gaz pour le chlorométhane ; liquide pour les autres à 25 °C sous 1 bar.Cl3C - CHCl2 --> Cl2C = CCl2+ HCl
Réaction acide base H3O+ + HO- --> 2H
n(mol) = m(g) / M (g/mol) m(méthanol)= M* n139 000 t.
volume chlorométhane (L) = Qté matière (mol) fois volume molaire (L/mol) m3.CH3-CO-CH3 acétone ou propanone ( cétone)
CHOH=CH-CH3 ( instable) ; CH2=C(OH)-CH3 (instable)carbone tétragonal ( lié à 4 groupes d"atomes) :le carbone est au centre d"un tétraèdre et les quatre liaisons sont
rbone trigonal ( lié à 3 groupes d"atomes) : structure triangle plan ( angles proches de 120°)
CH13 Nomenclature des molécules organiques page 201 11 Exercices chimie organique Feuille Première S deux isomères Z et E du but-2-ène donc 0,05 mol alcène de masse molaire 12 n + 2n = 14 n + HCl > 2H2O acétone ou propanone ( cétone) (instable)carbone tétragonal ( lié à 4 groupes d"atomes) :le carbone est au centre d"un tétraèdre et les quatre liaisons sont
rbone trigonal ( lié à 3 groupes d"atomes) : structure triangle plan ( angles proches de 120°)
quotesdbs_dbs6.pdfusesText_12[PDF] chimie organique paul arnaud pdf gratuit
[PDF] chimie organique stéréochimie exercices corrigés pdf
[PDF] chimie organique terminale s cours
[PDF] chimie organique terminale s pdf
[PDF] chimie peinture pdf
[PDF] chimie pharmaceutique livre
[PDF] chimie pharmaceutique usthb
[PDF] chimie quantique cours pdf
[PDF] chimie quantique exercices et problèmes résolus
[PDF] chimie quantique pour les nuls
[PDF] chimie terminale d pdf
[PDF] chimie theorique exercices corriges pdf
[PDF] chimie théorique s5
[PDF] chimie tout en un pcsi dunod pdf
