 Les molécules de lair (modèles moléculaires)
Les molécules de lair (modèles moléculaires)
1°) Formules et molécules symboles et atomes : CO2 est la formule chimique du dioxyde de carbone. Le 2 indique le nombre d'atome d'oxygène. C est
 Jeu dominos molécules formules modèles moléculaires
Jeu dominos molécules formules modèles moléculaires
Formules et modèles moléculaires. Jeu de Dominos formule au modèle et du modèle à la formule. ... de dihydrogène. Une molécule de dioxyde de carbone.
 Chimie 1 Composition dune molécule- TCAP
Chimie 1 Composition dune molécule- TCAP
La masse molaire de la molécule d'eau se calcule donc ainsi : M (H2O) = 2 M(H) + M(O). 3) La représentation à l'aide des modèles moléculaires (modèle de Lewis).
 Les molécules de lair (modèles moléculaires)
Les molécules de lair (modèles moléculaires)
Lorsqu'on associe des atomes on obtient une particule de matière appelée molécule et représentée par une formule. D'autres particules appelées ions sont
 H2 N2 O2 O3 H2O CO2 ........... .............. ..............
H2 N2 O2 O3 H2O CO2 ........... .............. ..............
Chaque corps pur moléculaire possède un enchaînement d'atomes qui lui est Modèle dihydrogène. H2. 2 atomes d'hydrogène diazote. N2 … atomes d'azote.
 CHP 4 : les combustions les combustions les combustions
CHP 4 : les combustions les combustions les combustions
Complète alors le résumé ci-dessous en dessinant les modèles moléculaires. +. 3) Equation chimique de la combustion du carbone : L'équation ci-dessus s
 Exemple : C4H10 est la formule chimique du butane. Le C est le
Exemple : C4H10 est la formule chimique du butane. Le C est le
Dans deux molécules de butane il y aura donc 8 atomes de carbone et20 atomes d'hydrogène. Document 1 : Modèles moléculaires et formules.
 CHIMIE 3e 1. LEAU FICHE PÉDAGOGIQUE
CHIMIE 3e 1. LEAU FICHE PÉDAGOGIQUE
Construire (ou montrer) un modèle moléculaire éclaté et montrer un modèle compact. Faire reproduire le modèle éclaté. double de dihydrogène qui brûle en.
 LES ALCANES
LES ALCANES
Remplaçons l'un des atomes d'hydrogène du modèle moléculaire de l'éthane par un groupe méthyle - CH3 ; nous obtenons ainsi celui de la molécule de propane
 Applications de la chimie quantique. Surfaces de molybdène nues
Applications de la chimie quantique. Surfaces de molybdène nues
May 29 2007 Modèle pour la surface d'un nanotube de carbone. ... la détermination du nombre de molécules de dihydrogène greffées par centre métallique
 [PDF] Les molécules de lair (modèles moléculaires)
[PDF] Les molécules de lair (modèles moléculaires)
L'atome d'hydrogène a pour symbole H et est modélisé par une sphère blanche L'atome d'oxygène a pour symbole O et est modélisé par une sphère rouge L'atome de
 [PDF] Chimie 1 Composition dune molécule- TCAP
[PDF] Chimie 1 Composition dune molécule- TCAP
Exemple : la molécule d'eau dispose de 2 atomes d'Hydrogène et 1 atome d'Oxygène On placera le nombre d'atome de chaque type en indice à droite du symbole
 [PDF] Modélisation moléculaire
[PDF] Modélisation moléculaire
1 2 La mécanique moléculaire Cette technique calcule l'énergie des atomes (et non plus des électrons) au moyen d'approximations semi-classiques
 [PDF] Les atomes et les molécules - Physique-Chimie Créteil
[PDF] Les atomes et les molécules - Physique-Chimie Créteil
Voici les modèles et symboles des quatre atomes qui constituent 96 de la matière organique : modèle symbole Atome de carbone C Atome d'hydrogène
 [PDF] UTILISATION DES MODELES MOLECULAIRES ET DUN LOGICIEL
[PDF] UTILISATION DES MODELES MOLECULAIRES ET DUN LOGICIEL
Utiliser des modèles moléculaires et des logiciels de représentation Pré requis : o Modèle de l'atome Mots-clé o Espèces synthétique et naturelle
 [PDF] TP 14: DES ATOMES AUX MOLECULES (livre : chap9) - AlloSchool
[PDF] TP 14: DES ATOMES AUX MOLECULES (livre : chap9) - AlloSchool
La formule développée comme le modèle moléculaire donne la structure de la molécule (enchainement des atomes et nombre de liaisons) Chaque atome est
 [PDF] Atomes et molécules
[PDF] Atomes et molécules
Couleur du modèle carbone noir hydrogène blanc oxygène rouge 2 Formule et modèle de quelques molécules On représente une molécule par une formule
 [PDF] Composition de la boîte de modèles moléculaires
[PDF] Composition de la boîte de modèles moléculaires
Hydrogène H? (terminal) blanc 10 H1 terminal (s) H? 60 Carbone C(C4) noir 1 Tétraédrique (sp3) 1095° 25 C(C3) noir 4 Trigonal plan (sp2) 120°
 Dihydrogène - Wikipédia
Dihydrogène - Wikipédia
modifier · Consultez la documentation du modèle Le dihydrogène est la forme moléculaire de l'élément hydrogène qui existe à l'état gazeux L'hydrogène dans la transition énergétique [archive] [PDF] Ademe
Quel est le modèle moléculaire du dihydrogène ?
Le dihydrogène est la forme moléculaire de l'élément hydrogène qui existe à l'état gazeux aux conditions normales de température et de pression. La molécule comporte deux atomes d'hydrogène ; sa formule chimique est H2.Quel est le modèle moléculaire de H2O ?
H2O est la formule chimique de la molécule d'eau. Le 2 indique le nombre d'atomes d'hydrogène. H est le symbole de l'atome d'hydrogène. O est le symbole de l'atome d'oxygène.Comment construire un modèle moléculaire ?
Etant donné qu'une molécule est (par définition) un ensemble d'atomes liés entre eux, un modèle moléculaire est réalisé gr? à un “kit” comprenant : toujours des billes colorées symbolisant les atomes. parfois des tiges permettant d'associer les billes et symbolisant les liaisons.- L'hydrogène (H) est un gaz très léger dont la formule chimique est H2. Très inflammable, il est inodore, incolore, non toxique et non corrosif.
Pro-Ed, projet FAD II
1/5 Les pré-requis de l'école élémentaire n'ont pas été pris en compte
CHIMIE 3
e1. L'EAU FICHE PÉDAGOGIQUE
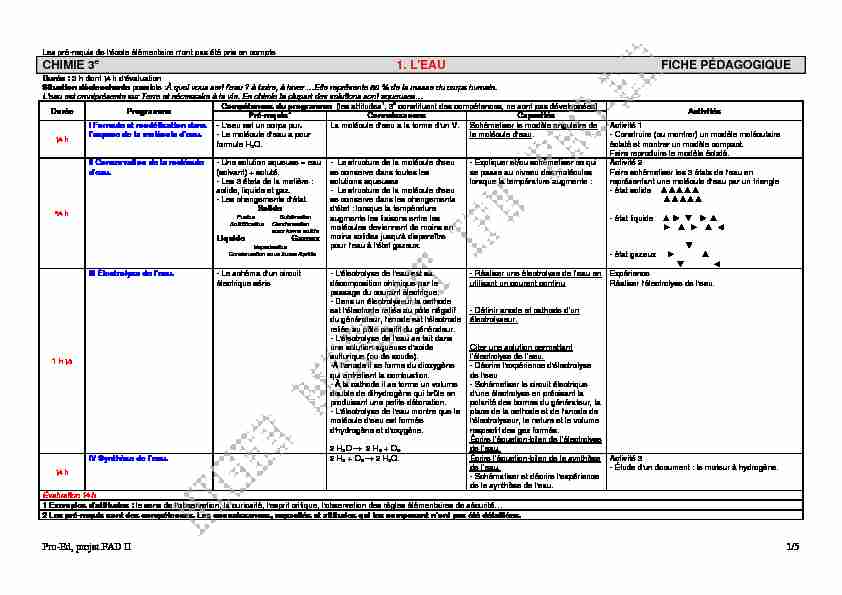
Durée : 3 h dont ¼ h d'évaluation
Situation déclenchante possible :À quoi vous sert l'eau ? à boire, à laver ...Elle représente 80 % de la masse du corps humain.
L'eau est omniprésente sur Terre et nécessaire à la vie. En chimie la plupart des solutions sont aqueuses...
Durée Programme Compétences du programme (les attitudes 1 , 3 e constituant des compétences, ne sont pas développées)Activités Pré-requis
2Connaissances Capacités
¼ h I Formule et modélisation dans
l'espace de la molécule d'eau. - L'eau est un corps pur. - La molécule d'eau a pour formule H 2O. La molécule d'eau a la forme d'un V.
Schématiser le modèle angulaire de
la molécule d'eau. Activité 1 - Construire (ou montrer) un modèle moléculaire éclaté et montrer un modèle compact.
Faire reproduire le modèle éclaté.
¾ h II Conservation de la molécule
d'eau. - Une solution aqueuse = eau (solvant) + soluté. - Les 3 états de la matière : solide, liquide et gaz. - Les changements d'état.Solide
Fusion Sublimation
Solidification Condensation
sous forme solideLiquide Gazeux
Vaporisation
Condensation sous forme liquide
- La structure de la molécule d'eau se conserve dans toutes les solutions aqueuses - La structure de la molécule d'eau se conserve dans les changements d'état : lorsque la température augmente les liaisons entre les molécules deviennent de moins en moins solides jusqu'à disparaître pour l'eau à l'état gazeux. - Expliquer et/ou schématiser ce qui se passe au niveau des molécules lorsque la température augmente : Activité 2 Faire schématiser les 3 états de l'eau en représentant une molécule d'eau par un triangle - état solide ŸŸŸŸŸ - état liquide Ÿ Ź ź Ź Ÿ - état gazeux Ź Ÿ ź Ż 1 h ½ III Électrolyse de l'eau. - Le schéma d'un circuitélectrique série
- L'électrolyse de l'eau est sa décomposition chimique par le passage du courant électrique. - Dans un électrolyseur la cathode est l'électrode reliée au pôle négatif du générateur, l'anode est l'électrode reliée au pôle positif du générateur. - L'électrolyse de l'eau se fait dans une solution aqueuse d'acide sulfurique (ou de soude). -À l'anode il se forme du dioxygène qui entretient la combustion. - À la cathode il se forme un volume double de dihydrogène qui brûle en produisant une petite détonation. - L'électrolyse de l'eau montre que la molécule d'eau est formée d'hydrogène et d'oxygène. 2 H 2O ĺ 2 H
2 + O 2 . - Réaliser une électrolyse de l'eau en utilisant un courant continu - Définir anode et cathode d'unélectrolyseur.
Citer une solution permettant
l'électrolyse de l'eau. - Décrire l'expérience d'électrolyse de l'eau - Schématiser le circuit électrique d'une électrolyse en précisant la polarité des bornes du générateur, la place de la cathode et de l'anode de l'électrolyseur, la nature et le volume respectif des gaz formés.Écrire l'équation-bilan de l'électrolyse
de l'eau.Expérience
Réaliser l'électrolyse de l'eau.
¼ h IV Synthèse de l'eau. 2 H
2 + O 2 2 H 2 O. Écrire l'équation-bilan de la synthèse de l'eau. - Schématiser et décrire l'expérience de la synthèse de l'eau. Activité 3 - Étude d'un document : le moteur à hydrogène.Évaluation ¼ h 1 Exemples d'attitudes : le sens de l'observation, la curiosité, l'esprit critique, l'observation des règles élémentaires de sécurité... 2 Les pré-requis sont des compétences. Les connaissances, capacités et attitudes qui les composent n'ont pas été détaillées.
Pro-Ed, projet FAD II
CHIMIE 3
e1. L'EAU FICHE PROFESSEUR
Le questionnement des élèves doit permettre de montrer l'importance de l'eau pour la vie sur Terre, d'où l'intérêt
de l'étudier en chimie.L'expérience de l'électrolyse de l'eau a été montrée lors d'une formation précédente.
I Formule et modélisation dans l'espace de la molécule d'eau.Objectif : construire un modèle de la molécule d'eau pour montrer aux élèves sa structure en V. Les propriétés
physiques et chimiques de l'eau sont dues à cette structure (dipôle électrique)Pré requis
- L'eau est un corps pur. - La molécule d'eau a pour formule H 2 O. Matériel : Modèle éclaté Modèle compactLaboratoire équipé Pas de laboratoire
Une boite de
modèles moléculairesModèle éclaté : 3 boules : 1
grosse ( 3 cm de diamètre) rouge, 2 petites ( 1 cm de diamètre) blanches ou naturelles.Elles peuvent être en terre
séchée, terre cuite, bois, pâteà modeler 2 bâtons ou pailles
( 8 cm de long) pour symboliser les liaisonsUn modèle compact peut être
fabriqué de la même façon.La molécule d'eau a la forme d'un V.
L'angle est légèrement supérieur à 90 °II Conservation de la molécule d'eau
Objectif : Expliquer et/ou schématiser ce qui se passe au niveau des molécules lorsque la température
augmente.Pré requis
- Une solution aqueuse = eau (solvant) + soluté. - Les 3 états de la matière : solide, liquide et gaz. - Les changements d'état. - La structure de la molécule d'eau se conserve dans toutes les solutions aqueuses- La structure de la molécule d'eau se conserve dans les changements d'état : lorsque la température augmente
les liaisons entre les molécules deviennent de moins en moins solides jusqu'à disparaître pour l'eau à l'état
gazeux.Le professeur peut schématiser les 3 états de l'eau en représentant une molécule par un triangle
- état solide ŸŸŸŸŸ État dense et ordonné ŸŸŸŸŸ - état liquide Ÿ Ź ź Ź Ÿ État dense et désordonné Ź Ÿ Ź Ÿ Ż - état gazeux Ź Ÿ État dispersé et désordonné ź Ż104,5 °
Indiquer seulement que l'angle est
légèrement supérieur à 90 °Pro-Ed, projet FAD II
III Électrolyse de l'eau.
Objectif : - réaliser un montage électrique
- acquérir le vocabulaire de l'électrolyse (électrode, anode, cathode, cuve à électrolyse)
- montrer que la molécule d'eau peut-être décomposée par le courant électrique et qu'il se forme du dioxygène et
du dihydrogènePré requis
: le schéma d'un circuit électrique sérieMatériel et produits
Laboratoire équipé Pas de laboratoire
- 1cuve à électrolyse - 2 éprouvettes à gaz - 1 générateur de courant continu ou des piles montées en série (6V) - 3 fils de jonction - 1 interrupteur - eau (distillée de préférence) - soude - allumettes - électrolyseur confectionné avec un fond de bouteille minérale percé à sa base pour enfiler 2 électrodes de graphite récupérées dans une pile usagée (pate à modeler ou colle pour rendre la cuve hermétique - 2 flacons pour recueillir les gaz formés - fils électriques - 4 piles R 20- L'électrolyse de l'eau est sa décomposition chimique par le passage du courant électrique.
- Dans un électrolyseur la cathode est l'électrode reliée au pôle négatif du générateur, l'anode est l'électrode
reliée au pôle positif du générateur. - L'électrolyse de l'eau se fait dans une solution aqueuse d'acide sulfurique (ou de soude). - À l'anode il se forme du dioxygène qui entretient la combustion.- À la cathode il se forme un volume double de dihydrogène qui brûle en produisant une petite détonation.
- L'électrolyse de l'eau montre que la molécule d'eau est formée d'hydrogène et d'oxygène.
2 H 2O ĺ 2 H
2 + O 2IV Synthèse de l'eau.
L'équation de la synthèse de l'eau est :
2 H 2 + O 2ĺ 2 H
2 OObjectif :
- comprendre un texte scientifique en relation avec ce qui vient d'être étudié - savoir restituer les informations - rédiger dans un français correct les réponsesLe professeur peut lire ce texte aux élèves, d'abord en entier, puis partie par partie afin qu'ils répondent aux
questions au fur et à mesure.Le moteur à hydrogène.
Actuellement, pour les moteurs qui équipent les voitures, l'essence (ou le diesel) est le carburant et le dioxygène
de l'air le comburant. La combustion du carburant apporte l'énergie.Le moteur à hydrogène est également un moteur à combustion, il utilise le dihydrogène comme carburant.
Il est souvent nommé improprement " moteur à eau ». L'avantage principal de ce moteur est la réduction des émissions polluantes. dihydrogène dioxygène GEprouvettes
à gaz
Eau + solution de soudeCuve à
électrolyse
AnodeCathode
GPro-Ed, projet FAD II
Sans évoquer les problèmes technologiques qui accompagnent la mise au point du moteur, on peut citer pour le
dihydrogène les problèmes de stockage :- il est fortement inflammable en présence du dioxygène de l'air et cela fait craindre les risques d'explosion
quand il est stocké en quantité ;- il est le plus petit élément chimique et peut traverser facilement les récipients, il faut donc utiliser des
matières spéciales empêchant toute fuite.D'autre part le dihydrogène n'existe pas à l'état naturel sur Terre, il doit être produit :
- par électrolyse de l'eau ;- par photosynthèse : sous l'action de la lumière certaines bactéries peuvent décomposer chimiquement l'eau
en dioxygène et dihydrogène ; - à partir du " reformage » d'hydrocarbures, composants du pétrole ;- par réaction chimique, par exemple la réaction d'une solution de soude sur de l'aluminium produit du
dihydrogène.Le moteur à hydrogène est aujourd'hui l'objet de nombreuses études et il pourrait équiper les voitures dans
l'avenir.Questions :
Le moteur à hydrogène :
1. La réaction de combustion du dihydrogène est identique à celle la synthèse de l'eau étudiée en cours. Écrire
l'équation-bilan de cette réaction.2. Compléter le tableau Carburant Comburant
Moteur à essence
Moteur à hydrogène
3. Pourquoi nomme-t-on le moteur à hydrogène " moteur à eau » et pourquoi cette dénomination n'est pas
correcte ?4. Donner le nom de quelques émissions polluantes produites par un moteur à essence.
5. Pourquoi évoque-t-on pour le dihydrogène des problèmes de stockage ?
6. À votre avis, pourquoi, malgré tous les problèmes que posent le stockage et la production du dihydrogène,
envisage-t-on de l'utiliser dans les voitures ?Corrigé :
1. 2 H
2 + O 2ĺ 2 H
2 O2. Compléter le tableau Carburant Comburant
Moteur à essence Essence ou diesel Dioxygène de l'air Moteur à hydrogène Dihydrogène Dioxygène de l'air3. On nomme le moteur à hydrogène " moteur à eau » car il produit de l'eau. Cette dénomination n'est pas
correcte car on pourrait croire que le carburant est l'eau (comme on dit " moteur à essence »)4. Noms de quelques émissions polluantes produites par un moteur à essence : dioxyde de carbone, oxydes
d'azote,5. On évoque pour le dihydrogène des problèmes de stockage car il est inflammable et qu'il est difficile de
trouver des récipients qui ne fuient pas.6. On envisage d'utiliser le dihydrogène dans les voitures car il est moins polluant et qu'on peut en fabriquer à
partir de ressources naturelles.Pro-Ed, projet FAD II
CHIMIE 3
e1. L'EAU PROPOSITION D'ÉVALUATION
Le texte sur le moteur à hydrogène peut être donné en évaluation. Le professeur lit une première fois le texte en
entier puis reprend la lecture en s'arrêtant pour que les élèves répondent aux questions.
Texte Barème
1. La réaction de combustion du dihydrogène est identique à celle la synthèse de l'eau étudiée en
cours. Écrire l'équation-bilan de cette réaction.2. Compléter le tableau Carburant Comburant
Moteur à essence
Moteur à hydrogène
3. Pourquoi nomme-t-on le moteur à hydrogène " moteur à eau » et pourquoi cette dénomination
n'est pas correcte ?4. Donner le nom de quelques émissions polluantes produites par un moteur à essence.
5. Pourquoi évoque-t-on pour le dihydrogène des problèmes de stockage ?
6. À votre avis, pourquoi, malgré tous les problèmes que posent le stockage et la production du
dihydrogène, envisage-t-on de l'utiliser dans les voitures ? 1 1 + 1 2 1+1 1Total 10
ouRéaliser un schéma annoté de l'électrolyse de l'eau. Décrire les réactions observées et les tests de
reconnaissance des gaz.Barème
Schéma annoté (½ pour le schéma, ½ pour le nom)Cuve à électrolyse
Solution de soude
Eprouvettes à gaz
Générateur
Fils de jonction
AnodeCathode
Qualité et propreté du schéma
Description
À l'anode il se forme du dioxygène qui entretient la combustion. À la cathode il se forme un volume double de dihydrogène qui brûle en produisant une petite détonation. 1 + 1 1 + 1Total10
quotesdbs_dbs33.pdfusesText_39[PDF] les fourberies de scapin résumé très court
[PDF] modèle compacte
[PDF] note de service horaire de travail ramadan
[PDF] respect des horaires de travail par le salarié
[PDF] note de service changement horaire de travail
[PDF] note de rappel exemple
[PDF] bayard anglais
[PDF] comment présenter la première page d'un exposé
[PDF] http enseignant digitheque belin fr login
[PDF] exemple de page de garde d'un exposé
[PDF] bayard education
[PDF] page de presentation histoire geographie
[PDF] ecolenumérique education gouv
[PDF] page de présentation anglais
