[PDF] les etats face ? la dette me corriger svp ;)
[PDF] les Etats facent aux acteurs transnationaux
[PDF] les etats financiers cours
[PDF] les etats financiers definition
[PDF] les états physiques de l'eau 5ème
[PDF] les états physiques de la matière
[PDF] Les etats unis !!
[PDF] Les Etats Unis ( une question)
[PDF] Les Etats Unis - Les grandes villes américaines
[PDF] Les états unis : une puissance culturelle
[PDF] les etats unis après la seconde guerre mondiale
[PDF] les etats unis dans la mondialisation
[PDF] Les Etats Unis dans la mondialisation ( Geographie
[PDF] les états unis dans la mondialisation 4ème
[PDF] les états unis dans la mondialisation 4ème control
MATIÈRE
FICHE DE
SYNTHÈSE
CARACTÉRISATION DES SUBSTANCES
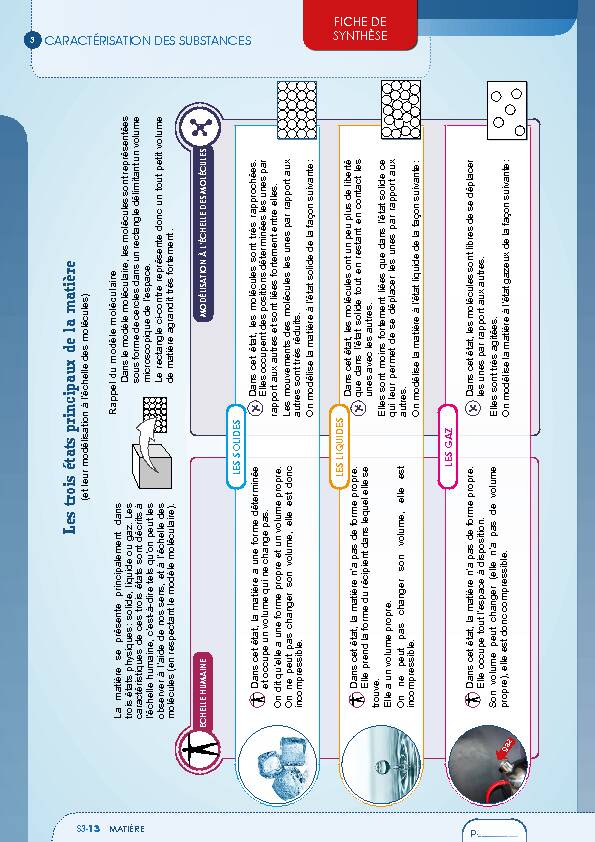
La matière se présente principalement dans trois états physiques : solide, liquide ou gaz. Les caractéristiques de ces trois états sont décrits à l"échelle humaine, c"est-à-dire tels qu"on peut les observer à l"aide de nos sens, et à l"échelle des molécules (en respectant le modèle moléculaire).
Rappel du modèle moléculaire
Dans le modèle moléculaire, les molécules sont représentées sous forme de cercles dans un rectangle délimitant un volume microscopique de l"espace.Le rectangle ci-contre représente donc un tout petit volume de matière agrandit très fortement .et occupe un volume qui ne change pas.
On dit qu"elle a une forme propre et un volume propre. On ne peut pas changer son volume, elle est donc incompressible.
Elle prend la forme du récipient dans lequel elle se
trouve. Elle a un volume propre. On ne peut pas changer son volume, elle est incompressible.ECHELLE HUMAINE
MODÉLISATION À L"ÉCHELLE DES MOLÉCULES
LES SOLIDES
LES LIQUIDES
LES GAZDans cet état, les molécules sont très rapprochées. Elles occupent des positions déterminées les unes par
rapport aux autres et sont liées fortement entre elles. Les mouvements des molécules les unes par rapport aux autres sont très réduits.On modélise la matière à l"état solide de la façon suivante :
que dans l"état solide tout en restant en contact les unes avec les autres.
Elles sont moins fortement liées que dans l"état solide ce qui leur permet de se déplacer les unes par rapport aux autres.On modélise la matière à l"état liquide de la façon su
ivante : les unes par rapport aux autres.
Elles sont très agitées. On modélise la matière à l"état gazeux de la façon suivante :
Elle occupe tout l"espace à disposition.
Son volume peut changer (elle n"a pas de volume propre), elle est donc compressible.
Les trois états principaux de la matière
(et leur modélisation à l'échelle des molécules)
MATIÈRE
FICHE DE
SYNTHÈSE
CARACTÉRISATION DES SUBSTANCES
augmentation de la température
Les changements d'état
A l'échelle humaine
Lorsque la température d"une matière varie, c"est-à-dire lorsque son énergie varie, elle peut changer d"état. Lorsque la température augmente, la matière à l"état solide va successivement passer à l"état liquide, puis à l"état gazeux. Les matière. solide liquide gaz Modélisation à l'échelle des molécules La température est une mesure de l"agitation moyenne des molécules. Lorsque la matière reçoit de l"énergie de son environnement, l"agitation des molécules augmente. A un niveau d"agitation donné, propre à chaque substance, les liens entre les molécules changent : c"est le changement d"état.
Nom des changements d'état
Lorsque la température augmente, la matière à l'état solide va successivement passer à l"état liquide, puis à l"état gazeux. Les noms des changements d"état que va subir la matière sont les suivants fusion vaporisation solide liquide gaz On regroupe l'évaporation et l'ébullition sous le terme de vaporisation. L"ébullition est une vaporisation rapide et désordonnée qui a lieu dans le liquide et qui ne commence qu"à une température précise. L"évaporation est une vaporisation spontanée et lente qui se produit à la surface du liquide et à toute température. Lorsque la température diminue, la matière à l'état gazeux va successivement passer à l"état liquide, puis à l"état solide. Les noms des changements d"état que va subir la matière sont les suivants solide liquide gaz ou condensation
MATIÈRE
T emps min) T empérature
°C)
température de fusion température d'ébullition
FICHE DE
SYNTHÈSE
CARACTÉRISATION DES SUBSTANCES
Evolution de la température d'une substance pure en fonction du temps (réchauffement) On effectue l'expérience suivante dans une enceinte fermée. On chauffe une substance pure - c'est-à-dire formée de molécules identiques - initialement à l"état solide. On mesure sa température à intervalles de temps réguliers et on reporte ensuite les mesures sur un graphique T emps min) T empérature
°C)
température de fusion température d'ébullition
Observations
On chauffe la matière, la température augmente. La matière est à l"
état solide.
On chauffe encore la matière, la température se stabilise. La matière change d"état, elle passe de l"état solide à l"état liquide : c"est la fusion. La température de fusion reste stable : elle ne varie pas tant qu"il reste encore de la matière à l"état solide dans le récipient. On se trouve sur un palier de température. On chauffe encore, la température augmente. La matière est à l"état liquide. Mais une partie se transforme déjà en vapeur (état gazeux), c"est l"évaporation. On chauffe encore la substance, la température se stabilise. La matière ch ange d"état, elle passe de l"état liquide à l"état gazeux : c"est l"ébullition. La température de vaporisation reste stable : elle ne varie pas tant qu"il reste encore de la matière à l"état liquide dans le récipient. On se trouve sur un palier de température qui correspond à la température d"ébullition. On continue à chauffer, la température augmente. La matière est à l"état gazeux o p q r
MATIÈRE
1
Température
température de fusion / so li dification température débullition / condensa tion chauffage refroidissement temps
FICHE DE
SYNTHÈSE
CARACTÉRISATION DES SUBSTANCES
Evolution de la température d'une substance pure en fonction du temps (refroidissement) On poursuit ensuite l'expérience en refroidissant la substance. On continue à mesurer sa température à intervalle de temps régulier et on obtient le graphique suivant 1
Température
température de fusion / so li dification température débullition / condensa tion chauffage refroidissement temps
Observations
On refroidit la substance, la température diminue. La matière est à l"état gazeux. On refroidit encore la substance, la température se stabilise. La matière change d"état, elle passe progressivement de l"état gazeux à l"
état liquide
: c"est la liquéfaction ou condensation. La température de condensation reste stable elle ne varie pas tant qu"il reste encore de la matière à l"état gazeux dans le récipient. On se trouve sur un palier de température. On refroidit encore, la température diminue. La matière est à l "état liquide. On refroidit encore, la température se stabilise. La matière change d"état, elle /DWHPSpUDWXUHGHVROLGLquotesdbs_dbs2.pdfusesText_2

 Les trois états principaux de la matière
Les trois états principaux de la matière