 Nombres quantiques et Orbitales Atomiques (OA)
Nombres quantiques et Orbitales Atomiques (OA)
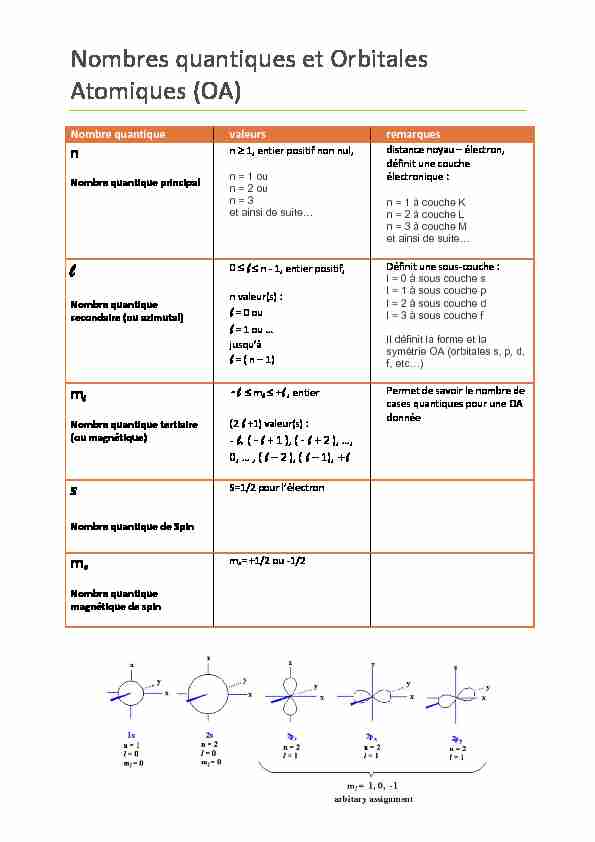
Nombres quantiques et Orbitales Atomiques (OA) Nombre quantique valeurs remarques n Nombre quantique principal n 1, entier positif non nul, n = 1 ou n = 2 ou n = 3 et ainsi de suite distance noyau – électron, définit une couche électronique : n = 1 à couche K n = 2 à couche L n = 3 à couche M
 Corrigé exercice 4 - PCSI
Corrigé exercice 4 - PCSI
Tous les autres quadruplets vérifient les conditions sur les nombres quantiques (( entier >0 ; 0≤ℓ≤ (−1 ; −ℓ≤ ℓ≤ℓ et 2=± $ ), donc peuvent bien décrire l’électron dans un atome On nomme l’orbitale à partir du tableau de nomenclature : ℓ=0 orbitale 4 ℓ=1 orbitale 5 ℓ=2 orbitale 6 ℓ=3 orbitale 8 ℓ=4
 Nombres quantiques et orbitales atomiques (2016-2017)
Nombres quantiques et orbitales atomiques (2016-2017)
Nombres quantiques et orbitales atomiques (2016-2017) I- Nombres quantiques L’état d’un éle tron dans un atome, ’est-à-dire : son énergie, ses mouvements autour du noyau, la forme de l’oritale, est défini par 4 paramètres appelés nombres quantiques a- Le nombre n, nombre quantique principal : n = 1, 2,
 Corrigé exercice 3 - PCSI
Corrigé exercice 3 - PCSI
La dégénérescence de ce niveau est de 16 , c’est-à-dire qu’il y a 16 états quantiques dans lequel peut se trouver l’électron au niveau ????= 4 ; en effet, les valeurs du nombre quantique secondaire ℓ peuvent
 Mecanique quantique Cours et exercices corriges
Mecanique quantique Cours et exercices corriges
Exercices 61 Chapitre3 FormalismedeDirac–Postulats(1) 63 3 1 Introduction 63 3 2 Prélude : espace des fonctions d’onde 63 3 3 Formalisme de Dirac 67 Annexe 3 A : Quelques rappels d’algèbre linéaire 78 Exercices 80 Chapitre4 Lamesure–Postulats(2) 81 4 1 Motivations 81 4 2 Les postulats de mesure 82 4 3 Valeur moyenne d’une observable 85
 Chapitre 5: Structure électronique des atomes
Chapitre 5: Structure électronique des atomes
L’état quantique de l’életron d’un atome est l’ensemle des valeurs pour ses quatre nombres quantiques n, l, m l et m s Exemple : (exercice 5 12 (p 150) + améliorations) Déterminez le nom re d’états quantiques possi les lorsque, simultanément, n=3 et l=2, et représentez leurs combinaisons Lorsque n=3, l peut valoir
 Kevin Moris Philippe Hermann
Kevin Moris Philippe Hermann
Chapitre 1 • Les lois de NewtonTable des matières 1 Configurations électroniques 1 1 1 Structure d’un atome 1 1 2 Cas de l’atome d’hydrogène 2 1 3 Les nombres quantiques 2 1 4 Atomes polyélectroniques 3 1 5 Schéma de Lewis des atomes 6 1 6 Cas des ions 6 Synthèse 7 Tests et exercices 8 Corrigés des exercices 10 2 Classification
 UE1 : Chimie – Chimie physique - CERIMES
UE1 : Chimie – Chimie physique - CERIMES
Parmi les triplets de nombres quantiques (n, l, m) suivants, déterminer Exercices Question 1 26 protons, 56 nucléons, 30 neutrons et 26 électrons
 1 Michel Le Bellac Correction d’une s´election des exercices
1 Michel Le Bellac Correction d’une s´election des exercices
Exercices du chapitre 1 1 6 1 Ordres de grandeur 1 Il faut utiliser des particules dont la longueur d’onde λsoit de 1 ˚A ou moins On utilisera λ= 1˚A dans les calculs num´eriques Pour les photons cela donne une ´energie en eV Ephot = hc λ = 6 63×10−34 ×3×108 10−10 ×1 6×10−19 = 1 24×104 eV = 12 4keV Pour les neutrons on
[PDF] représentation de lewis exercices pdf
[PDF] règle de klechkowski exception
[PDF] configuration electronique ion
[PDF] reséau informatique pdf
[PDF] reséau informatique ppt
[PDF] reséau informatique cours complet pdf
[PDF] reséau informatique cours ppt
[PDF] projet maintenance informatique pdf
[PDF] reséau informatique definition
[PDF] les droites ab et cd sont elles parallèles vecteurs
[PDF] exercice calculer les coordonnées du milieu d un segment
[PDF] exercices corrigés de stéréoisomérie
[PDF] exercices corrigés en stéreochimie
[PDF] projection de newman exercices corrigés
 Q RX Q
Q RX Q