 Chapitre 4 Équations chimiques
Chapitre 4 Équations chimiques
Dans toute réaction chimique la masse totale des réactifs est égale à la masse totale des produits. Donc
 I. Définition de léquation chimique
I. Définition de léquation chimique
ZnCℓ2 + H2. Page 3. V. Formules chimiques et équations chimiques. 123. Remarque : - Certains métaux peuvent réagir avec des acides dilués et donnent du
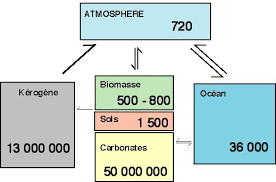 5 Équations chimiques et biochimiques du cycle du carbone 5.1.Les
5 Équations chimiques et biochimiques du cycle du carbone 5.1.Les
En combinant (1.2) et (1.1) on obtient l'équation 1. 2. CH2O + O2 --> CO2 + H2O. Écriture des demi-réactions d'oxydo-réduction. CH2O + H2O --
 Fiche Méthode Bilan chimique 1 : les équations chimiques
Fiche Méthode Bilan chimique 1 : les équations chimiques
FMch-1a bilan chimique 1/ STL Lycée Borde Basse. Page 1/1. Fiche. Méthode. Bilan chimique 1 : les équations chimiques. Signification d'une équation bilan.
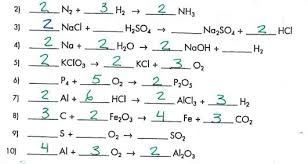 Exercices supplémentaires sur le balancement déquations
Exercices supplémentaires sur le balancement déquations
Exercices supplémentaires sur le balancement d'équations chimiques. 1- Balance les équations suivantes : FeS + O2. Fe2O3 + SO2. C3H8 + O2. CO2. + H2O. K2CrO4 +
 Calculs à partir des équations chimiques
Calculs à partir des équations chimiques
Significations de l'équation chimique: 1. L'alcool éthylique (ordinaire) brûle suivant l'équation non équilibrée: C2H6O + O2. CO2 + H2O.
 Comment choisir un logiciel permettant dapprendre à équilibrer les
Comment choisir un logiciel permettant dapprendre à équilibrer les
La réaction chimique : bilan conservation de la masse et des atomes. Technique opératoire de l'équation-bilan d'une réaction chimique déjà étudiée en classe.
 Le balancement déquations chimiques
Le balancement déquations chimiques
Complétez la phrase suivante. Le balancement d'équations chimiques se fait par l'ajout d'un devant la formule chimique de certains des et de certains des.
 Feuille de TD -Équations chimiques 1
Feuille de TD -Équations chimiques 1
Les équations chimiques nous permettent de modéliser la transformation des molécules et atomes dans une réaction chimique. Par exemple l'équation chimique.
 Règlements pour écrire les équations chimiques équilibrées
Règlements pour écrire les équations chimiques équilibrées
la droite d'une équation chimique. *Trucs pour équilibrer des équations chimiques : 1. Si un ion polyatomique existe à la gauche et à la droite de la flèche
 Exercices supplémentaires sur le balancement déquations
Exercices supplémentaires sur le balancement déquations
Exercices supplémentaires sur le balancement d'équations chimiques. 1- Balance les équations suivantes : FeS + O2. Fe2O3 + SO2. C3H8 + O2.
 Calculs à partir des équations chimiques
Calculs à partir des équations chimiques
Significations de l'équation chimique: 1. L'alcool éthylique (ordinaire) brûle suivant l'équation non équilibrée: C2H6O + O2. CO2 + H2O.
 Chapitre 4 Équations chimiques
Chapitre 4 Équations chimiques
Donc l'équation ionique nette est l'équation ionique totale à laquelle on a enlevé les ions spectateurs. Page 16. Ch4. 16. 2013. Équations ioniques (suite).
 5 Équations chimiques et biochimiques du cycle du carbone 5.1.Les
5 Équations chimiques et biochimiques du cycle du carbone 5.1.Les
En combinant (1.2) et (1.1) on obtient l'équation 1. 2. CH2O + O2 --> CO2 + H2O. Écriture des demi-réactions d'oxydo-réduction. CH2O + H2O --
 Écrire des équations chimiques équilibrées
Écrire des équations chimiques équilibrées
Pourquoi Équilibrer les équations? La théorie atomique: les atomes ne peuvent pas être crée ni détruit dans une réaction chimique ordinaire. La loi de la
 Chapitre 4 Ce sont les Chinois qui ont inventé les feux dartifice.
Chapitre 4 Ce sont les Chinois qui ont inventé les feux dartifice.
des réactifs et des produits est modifiée. d. Lors d'une transformation chimique seules les liaisons entre les atomes qui participent à une réaction chimique
 Feuille de TD -Équations chimiques 1
Feuille de TD -Équations chimiques 1
Les équations chimiques nous permettent de modéliser la transformation des molécules et atomes dans une réaction chimique. Par exemple l'équation chimique.
 Chapitre 4 Équations chimiques
Chapitre 4 Équations chimiques
Dans toute réaction chimique la masse totale des réactifs est égale à la masse totale des produits. Donc
 Le balancement déquations chimiques
Le balancement déquations chimiques
Complétez la phrase suivante. Le balancement d'équations chimiques se fait par l'ajout d'un devant la formule chimique de certains des et de certains des.
 Equilibrer les équations suivantes : a) b) c) d) ? 5 CO2 + 4 H2O e
Equilibrer les équations suivantes : a) b) c) d) ? 5 CO2 + 4 H2O e
Exercices : équation-bilan. I- Equilibrer les équations suivantes : Ajuster les nombres stœchiométriques des équations chimiques ci-dessous.