 Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude d'une réaction : titrage des ions fer II par les ions permanganate. I – Généralités sur les titrages. 1) Objectif d'un titrage. Il permet à l
 LES RÉACTIONS DOXYDORÉDUCTION DANS LES TITRAGES
LES RÉACTIONS DOXYDORÉDUCTION DANS LES TITRAGES
Le réactif titré est l'ion fer (II) et le réactif titrant est l'ion permanganate. 13. L'équation de la réaction support de ce titrage est : MnO4. —(aq) + 8H+
 Titrage des ions fer II
Titrage des ions fer II
Il a fallu verser un volume VBéq de la solution de permanganate de potassium de concentration cB pour atteindre l'équivalence. Quelle est la relation entre cA
 Détermination dune quantité de matière Fiche
Détermination dune quantité de matière Fiche
On ajoute progressivement une solution d'ions permanganate (solution titrante) à une solution d'ions fer (II) (solution titrée) en milieu acide. Le volume
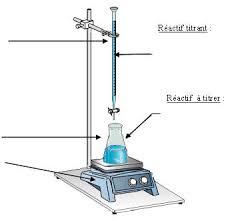 TP- Dosage des ions Fer II dans un produit anti- mousse
TP- Dosage des ions Fer II dans un produit anti- mousse
Alors que l'on ajoute de la solution aqueuse de permanganate de potassium de couleur violette dans le tube la le mélange reste incolore. Q2-2 : Une réaction
 Dosage du fer ferreux La manganimétrie est une technique
Dosage du fer ferreux La manganimétrie est une technique
Dosage du fer (II) en solution aqueuse. On utilisera Ecrire l'équation chimique de la réaction entre les ions Fe (II) et les ions permanganate en milieu.
 TP N° 03 : DOSAGE DES IONS FER (II) PAR COLORIMETRIE
TP N° 03 : DOSAGE DES IONS FER (II) PAR COLORIMETRIE
Mettre en marche l'agitation (pas trop forte !). • On effectue un premier titrage rapide verser mL par mL la solution de permanganate de potassium. • Arrêter
 TP- Dosage des ions Fer (II) dans un produit anti-mousse
TP- Dosage des ions Fer (II) dans un produit anti-mousse
ions fer (II) Fe2+ et les ions permanganate. MnO4. -. Cette réaction servira ensuite de réaction support au dosage. Expérience n°1 : - Dans un tube à essais ...
 Dosage potentiométrique
Dosage potentiométrique
DOC3 : Courbe théorique du dosage des ions permanganate par les ions fer II. Etudions l'exemple du dosage des ions fer Fe2+ par les ions permanganate MnO4. -.
 Untitled
Untitled
5.2: dosage du Fe(II) par le permanganate. 1. 1. 1. Page 3. RIENCES. 5 fer(II) sont en partie oxydés par les ions nitrates. 4) Pourquoi le permanganate dans ...
 Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude d'une réaction : titrage des ions fer II par les ions permanganate. I – Généralités sur les titrages. 1) Objectif d'un titrage.
 TP 13 DOSAGE des IONS FER (II) contenus dans le SEL de MOHR
TP 13 DOSAGE des IONS FER (II) contenus dans le SEL de MOHR
une solution aqueuse de concentration connue en ion fer (II) dosage des ions. 2+. (aq). Fe de S1 par une solution acidifiée de permanganate de potassium.
 Compte rendu du TP de chimie n°9 Les dosages rédox
Compte rendu du TP de chimie n°9 Les dosages rédox
II) Dosages des ions Fe2+ réagir avec un oxydant tel l'ion permanganate MnO4 ... d'hydroxyde de fer (II) en présence d'ions fer (II) Fe2+. (aq) selon.
 LES RÉACTIONS DOXYDORÉDUCTION DANS LES TITRAGES
LES RÉACTIONS DOXYDORÉDUCTION DANS LES TITRAGES
Partie A : L'ion permanganate un bon oxydant. L'ion permanganate est un bon tion d'oxydoréduction entre le fer et le dioxygène dissout dans l'eau.
 Titrage des ions fer II
Titrage des ions fer II
Il a fallu verser un volume VBéq de la solution de permanganate de potassium de concentration cB pour atteindre l'équivalence. Quelle est la relation entre cA
 TP- Dosage des ions Fer (II) dans un produit anti-mousse
TP- Dosage des ions Fer (II) dans un produit anti-mousse
Cette partie permet d'étudier la réaction entre les ions fer (II) Fe2+ et les ions permanganate. MnO4. -. Cette réaction servira ensuite de réaction support
 TP- Dosage des ions Fer II dans un produit anti- mousse
TP- Dosage des ions Fer II dans un produit anti- mousse
Q2-2 : Une réaction chimique a-t-elle eu lieu ? Si oui quel réactif pouvez-vous déjà identifier ? L'expérience 2 prouve que les ions permanganate
 TP14 – Titrages avec suivi potentiométrique
TP14 – Titrages avec suivi potentiométrique
Titrage par précipitation des ions chlorure par les ions argent(I) : Titrage redox des ions fer(II) par les ions permanganate :.
 Loxalate de fer (II)
Loxalate de fer (II)
I. Dosage des ions fer (II) et des ions oxalate dans le complexe Fe2+ seuls à l'aide d'une solution de permanganate de potassium et de poudre de zinc.
 Ex 3 Constante déquilibre On considère la réaction entre les ions
Ex 3 Constante déquilibre On considère la réaction entre les ions
On considère la réaction entre les ions permanganate et les ions fer II. Données : potentiels standards à 298 K. ? couple MnO?. 4(aq)/Mn2+ : E0.