 Cours Atomistique(1).pdf
Cours Atomistique(1).pdf
1. Chapitre 1: Structure de l'atome ; Constituants de la matière. Avant propos: Ce cours de Structure de l'atome Constituants de la matière est destiné aux
 Chapitre 1 : Atomistique
Chapitre 1 : Atomistique
La chimie est la science de la matière et de sa transformation. Au cours de ce chapitre nous étudierons les « briques élémentaires » de la matière : les atomes.
 COURS DE CHIMIE ATOMISTIQUE
COURS DE CHIMIE ATOMISTIQUE
Celle-ci est caractérisée par sa masse et son énergie qui mesure sa capacité à produire du travail. I-1 Structure de la matière. La matière est formée à partir
 Atomistique et Chimie Organique Cours et Exercices Corrigés
Atomistique et Chimie Organique Cours et Exercices Corrigés
4 orbitales moléculaires (liaisons chimiques) de type σ entre
 SUPPORT PAPIER DU COURS NECESSAIRE TRES UTILE
SUPPORT PAPIER DU COURS NECESSAIRE TRES UTILE
[1] J. Mesplède J.-L. Queyrel
 Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
carbone. ➢ Unité de masse atomique : uma. Par définitionl'uma est le 1/12 de la masse d'un atome de carbone 12
 COURS DE CHIMIE ATOMISTIQUE
COURS DE CHIMIE ATOMISTIQUE
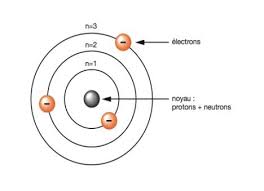
masse qui contient Z protons et (A-Z) neutrons et de Z e- qui assurent la neutralité de l'atome. Comment se situe les e- par rapport à ce noyau ? III-1
 COURS Atomistique 1er Semestre
COURS Atomistique 1er Semestre
CHAPITRE STRUCTURE DE L'ATOME. I.1 Historique. • Découvert il y'a 2500 ans par les Grecs. • « Atomos » = indivisible. • Expériences menées entre 1875 – 1910
 COURS DATOMISTIQUE
COURS DATOMISTIQUE
Conclusion : Toute la masse de l'atome est concentrée dans le noyau. III- IDENTIFICATION DES ELEMENTS. 1- Représentation. A chaque élément chimique on a
 Cours dAtomistique
Cours dAtomistique
- Chimie Générale Cours 1 – Atomistique : Structure de l'atome (1/2)
 Chapitre 1 : Atomistique
Chapitre 1 : Atomistique
La chimie est la science de la matière et de sa transformation. Au cours de ce chapitre nous étudierons les « briques élémentaires » de la matière : les atomes.
 Chapitre 1 : Atomistique
Chapitre 1 : Atomistique
La chimie est la science de la matière et de sa transformation. Au cours de ce chapitre nous étudierons les « briques élémentaires » de la matière : les atomes.
 Cours Atomistique(1).pdf
Cours Atomistique(1).pdf
1. Chapitre 1: Structure de l'atome ; Constituants de la matière. Avant propos: Ce cours de Structure de l'atome Constituants de la matière est.
 COURS Atomistique 1er Semestre
COURS Atomistique 1er Semestre
CHAPITRE STRUCTURE DE L'ATOME. I.1 Historique. • Découvert il y'a 2500 ans par les Grecs. • « Atomos » = indivisible. • Expériences menées entre 1875 – 1910
 SUPPORT PAPIER DU COURS NECESSAIRE TRES UTILE
SUPPORT PAPIER DU COURS NECESSAIRE TRES UTILE
[1] J. Mesplède J.-L. Queyrel
 Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
COURS. ATOMISTIQUE/LIAISON CHIMIQUE. Réalisé par : Pr. Hamid MAGHAT Par définitionl'uma est le 1/12 de la masse d'un atome de carbone 12 (.
 Atomistique et Chimie Organique Cours et Exercices Corrigés
Atomistique et Chimie Organique Cours et Exercices Corrigés
4 orbitales moléculaires (liaisons chimiques) de type ? entre
 COURS DATOMISTIQUE
COURS DATOMISTIQUE
Conclusion : Toute la masse de l'atome est concentrée dans le noyau. III- IDENTIFICATION DES ELEMENTS. 1- Représentation. A chaque élément chimique on a
 COURS DE CHIMIE N°1 ATOMISTIQUE ET LIAISON CHIMIQUE L
COURS DE CHIMIE N°1 ATOMISTIQUE ET LIAISON CHIMIQUE L
Définition : 1 uma = m12c / 12. 1 mole d'atome de l'isotope de 12C = 12000000 g. La masse d'un atome de C est donnée par mC = 12/N g avec N=6
 COURS DE CHIMIE N°1 ATOMISTIQUE ET LIAISON CHIMIQUE L
COURS DE CHIMIE N°1 ATOMISTIQUE ET LIAISON CHIMIQUE L
Définition : 1 uma = m12c / 12. 1 mole d'atome de l'isotope de 12C = 12000000 g. La masse d'un atome de C est donnée par mC = 12/N g avec N=6