 ISO 13485:2016 Foire aux questions
ISO 13485:2016 Foire aux questions
1 mar. 2016 BSI vous évaluera par rapport à la norme ISO. 13485:2016 une fois votre transition débutée. Si vous décidez de ne pas débuter la transition ...
 Auditeur Interne - ISO 13485:2016
Auditeur Interne - ISO 13485:2016
ISO 13485:2016. Objectifs pédagogiques : • Parvenir à une meilleure compréhension de la norme ISO 13485:2016 et la façon dont elle s'applique à votre.
 CERTIFICAT CERTIFICATE OF REGISTRATION ISO 13485 : 2016
CERTIFICAT CERTIFICATE OF REGISTRATION ISO 13485 : 2016
ISO 13485 : 2016 / EN ISO 13485 : 2016. Début de validité. Valable jusqu'au. / Effective date. / Expiry date : March 27th 2023 (included). October 29th
 la mise en place dun système de management de la qualité
la mise en place dun système de management de la qualité
4 juil. 2019 Pendant que la norme ISO 13485 : 2016 maintient les exigences relatives à la documentation des processus clés et de la documentation associée ...
 New England Biolabs Inc. ISO 13485:2016
New England Biolabs Inc. ISO 13485:2016
ISO 13485:2016. For and on behalf of NQA USA. K. 14124. Certificate Number: 34. EAC Code: August 15
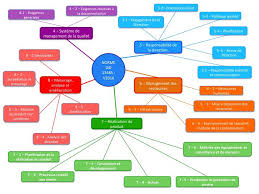 Les différents sous articles des critères de la norme ISO 13485 : 2016
Les différents sous articles des critères de la norme ISO 13485 : 2016
Les différents sous articles des critères de la norme ISO 13485 : 2016 - Les sous articles > Les critères de l'article 4. 4. 1. Les critères de l'article 4.
 ISO 13485:2016
ISO 13485:2016
ISO 13485:2016. • Décrire les exigences de l'ISO 13485:2016. • Expliquer comment interpréter les exigences de la norme au sein d'une organisation. • Développer ...
 Article de la norme ISO 13485 : 2016
Article de la norme ISO 13485 : 2016
Présentation des différents article de la norme ISO 13485 : 2016 > Sous articles du critère 4 - Système de management de la qualité.
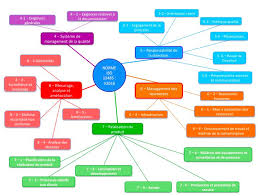 PROJET : Aide à lappropriation de la norme ISO 13485 : 2016
PROJET : Aide à lappropriation de la norme ISO 13485 : 2016
Afin d'appréhender les différentes parties de la norme ISO 13485 : 2016 nous avons pensé à élaborer une solution qui se devait d'être une approche processus.
 ISO 13485
ISO 13485
Pour en savoir plus sur la transition vers ISO 13485:2016 vous pouvez vous renseigner auprès de votre organisme de certification. De plus amples informations
 Commission Implementing Decision (EU) 2022/6
Commission Implementing Decision (EU) 2022/6
5 janv. 2022 harmonised standards EN ISO 10993-9:2009 EN ISO 10993-12:2012
 CERTIFICAT CERTIFICATE OF REGISTRATION ISO 13485:2016
CERTIFICAT CERTIFICATE OF REGISTRATION ISO 13485:2016
ISO 13485:2016. Début de validité. Valable jusqu'au. / Effective date. / Expiry date : December 9th 2021 (included). December 17th
 CERTIFICAT CERTIFICATE OF REGISTRATION ISO 13485 : 2016
CERTIFICAT CERTIFICATE OF REGISTRATION ISO 13485 : 2016
6 mai 2022 ISO 13485 : 2016 - NF EN ISO 13485 : 2016. GMED N° 31150–5. Ce certificat est délivré selon les règles de certification GMED.
 ILNAS-EN ISO 13485:2016/A11:2021
ILNAS-EN ISO 13485:2016/A11:2021
11 sept. 2021 Le présent amendement A11 modifie la Norme européenne EN ISO 13485:2016. Il a été adopté par le CEN le 12 avril 2021. Les membres du CEN et ...
 Untitled
Untitled
has been assessed and certified as meeting the requirements of. SUSTASIUOSGSGSCSGSGSGSGSGSGS. ISO 13485. SGS. USGSGSGSGSGSGSGSGSGSGSE. TESOSSASSESSE.
 ISO/TC 210/WG 1 N 233
ISO/TC 210/WG 1 N 233
18 nov. 2015 wg1N233 Draft White Paper - ISO Transition Planning Guidance for ISO 13485:2016. Replaces: N 224. Document type: Other committee document.
 ISO 13485:2016
ISO 13485:2016
EN ISO 13485:2016+AC:2016. Management system as per. Evidence of conformity with the above standard(s) has been furnished. Certificate registration No.
 ISO 13485:2016
ISO 13485:2016
Décrire les exigences de l'ISO 13485:2016. • Expliquer comment interpréter les exigences de la norme au sein d'une organisation.
 PROJET : Aide à lappropriation de la norme ISO 13485 : 2016
PROJET : Aide à lappropriation de la norme ISO 13485 : 2016
Aide à l'appropriation de la norme ISO 13485 : 2016 ». Laurine BEUZELIN Amaury DESGRANGES
 CERTIFICAT CERTIFICATE OF REGISTRATION NF EN ISO 13485
CERTIFICAT CERTIFICATE OF REGISTRATION NF EN ISO 13485
NF EN ISO 13485 : 2016. GMED N° 9462–7. Ce certificat est délivré selon les règles de certification GMED. Début de validité. Valable jusqu'au.
 [PDF] ISO 13485
[PDF] ISO 13485
ISO 13485:2016 tient compte des pratiques les plus récentes en matière de SMQ reflétant l'évolution technologique des dispositifs médicaux ainsi que les
 ISO 13485:2016(fr) Dispositifs médicaux
ISO 13485:2016(fr) Dispositifs médicaux
ISO 13485:2016(fr) Dispositifs médicaux — Systèmes de management de la qualité — Exigences à des fins réglementaires Medical devices — Quality management
 ISO 13485:2016 - Dispositifs médicaux
ISO 13485:2016 - Dispositifs médicaux
16600 CHF
 [PDF] Article de la norme ISO 13485 : 2016
[PDF] Article de la norme ISO 13485 : 2016
Présentation des différents article de la norme ISO 13485 : 2016 > Sous articles du critère 4 - Système de management de la qualité
 [PDF] Management de la qualité des dispositifs médicaux selon lISO 13485
[PDF] Management de la qualité des dispositifs médicaux selon lISO 13485
Management de la qualité des dispositifs médicaux selon l'ISO 13485: 2016 Université de Technologie Compiègne (UTC) Master 2 - Ingénierie de la Santé
 [PDF] ISO 13485:2016
[PDF] ISO 13485:2016
COPYRIGHT PROTECTED DOCUMENT © ISO 2016 Published in Switzerland All rights reserved Unless otherwise specified no part of this
 [PDF] NM ISO 13485 2016 - Fortrust : Consulting & Formation
[PDF] NM ISO 13485 2016 - Fortrust : Consulting & Formation
NM ISO 13485 : 2016 Dispositifs médicaux Système de management de la qualité Exigences à des fins réglementaires Notre formation au management de la
 CERTIFICATION ISO 13485 : 2016 - Polycert
CERTIFICATION ISO 13485 : 2016 - Polycert
CERTIFICATION ISO 13485 : 2016 Cette norme a été rédigée dans le but d'aider les fabricants de dis- positifs médicaux à concevoir des systèmes de gestion
 [PDF] E 22v16 Préparation à lISO 13485 - PQB
[PDF] E 22v16 Préparation à lISO 13485 - PQB
La deuxième édition est de 2003 Le texte de l'ISO 13485 s'appuie sur la norme ISO 9001 : Systèmes de management de la qualité – Exigences version 2008