 Exercices sur lélectrolyse
Exercices sur lélectrolyse
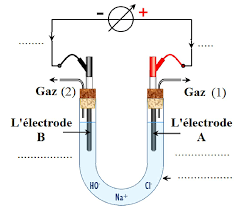
corrigé à l'anode oxydation des ions chlorures. 2 Cl- donne Cl. 2. + 2e- à la cathode réduction de l'eau. 2 H. 2. O + 2e- donne H. 2. + 2HO-. Danger !!! dans le
 Série électrolyse
Série électrolyse
Série électrolyse. Exercice 1 : Électrolyse de l'eau. Dans un électrolyseur on introduit 200 mL d'eau et 50 mL d'acide sulfurique ; on coiffe chaque électrode.
 electrolyse-et-synthese-de-leau-1.pdf
electrolyse-et-synthese-de-leau-1.pdf
EXERCICE 3: On réalise l'électrolyse de l'eau. 1) On recueille à la cathode 80 cm3 de gaz. Quel est son nom ? Comment peut-on l'identifier ?
 transformations-forcees-electrolyse-exercices-non-corriges-1.pdf
transformations-forcees-electrolyse-exercices-non-corriges-1.pdf
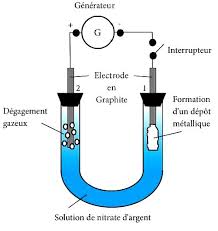
L'objectif de cette partie de l'exercice est d'étudier l'argenture d'une plaque de cuivre par électrolyse. Données : Recopier sur la feuille de rédaction
 Corrigé : Travaux Dirigés de la série 4 Exercice n°1 1-lélectrolyse d
Corrigé : Travaux Dirigés de la série 4 Exercice n°1 1-lélectrolyse d
Corrigé : Travaux Dirigés de la série 4. Exercice n°1. 1-l'électrolyse d'une solution de sulfate de cuivre CuSO4 : a- les Réactions de réduction possibles
 EXERCICE IV
EXERCICE IV
I-6- Donner le bilan de l'électrolyse et préciser la constante d'équilibre K′. mol-1 . 1 Faraday = 96500 C
 Conversion dénergie : piles et électrolyses
Conversion dénergie : piles et électrolyses
27 mar. 2022 Vous pouvez lire la page Wikipedia « pile à combustible » à ce sujet. 1/11 ... Exercice 6 : Électrolyse de l'alumine oral CCINP PSI
 PSI* 2020 – 2021 TD CHIMIE N°3 ELECTROLYSE Exercice 1
PSI* 2020 – 2021 TD CHIMIE N°3 ELECTROLYSE Exercice 1
ELECTROLYSE. Exercice 1 : Electrolyse du sulfate de cobalt (e3a PSI 2012 - extrait). Données nécessaires à la résolution de ce problème : - Potentiels
 DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
%20accu%20%26%20e%CC%81lectrolyse-Complet.pdf
 Exercices Cinétique électrochimique – Courbes intensité-potentiel
Exercices Cinétique électrochimique – Courbes intensité-potentiel
Correction en vidéo. Page 4. Usage personnel uniquement. 4. Exercice n° 2 : Électrolyse d'une solution d'ions cuivrique. On souhaite réaliser l'électrolyse d'
 EXERCICE IV
EXERCICE IV
I-7- Calculer les quantités des produits de l'électrolyse au bout d'une heure. I-8- Quelle a été l'intensité moyenne du courant pendant l'heure qu'a duré l'
 Corrigé : Travaux Dirigés de la série 4 Exercice n°1 1-lélectrolyse d
Corrigé : Travaux Dirigés de la série 4 Exercice n°1 1-lélectrolyse d
Corrigé : Travaux Dirigés de la série 4. Exercice n°1. 1-l'électrolyse d'une solution de sulfate de cuivre CuSO4 : a- les Réactions de réduction possibles
 Série électrolyse
Série électrolyse
Exercice 1 : Électrolyse de l'eau. Dans un électrolyseur on introduit 200 mL d'eau et 50 mL d'acide sulfurique ; on coiffe chaque électrode.
 Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Exercice n°4. On réalise simultanément l'électrolyse d'une solution de bromure de cuivre (II) (Cu2+. (aq) + 2 Br-. (aq)) dans un premier tube en U et.
 Liaisons chimiques (6 points) Deuxième exercice : Réalisation de la
Liaisons chimiques (6 points) Deuxième exercice : Réalisation de la
Troisième exercice : Électrolyse de l'eau (6 points). Le schéma ci-dessous représente Corrigé. Barème. Premier exercice : Liaisons chimiques (6 points).
 electrolyse-et-synthese-de-leau-1.pdf
electrolyse-et-synthese-de-leau-1.pdf
Exercice d'application. Au cours d'une électrolyse de l'eau on a recueilli 120 ml d'un gaz à la cathode. 1-de quel gaz s'agit-il ?
 Conversion dénergie : piles et électrolyses
Conversion dénergie : piles et électrolyses
Correction TD 26 : Conversion d'énergie : piles et électrolyses. Blaise Pascal PT 2020-2021. Exercice 2 : Pile argent-zinc.
 ( ) Na Cl +
( ) Na Cl +
L'objectif de cette partie de l'exercice est d'étudier l'argenture d'une plaque de cuivre par électrolyse. Données : Recopier sur la feuille de rédaction
 DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
%20accu%20%26%20e%CC%81lectrolyse-Complet.pdf
 Exercices Séquence n°10 Des synthèses forcées
Exercices Séquence n°10 Des synthèses forcées
EXERCICE 1 : Transformation spontanée ou forcée ? On réalise l'électrolyse d'une solution de bromure de cuivre (Cu2+. (aq) + 2 Br–.
 Electrolyse : Cours et Exercices corrigés-PDF - F2School
Electrolyse : Cours et Exercices corrigés-PDF - F2School
Electrolyse : Cours et Exercices corrigés PDF L'électrolyse (une transformation forcée) est un phénomène chimique lié au passage du courant électrique
 [PDF] Exercices sur lélectrolyse - F2School
[PDF] Exercices sur lélectrolyse - F2School
exercice 1: électrolyse d'une saumure préparation Cl 2 Une saumure est une solution concentrée de chlorure de sodium Les électrodes sont inattaquables A
 [PDF] Série électrolyse - AlloSchool
[PDF] Série électrolyse - AlloSchool
Exercice 1 : Électrolyse de l'eau Dans un électrolyseur on introduit 200 mL d'eau et 50 mL d'acide sulfurique ; on coiffe chaque électrode
 [PDF] transformations-forcees-electrolyse-exercices-non-corriges-1pdf
[PDF] transformations-forcees-electrolyse-exercices-non-corriges-1pdf
L'objectif de cette partie de l'exercice est d'étudier l'argenture d'une plaque de cuivre par électrolyse Données : Recopier sur la feuille de rédaction le
 [PDF] Corrigé : Travaux Dirigés de la série 4 Exercice n°1 1-lélectrolyse d
[PDF] Corrigé : Travaux Dirigés de la série 4 Exercice n°1 1-lélectrolyse d
1 Corrigé : Travaux Dirigés de la série 4 Exercice n°1 1-l'électrolyse d'une solution de sulfate de cuivre CuSO4 : a- les Réactions de réduction
 [PDF] PSI* 2020 – 2021 TD CHIMIE N°3 ELECTROLYSE Exercice 1
[PDF] PSI* 2020 – 2021 TD CHIMIE N°3 ELECTROLYSE Exercice 1
Exercice 1 : Electrolyse du sulfate de cobalt (e3a PSI 2012 - extrait) Données nécessaires à la résolution de ce problème : - Potentiels standard à 298 K :
 Electrolyse exercices de chimie de terminale S correction ts09chc
Electrolyse exercices de chimie de terminale S correction ts09chc
1)- Exercice 11 page 224 Le bilan de l'électrolyse d'une solution aqueuse de chlorure d'étain II
 [PDF] electrolyse-et-synthese-de-leau-1pdf - WordPresscom
[PDF] electrolyse-et-synthese-de-leau-1pdf - WordPresscom
Exercice d'application Au cours d'une électrolyse de l'eau on a recueilli 120 ml d'un gaz à la cathode 1-de quel gaz s'agit-il ?
 [PDF] EXERCICE IV - Toupty
[PDF] EXERCICE IV - Toupty
I-6- Donner le bilan de l'électrolyse et préciser la constante d'équilibre K? REPONSES A L'EXERCICE I I-1- Equation-bilan : Zn + Br2 ? Zn2+ + 2 Br-