|
Cinétique enzymatique à deux et plusieurs substrats
Cinétique enzymatique à deux et plusieurs substrats Dr DASSAMIOUR Page 2 INTRODUCTION Réactions enzymatiques Simples = rares (Isomérisation) G1-p G 6-p |
|
Cinétique enzymatique à deux substrats
L'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer l'ordre de fixation des substrats les constantes cinétiques |
|
Cinétique enzymatique à deux substrats
L'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer l'ordre de fixation des substrats les constantes cinétiques |
|
Enzymologie fondamentale
Chapitre 4 : Cinétique enzymatique à deux substrats Introduction Les réactions enzymatiques à un seul substrat sont rares Les enzymes catalysent des |
|
La Cinétique enzymatique À Un substrat
La Cinétique enzymatique À Un substrat Page 2 Définition de la cinétique 2- Quand la concentration initiale en substrat est très supérieure à Km (Km |
|
LA CINETIQUE ENZYMATIQUE
L'association enzyme-substrat (ES) est stabilisée par des liaisons de faibles énergie : liaisons hydrogène interactions hydrophobes liaisons ioniques 2 Le |
|
M1 Chimie des biomolécules (2021) Cinétique enzymatique
L'enzyme transforme un certain substrat mais le plus sou- vent elle ne réagit pas avec des molécules qui ressemblent au substrat (on parle d' analogues du |
|
Série de Travaux Dirigés N° 3 -:: UMI E-Learning ::
(Réactions enzymatiques à deux substrats) Exercice N°1 Une enzyme catalyse une réaction selon un mécanisme ordonné On mesure la vitesse initiale de la |
|
X Cinétique enzymatique X1 Notions de base X11 Vitesse de
Ordre 1 : la vitesse dépend de la concentration du substrat A P - Ordre 2 : la vitesse dépend de la concentration des deux substrats A + B P Page 3 |
Quelle est la relation entre l'enzyme et son substrat ?
L'enzyme fixe le substrat sur un site particulier, le site actif.
Le complexe enzyme substrat formé, la réaction chimique a lieu puis l'enzyme libère le ou les produits formés.
L'enzyme n'étant pas modifiée par la réaction, elle est immédiatement disponible pour fixer un autre substrat.Quel est le substrat de l'enzyme ?
En enzymologie, on désigne par substrat enzymatique toute molécule subissant une réaction chimique catalysée par une enzyme (ex : l'amidon est hydrolysé par l'amylase en glucose).
Il peut s'agir de molécules complexes, de polymères, de molécules simples (ex. : catalase dismutant du peroxyde d'hydrogène).Comment calculer la cinétique enzymatique ?
v = k x [S] Dans le cas de l'expérience B, la cinétique est linéaire, v est constante : La réaction est d'ordre zéro : réaction dont la vitesse ne dépend pas de la concentration des réactifs, la vitesse est donc constante.
- Le diagramme de Lineweaver-Burk permet, en mesurant la vitesse d'une réaction pour différentes concentrations de substrat, d'identifier Km et Vmax : les données forment une droite sur le graphe, qui intersecte l'axe des abscisses au point -1/Km, et l'axe des ordonnées au point 1/Vmax.
|
Chapitre VII - Cinétique enzymatique à deux substrats Introduction
Les réactions enzymatiques à un seul substrat sont rares. Les enzymes catalysent des réactions entre 2 ou 3 substrats. Dans les réactions à deux substrats il |
|
Série de Travaux Dirigés N° 3
(Réactions enzymatiques à deux substrats). Exercice N°1. Une enzyme catalyse De quel paramètre cinétique ne détermine-t-on pas la valeur ? Exercice N°5. La ... |
|
Cinétique enzymatique à deux substrats.
L'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer l'ordre de fixation des substrats les constantes cinétiques |
|
Cinétique enzymatique
cinétiques enzymatiques in vivo répondent à un mécanisme impliquant deux ou plusieurs substrats. Les enzymes adoptant ce modèle catalysent généralement le |
|
Enzymologie fondamentale
Chapitre 4 : Cinétique enzymatique à deux substrats. Introduction. Les réactions enzymatiques à un seul substrat sont rares. Les enzymes catalysent des |
|
Cinétique enzymatique à un seul substrat (Partie 1) CINETIQUE
(Voir le tableau 2 en fin de cour). La constante de spécificité kcat / KM : dans les conditions physiologiques la concentration en substrat [S] est rarement. |
|
M1. Chimie des biomolécules (2021) Cinétique enzymatique
4 Cinétique enzymatique stationnaire (réactions `a un seul substrat). 8. 4.1 Ce enzyme est en présence de deux substrats A et. B qu'elle peut transformer `a ... |
|
Chapitre VII - Cinétique enzymatique à deux substrats Introduction
Les réactions enzymatiques à un seul substrat sont rares. Les enzymes catalysent des réactions entre 2 ou 3 substrats. Dans les réactions à deux substrats il |
|
Cinétique enzymatique à deux substrats S P Page facebook
b) Réaction enzymatique à deux substrats. • Elle représente la majorité des réactions enzymatiques ;. • Ces réactions donnent de cinétique plus complexe que |
|
Cours dEnzymologie
XII.2. Les réactions à plusieurs substrats. Les réactions enzymatiques à un seul substrat sont rares. La majorité des cinétiques. |
|
Chapitre VII - Cinétique enzymatique à deux substrats Introduction
Les réactions enzymatiques à un seul substrat sont rares. Les enzymes catalysent des réactions entre 2 ou 3 substrats. Dans les réactions à deux substrats il |
|
Cinétique enzymatique à un seul substrat
En fait l'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer l'ordre de fixation des substrats |
|
Enzymologie fondamentale
Chapitre 3 : Cinétique enzymatique à un seul substrat et inhibition Chapitre 4 : Cinétique enzymatique à deux substrats. 1. Approche expérimentale… |
|
Série de Travaux Dirigés N° 3
(Réactions enzymatiques à deux substrats). Exercice N°1. Une enzyme catalyse une Déterminer le mécanisme et les paramètres cinétiques de cette réaction. |
|
Cinétique enzymatique
II. Définition. III. Rappel de base. IV. Cinétique enzymatique à un seul Soit la réaction catalysée par l'enzyme E qui transforme le substrat S en ... |
|
Cinétique enzymatique à deux substrats.
L'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer l'ordre de fixation des substrats les constantes cinétiques |
|
TD C. enz17
Cinétique enzymatique à 2 substrats Déterminer les constantes Vmax et Km pour chacun des deux substrats et la constante catalytique. |
|
Les enzymes allostériques
II. Vue d'ensemble sur le contrôle de l'activité enzymatique V. Propriétés cinétiques des enzymes allostériques. VI. Conclusion. |
|
L3 NUTRITION Enzymologie
Chapitre 2 : Catalyse Enzymatique. 2.2. 2.3. Chapitre 4 : Cinétique enzymatique à deux substrats. 3. Réactions à double déplacements impliquant la formation |
|
TD n° 01 : Enzymologie 1- Unités dactivité enzymatique
(Cinétique enzymatique à un substrat – absence d'inhibiteurs) Un enzyme catalyse une réaction entre deux substrats A et B. Nous avons effectués. |
|
Cinétique enzymatique à deux substrats - Eklablog
L'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer l'ordre de fixation des substrats les constantes cinétiques caractérisant la fixation de chacun d'eux en présence et en absence de l'autre ainsi que la vitesse maximale de la réaction qui est mesurée quand les deux substrats sont à concentration |
|
TRAVAUX DIRIGES CINETIQUES ENZYMATIQUES GBA 1
Cinétique enzymatique à 2 substrats I- Réaction enzymatique impliquant 2 substrats A et B Pour déterminer le mécanisme de la réaction différentes mesures de vitesse initiale en présence de concentrations variables de substrats sont effectuées Les vitesses sont exprimées en mM de produit apparu par minute |
|
La Cinétique enzymatique À Un substrat
réaction enzymatique S : La vitesse de la réaction est indépendante de la concentration en substrat: Réaction d’ordre 0 Faible quantité de S: La vitesse de la réaction est proportionnelle à la concentration en substrat: Réaction d’ordre 1 Travailler en concentration saturante en substrat |
Qu'est-ce que la cinétique enzymatique?
la cinétique enzymatique, c’estl’ét�s variations des vitesses de la réaction en fonction de la concentration du substrat •A quoi ça sert ? •Elle permet de déterminer :
Quels sont les substrats de la réaction enzymatique?
Les molécules sur lesquelles agit une enzyme sont définies comme les substrats de la réaction enzymatique.
Qu'est-ce que le complexe de substrat enzymatique ?
Les complexe de substrat enzymatique est une molécule temporaire formé quand un enzyme entre en contact parfait avec son substrat. Les substrat provoque un changement de conformation, ou un changement de forme, lorsque le substrat entre dans le site actif. Le site actif est la zone du enzyme capable de formant liens faibles avec le substrat.
Qu'est-ce que l'enzyme-complexe de substrat ?
Quand un enzyme lie son substrat, il forme un enzyme–complexe de substrat. Cette complexe diminue l’énergie d’activation du réaction et favorise sa progression rapide en fournissant certains ions ou groupes chimiques qui forment en fait des liaisons covalentes avec des molécules en tant qu’étape nécessaire de la réaction traiter.
| Chapitre VII - Cinétique enzymatique à deux substrats |
| Chapitre VII - Cinétique enzymatique à deux substrats les |
| La Cinétique enzymatique À Un substrat |
| II-CINETIQUE ENZYMATIQUE |
| CINETIQUE ENZYMATIQUE Cinétique enzymatique à un seul |
Quelle est la relation entre l'enzyme et son substrat ?
. Le nom de l'enzyme peut indiquer le nom du substrat sur lequel elle agit : la lactase catalyse l'hydrolyse du lactose, sucre du lait ; la maltase catalyse l'hydrolyse du maltose ; la saccharase catalyse l'hydrolyse du saccharose.
Comment calculer la cinétique enzymatique ?
. En d'autres termes, l'enzyme doit être spécifique au substrat pour que la structure protéique (et l'interaction entre les atomes) « épouse » le substrat.
Quel est le substrat le produit et l'enzyme impliqués dans la réaction enzymatique ?
. Il peut s'agir de molécules complexes, de polymères, de molécules simples (ex. : catalase dismutant du peroxyde d'hydrogène).
|
Cinétique enzymatique à deux substrats
L'étude cinétique des réactions enzymatiques à deux substrats a pour but de déterminer l'ordre de fixation des substrats, les constantes cinétiques caractérisant |
|
Enzymologie fondamentale
Chapitre 4 : Cinétique enzymatique à deux substrats Introduction Les réactions enzymatiques à un seul substrat sont rares Les enzymes catalysent des |
|
Cinétique enzymatique - Faculté de Médecine dOran
II Définition III Rappel de base IV Cinétique enzymatique à un seul substrat V modulation de l'activité enzymatique VI Cinétique à plusieurs substrats |
|
Enzymologie élémentaire - CHUPS Jussieu
19 jui 2002 · les termes d'enzymologie : enzyme, substrat, produit, coenzyme, activateur, Donner des exemples de cinétiques à deux substrats, ou avec |
|
ENZYMOLOGIE mezaini
Chapitre 4 : Cinétique enzymatique à deux substrats 3 Réactions à double Lorsque l'enzyme utilise 2 substrats on les désigne tous les deux en indiquant |
|
TD C enz17 - Moodle UM
Cinétique enzymatique à 2 substrats Déterminer les constantes Vmax et Km pour chacun des deux substrats et la constante catalytique (exprimée en s-1) |
|
36 Cinétique enzymatique - ESI
- La signification de la constante Km est évidente Lorsque [S] = Km, V = Vmax/2 Km est la concentration de substrat nécessaire pour que l'enzyme atteigne |
|
Cours 3 : Conclusions - (LISM) CNRS UMR7255
Comment comprendre la cinétique des réactions enzymatiques La vitesse de cette réaction depend des rencotres entre les deux substrats d[P] dt = −d[S] dt |
Université Pierre et Marie Curie - F2School
• Donner des exemples de cinétiques à deux substrats, ou avec coenzyme libre • Etudier la vitesse d’une réaction enzymatique en fonction du pH ou de la température • Etudier les variations de l’énergie libre du complexe enzyme-substrat au cours des phases de la réaction enzymatique
Interactions médicamenteuses et cytochromes P450
Tableaux des substrats, des inhibiteurs et des inducteurs Les substrats, les inhibiteurs et les inducteurs des cytochromes P450 les plus significatifs en clinique sont regroupés dans les 3 tableaux figurant sur la carte plastifiée jointe Ils constituent une mise à jour des versions publiées précédemment (10-11) L’utilisation de deux
Utilisation clinique de l étude des interactions - Edimark
Cela implique la présence d’au moins deux sites (ex :CYP 3A) Ce type de cinétique enzymatique est difficile à distinguer dans une représentation hyperbolique de Michaelis-Menten Il est La Lettre du Pharmacologue - Volume 14 - n° 5 - mai 2000 115 A DPC Utilisation clinique de l’étude des interactions médicamenteuses G Danan*, G
Interactions médicamenteuses et cytochromes P450
Tableaux des substrats, des inhibiteurs et des inducteurs Les substrats, les inhibiteurs et les inducteurs des cytochromes P450 les plus significatifs en clinique sont re-groupés dans les 3 tableaux joints sur la carte plastifiée Ils constituent une mise à jour des versions publiées pré-cédemment (10-11) L’utilisation de deux teintes
La myéloperoxydase des neutrophiles, une enzyme de défense
deux noyaux pyrroles, trois liaisons cova-lentes avec des acides aminés de la protéine: deux groupes méthyles modifiés sont liés respective-ment à un résidu aspartate (Asp94) et à un résidu glutamate (Glu242) Ces deux liaisons sont com-munes à toutes les peroxydases de mam-mifère (figure 1) La troisième liaison se forme entre le
Interactions avec les nouveaux antirétroviraux
viroc et l’étravirine (en ATU de cohorte) À ce jour, ces quatre nouveaux antirétroviraux disponibles sont indi - qués chez les patients en échec Chez ces patients, le traitement comprendra au moins deux molécules actives, appartenant à deux classes différentes, sélec-tionnées en fonction du profil génotypique des virus
Activité protéolytique de souches de lactobacilles
acidifiant (à 44·C et en cycle thermique), et sur leurprofil biochimique déterminé à J'aidedes ga-leries API 50 CH (Bouton, 1992) Les souches sont conservées à -80·C dans un milieu synthé-tique M17 ou MRS (selon qu'il s'agisse de strep-tocoques ou de lactobacilles), additionné de gly-cérol stérile à la concentration de 15 (v/v)
|
réactions impliquant plusieurs substrats - ESI
[PDF] réactions impliquant plusieurs substrats ESIesilrch esi umontreal ca Cinetique Cinetique%enzymatique pdf |
|
cinétique enzymatique - ESI
[PDF] cinétique enzymatique ESIesilrch esi umontreal ca Cinetique Cinetique%enzymatique pdf |
|
Cinétique enzymatique ? deux substrats
[PDF] Cinétique enzymatique ? deux substrats ekladata PapgfmfuOR coursMPINGPONG pdf |
|
Enzymologie élémentaire - UMVF
[PDF] Enzymologie élémentaire UMVFumvf cerimes media ressWikinu Biochimie Pbiochimie ee pdf |
|
Enzymologie élémentaire - CHUPS #8211; Jussieu - UPMC
[PDF] Enzymologie élémentaire CHUPS Jussieu UPMC chups jussieu polys biochimie EEbioch eebioch pdf |
|
cinétique enzymatique - Grenoble Sciences
[PDF] cinétique enzymatique Grenoble Sciences grenoble sciences viennot sites pdf |
|
Cinétique Michaelienne - Pages Persos Chezcom
[PDF] Cinétique Michaelienne Pages Persos Chez mon ftp a moi chez alice Ecole DEUG SV Enzymo pdf |
|
Cinétique Enzymatique Michaélienne 1 La réaction enzymatique
[PDF] Cinétique Enzymatique Michaélienne La réaction enzymatiquefdanieau free cours CinetiqueEnzymatiqueMichaelienne pdf |
|
Les Enzymes - cloudfrontnet
[PDF] Les Enzymes cloudfront dniqszobad cloudfront pdf febfaa pdf |
|
TD de Biochimie TD de Biochimie - Institut supérieur de l éducation
Exercice n° Comparaison cinétique des enzymes de la phosphorylation du glucose cinétiques de ces deux enzymes vis ? vis de leur substrat commun |
- cinétique enzymatique ? deux substrats exercices corrigés pdf
- mécanisme ordonné
- cinétique enzymatique ? deux substrats ppt
- mécanisme aléatoire dépendant
- cinétique enzymatique a deux substrats exercices
- exercice corrigé cinétique enzymatique
- enzymologie n°3 - réactions enzymatiques ? deux substrats
- mecanisme ping pong
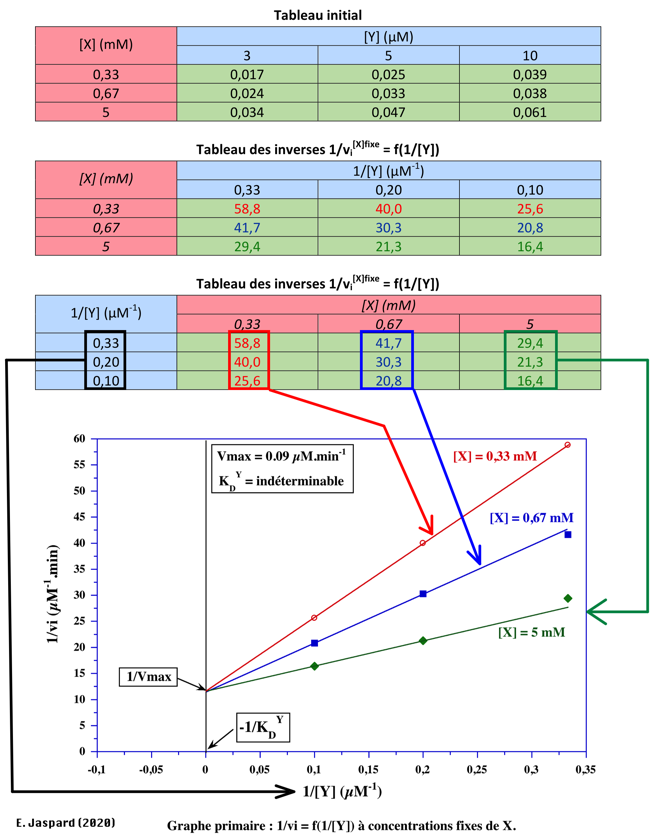
Cinétique Michaelienne - Pages Persos Chezcom
Source:http://biochimej.univ-angers.fr/Page2/TexteTD/2LicenceUE1/3TD2SUBSTRATS/1PremierSerieEXO/99LectureValeursDeY.png
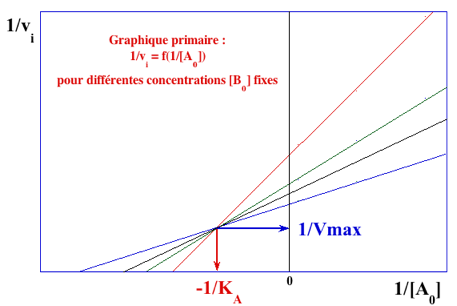
Correction Travaux diriges enzymologie deux substrats cinetique
Source:http://biochimej.univ-angers.fr/Page2/COURS/4EnzymologieLicence/4DeuxSUBSTRATS/7FigSequentiel/9GrPrimEtSecond/1GrPrimOrdonne.png

Cinetique enzymatique deux substrats hasard ordonne ping pong
Source:http://biochimej.univ-angers.fr/Page2/COURS/4EnzymologieLicence/4DeuxSUBSTRATS/ZFigureSUITE/9SuiteVmKmAuhasard.png
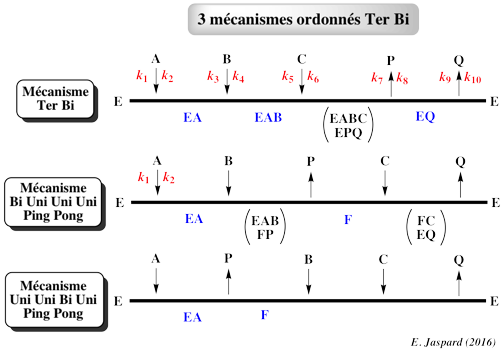
Cinetique enzymatique deux substrats hasard ordonne ping pong
Source:http://biochimej.univ-angers.fr/Page2/COURS/4EnzymologieLicence/4DeuxSUBSTRATS/6SuiteFigures/3TroisMecanismesTerBi.png
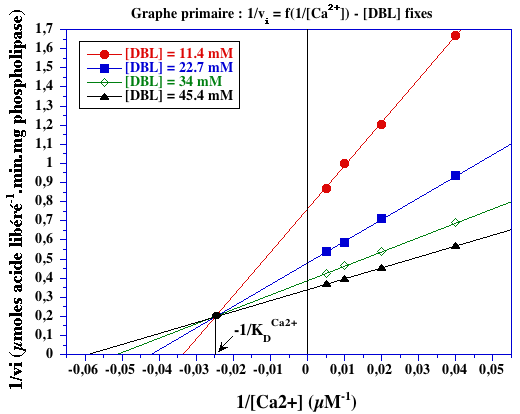
Cinetique enzymatique deux substrats hasard ordonne ping pong
Source:http://biochimej.univ-angers.fr/Page2/TexteTD/2LicenceUE1/3TD2SUBSTRATS/1PremierSerieEXO/5Exercice2/1GrCaAvecDBLfixe.png

Correction Travaux diriges enzymologie deux substrats cinetique
Source:http://biochimej.univ-angers.fr/Page2/COURS/4EnzymologieLicence/4DeuxSUBSTRATS/8Ping-PONG/1PingPongChymo.png
mise en évidence des sels minéraux dans le lait
CORRIGÉ TP 1 : Quels sont les principaux constituants du lait ? But
- mise en évidence des constituants du lait
- séparation des principaux constituants du lait
- (tp)mise en évidence des constituants du lait
- tp analyse du lait
- tp constituants du lait
- mise en évidence des lipides dans le lait
- test liqueur de fehling lait
- mise en évidence du calcium dans le lait
le lait et ses constituants st2s controle
PLANNING 1 ST2S CHIMIE
- programme 1ere st2s maths
- programme st2s terminale
- programme 1ere st2s physique chimie
- cours première st2s physique chimie
- 1ere st2s cours
- 1ere st2s programme biologie
- cours 1ere st2s maths
- premiere st2s emploi du temps
tp analyse du lait
AT - Analyses et contrôles du lait cru
- analyse microbiologique du lait cru de vache
- analyse microbiologique lait
- tp analyse microbiologique du lait
- analyse microbiologique du lait et des produits laitiers
- analyse microbiologique du lait pdf
- analyse bactériologique du lait
- analyse microbiologique du lait pasteurisé
- tp analyse microbiologique du lait cru de vache
mise en evidence des protéines
tests pour mettre en evidence [es constituants - Perennes SVT
- mise en évidence des lipides dans le lait
- protocole de mise en évidence des lipides
- mise en évidence des lipides rouge soudan
- test biuret protéine
- mise en évidence des glucides
- test du biuret svt
- mise en évidence des lipides pdf
- test du biuret protocole