| Chapitre 1 Acides et bases |
| Fiche de révisions sur les acides et les bases - Nicole Cortial |
| Transformations chimiques en solution aqueuse - Chimie en PCSI |
| Les couples acide-base conjuguées - La chimie |
| Les acides et bases en solution aqueuse - Groupe Transition |
| VIEtude sommaire des mélanges |
| § 7 (suite) Titrages acide-base - EPFL |
| COURS DE CHIMIE GENERALE Semestre 1 SVI - Ucama |
| PH et pKa - Eli Zysman-Colman |
| Chapitre n° : Notion d'acides et de bases fortes et faibles TP n |
| Déterminer si un acide est fort ou faible - archimede |
- l'acide chlorhydrique, solution aqueuse du chlorure d'hydrogène HCl ;
- l'acide sulfurique H
Quels sont les acides fort et faible ?
. Un acide appartenant à un couple acide-base de positif ne sera que partiellement transformé en ions H 3 O + : on dit qu'il s'agit alors d'un acide faible.
Quels sont les acides faibles ?
. Acides organiques comme les acides carboxyliques : acide méthanoïque, acide acétique. Acides minéraux : acide fluorhydrique (HF), acide hypochloreux (HOCl), acide borique (H3BO3), acide sulfureux (H2SO3), acide cyanhydrique (HCN).
Comment reconnaître acide fort acide faible ?
. Un acide A appartenant à un couple acide-base de pKa positif ne sera que partiellement transformé en ions H3O+ : on dit qu'il s'agit alors d'un acide faible.
Quelles sont les bases faible ?
. Pour un pKa négatif, on dit qu'elles sont « indifférentes ».
. L'acide1 se transforme en sa base conjuguée, et la base2 se transforme en son acide conjugué.
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
Les acides et bases en solution aqueuse - Groupe Transition
d'identifier, dans une liste donnée, les acides et les bases selon Brønsted ; Coefficient d'ionisation (de dissociation) d'un acide ou d'une base faible Comme NaOH et HCl sont des électrolytes forts, l'équation ionique doit s'écrire : Na + |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKa > 0 Dans le cas d'un acide fort, totalement dissocié dans l'eau, la concentration finale |
|
Déterminer si un acide est fort ou faible
Un acide est fort s'il de dissocie totalement lors de sa mise en solution On a alors la relation [H3O+]=C • Un acide est faible s'il se dissocie partiellement lors de |
|
Acides forts et bases fortes
La réaction n'est donc pas totale Les acides faibles sont d'autant moins dissociés dans l'eau qu'ils sont concentrés L'effet de la dilution tend |
|
Propriétés des acides et des bases
•pKa faible « Ka élevé : acide fort •pKa élevé « Ka faible : acide Les acides faibles en solution aqueuse se dissocient seulement partiellement, la majorité des |
|
PH et pKa - Eli Zysman-Colman
pKa = -log Ka Plus la valeur de pKa est faible, plus le Ka est grand, plus l'acide est fort 4 Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf |
|
VIEtude sommaire des mélanges
2) Acide fort 1 + acide faible 2 On calcule souvent le pH en négligeant l'acide faible Cette approximation grossière n'est justifiée que si l'apport d'ions |
ACIDE FAIBLE – BASE FAIBLE *** COUPLE ACIDE -BASE
• Préparation : c’est un mélange équimolaire d’acide faible et de base forte ou de base faible et d’acide fort : on se situe alors à la demi-équivalence : comme [ACIDE ] = [BASE ]⇒ pH = pKa Le pH de la solution tampon est correspond donc au pKa du couple acide/base 5 2 Zones de pré dominance des ions : Comme Ka =
Tables des pKa - Free
II – Acide faible et base conjuguée faible : Acide faible Base conjuguée faible pKa HO+ 3 H2O - 1,75 HClO3 − ClO3 0 Acide picrique HB B− 0,38 Acide trichloracétique HB B− 0,66 Acide benzène sulfonique HB B− 0,7 HBrO3 − BrO3 0,7 HIO3 − IO3 0,77 HSCN SCN− 0,8 H2CrO4 − HCrO4 0,8 H2P2O7 − HP2O7 0,85 Acide sulfamique HB B− 1,0
Chimie Exercice I : Acide fort ou faible ? Document 1 : Le
Exercice I : Acide fort ou faible ? Document 1 : Le venin des fourmis Lorsqu’elles se sentent en danger, les fourmis rousses projettent un venin sur leur agresseur Ce venin contient de l’acide formique concentré à plus de 50 Cet acide est un liquide incolore à l’odeur forte Il est
ACIDES ET BASES
acide conjugué, H 2O est faible 3) H 3 O H + H 2 O ← + → + Dans H 3O + la charge positive est portée par l'oxygène qui est un atome très électronégatif Sa tendance est donc de récupérer ses électrons en libérant le proton La dissociation est favorisée H 3O + est un acide fort et sa base conjuguée, l'eau est faible
IV Etude approximative des solutions acides et basiques diluées
Si le pH mesuré pour une solution d’acide est supérieur à celui auquel on s’attendrait pour un acide fort, il s’agit d’un acide faible La liste des acides faibles figure sur table en annexe Exemple: On mesure un pH de 2,1 pour une solution 0,1 molaire d’acide fluorhydrique Il ne peut s’agir d’un acide fort, sinon on
Fiche de révisions sur les acides et les bases
3°) Solution d’acide faible de concentration molaire C1 pH ≠−logC1 4°) Solution de base faible de concentration molaire C2 pH ≠14 +logC2 Les acides A1H et A 2H sont faibles Les bases − A1 et − A 2 sont faibles L’acide A1H est plus fort que l’acide A 2H ; la base − A 2 est plus forte que la base − A1
Thermodynamique chimique Chapitre 4 : Étude des titrages
2 Titrage d’un acide faible par une base forte et titrage d’une base faible par un acide fort III Titrages acido-basiques par suivi pH-métrique 1 Titrage d’un acide fort par une base forte et titrage d’une base forte par un acide fort 2 Titrage d’un acide faible par une base forte et titrage d’une base faible par un acide fort 3
GLUCIDES: LES OSES
En milieu acide faible les oses sont stables En milieu acide fort on observe des déshydratations et des cyclisations En milieu basique faible il y a des isomérisations En milieu basique fort il y oxydation et dégradation A Oxydation 1/ De la fonction aldéhyde
pH DES SOLUTIONS AQUEUSES I Généralités
a as d’un mono-acide fort HA Exemples de mono-acides forts Tableau 2: Exemples de mono-acides forts Soit C 0 moles d’un aide fort HA introduit à l’état pur dans 1 L d’eau et sans variation de volume aluler le pH de la solution ainsi obtenue HA + H 2O → A-+ H 3 O+ (Réaction totale) 2 H 2O ↔ H 3 O+ + OH-
|
Déterminer si un acide est fort ou faible - archimede
[PDF] Déterminer si un acide est fort ou faible archimedearchimede wifeo Dterminer si un acide est fort ou faible pdf |
|
Révisions sur les acides et les bases - Nicole Cortial
[PDF] Révisions sur les acides et les bases Nicole Cortialnicole cortial revisions rev ac bas pdf |
|
IV Etude approximative des solutions acides et basiques - LHCE
[PDF] IV Etude approximative des solutions acides et basiques LHCE lhce lu Chimie Publications PDF AB pdf |
|
Les acides et bases en solution aqueuse - Groupe Transition
[PDF] Les acides et bases en solution aqueuse Groupe Transition grptrans ulg ac be modules ac bas i pdf |
|
pH et pKa - Eli Zysman-Colman
[PDF] pH et pKa Eli Zysman Colman zysman colman courses chm Acidite pdf |
|
ACIDE FAIBLE #8211; BASE FAIBLE *** COUPLE ACIDE-BASE
[PDF] ACIDE FAIBLE BASE FAIBLE *** COUPLE ACIDE BASEclaude jeuch free gutenberg acidebase acbasfai PDF |
|
ACIDES ET BASES
[PDF] ACIDES ET BASESressources univ lemans AccesLibre UM Pedago ac=bases pdf |
|
Titrages acidobasiques de mélanges contenant une espèce forte et
[PDF] Titrages acidobasiques de mélanges contenant une espèce forte et eduscol education rnchimie chi gen titrages quanti pdf |
|
Le pH 3 Le pH des acides et bases forts - théorie - 2014
[PDF] Le pH Le pH des acides et bases forts théorie edu ge ch Le%pH%des%acides%et%bases%forts% file |
|
BTS BAT 1 Acide fort, base fort, acide faible, base faible
BTS BAT Acide fort, base fort, acide faible, base faible I ) Acide fort L ' acide chlorhydrique, un monoacide fort + + + HCl(g) + HO(l) HO+(aq) + |
- comment savoir si c'est un acide fort ou faible
- base forte ou faible
- chapitre 1 acide fort base forte
- comment savoir si un acide est fort ou faible
- acide fort ph
- acide faible ou fort
- acide fort pka
- base faible
CH 4 (Acide Base)
Source: Ph
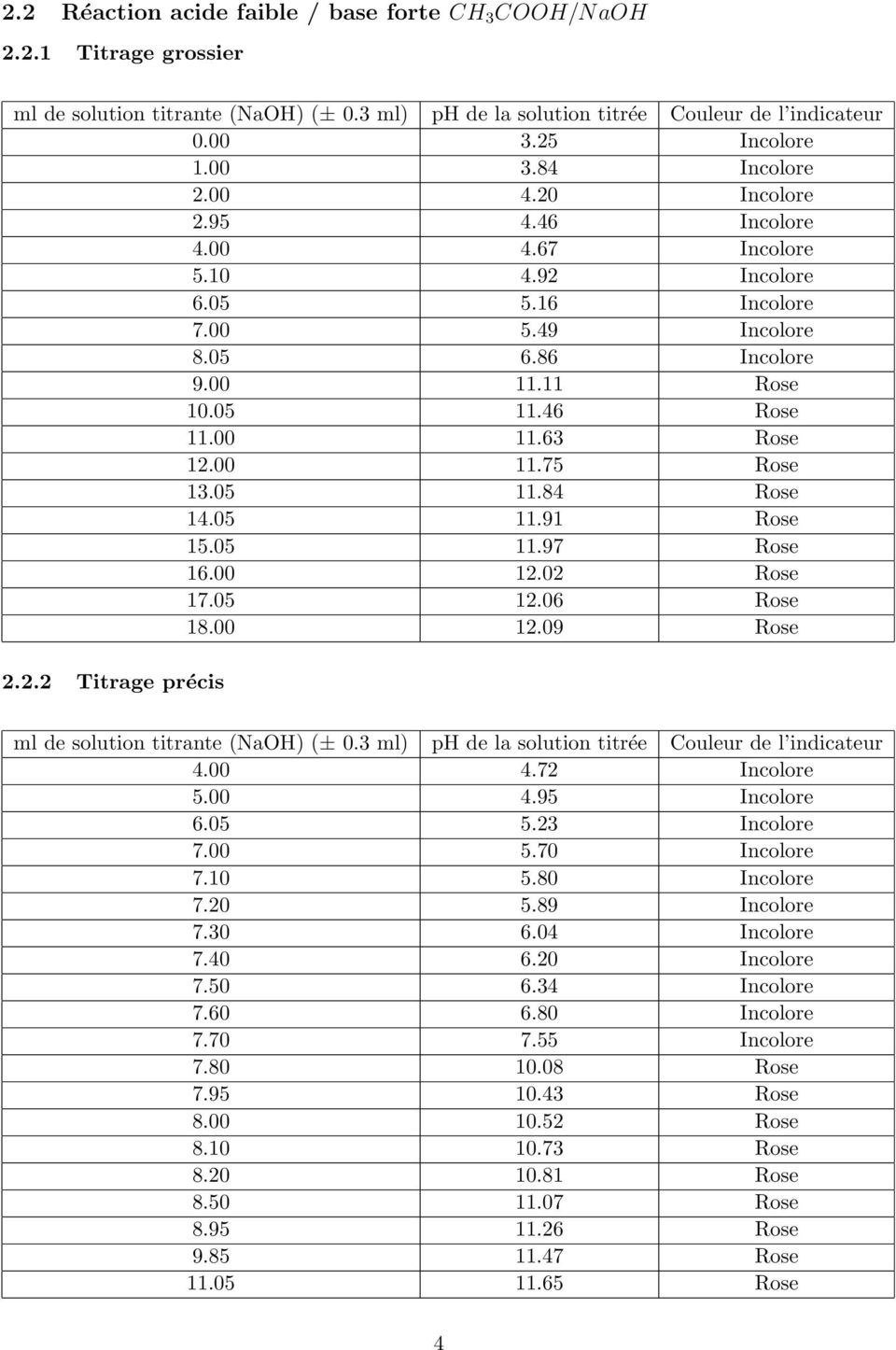
Cours de Chimie - Informatique Titrage acide/base - PDF Free Download
Source:https://docplayer.fr/docs-images/49/20287226/images/page_4.jpg
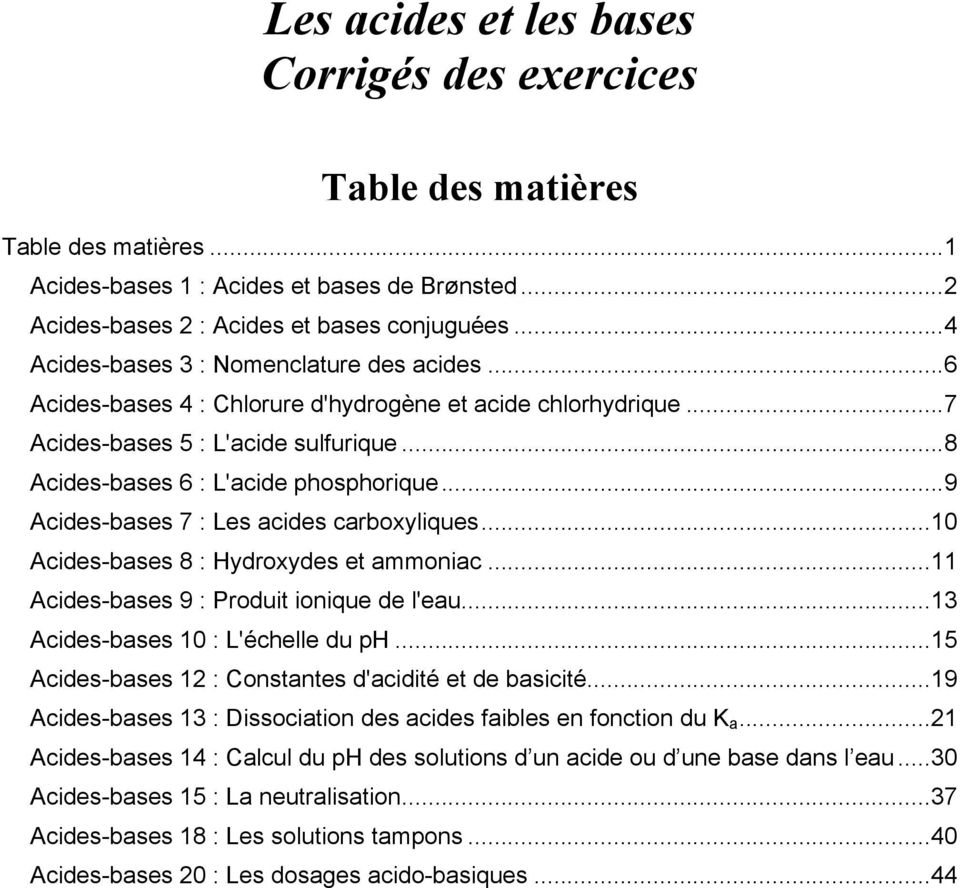
Rapport TP 2 : Titrage acide - base - PDF Free Download
Source:https://docplayer.fr/docs-images/40/6544693/images/page_1.jpg

Les acides et les bases Corrigés des exercices Table des matières
Source:https://docplayer.fr/docs-images/46/20841194/images/page_9.jpg

COURS DE CHIMIE N 4 REACTIONS ACIDE BASE Théorie de Brönsted - PDF
Source:https://books.openedition.org/irdeditions/docannexe/image/2821/img-20.jpg

Agriculture biologique en Martinique - Chapitre 5 Systèmes de
Source:https://s1.studylibfr.com/store/data/010037633_1-cba062296fdc59d84300cd91518d28bb.png
liste acs carso
liste ACS 2015_v2 - Ministère des Solidarités et de la Santé
- acs eurofins
- attestation de conformité sanitaire pdf
- attestation de conformité sanitaire acs
- conformité aux listes positives
- carso acs
liste activité commerciale
activités commerciales réglementées REGLEMENTAT - CCI Nancy
- nomenclature marocaine des activités 2016
- liste activité réglementée maroc
- liste des activités commerciales au maroc
- secteur et branche d'activité exemple
- les branches d'activité au maroc
- tableau de bord sectoriel maroc 2016
- nomenclature marocaine des activités 2015
- professions réglementées au maroc