 Travaux pratiques et travaux dirigés de biologie végétale
Travaux pratiques et travaux dirigés de biologie végétale
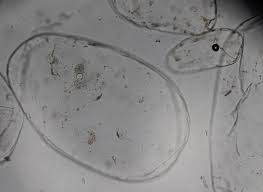
TP n°3 : Tissus végétaux. Séance I. Rappel : Chez la plupart des végétaux les différentes fonctions vitales sont assurées par des organes différents
 Polycopié Travaux pratiques Biologie végétale 1 année LMD
Polycopié Travaux pratiques Biologie végétale 1 année LMD
Ce travail présente les travaux pratiques qui sont au nombre de cinq (05 TP) et qui s'adressent aux étudiants de 1ere année Licence LMD (Tronc commun).
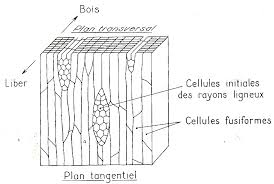 TP 2 cormophytes
TP 2 cormophytes
Filière SVT- S2 – Élément 2: Biologie végétale. Université Mohammed V- Agdal. Faculté des Sciences - Rabat. Département de Biologie. Pr. Hikmat TAHIRI. Les
 BIOLOGIE VEGETALE (S2)
BIOLOGIE VEGETALE (S2)
Parmi ces tissus on compte l'épiderme le suber (liège) . A- Epiderme. En botanique
 BIOLOGIE VEGETALE
BIOLOGIE VEGETALE
- TP 1 : La cellule végétale vue au microscope photonique. - TP 2 : La cellule végétale - Travaux pratiques : Chaque TP donne lieu à un compte rendu corrigé.
 L1 Chimie-Biologie accompagné
L1 Chimie-Biologie accompagné
28 sept. 2023 Pour la Biologie végétale 1: Le contrôle continu pratique (30%) comprend des notes de compte-rendu manipulations
 Objectifs de lenseignement ............................................... : .......
Objectifs de lenseignement ............................................... : .......
✓ La première page (voir le modèle du compte rendu sur la page 7) : L'étude des tissus en Biologie Végétale se base sur la paroi pecto-cellulosique.
 DESCRIPTIF DE MODULE - Biologie Végétale
DESCRIPTIF DE MODULE - Biologie Végétale
Comptes rendus et Travaux Pratiques (NTP). 3.2. Note du module. (Préciser les coefficients de pondération attribués aux différentes évaluations et composantes ...
 TP N° 2 : observation microscopique des cellules végétales
TP N° 2 : observation microscopique des cellules végétales
TP N 02 de biologie générale ; La cellule végétale. Département de géologie. Mme: ADJROUD.S. 1. TP N° 2 : observation microscopique des cellules végétales.
 TB SVT TP 4.2. - Mycètes / Champignons - T. JEAN - SVT - Biologie
TB SVT TP 4.2. - Mycètes / Champignons - T. JEAN - SVT - Biologie
Il est donc abusif de compter les noyaux d'une cellule. Que dire des Biologie végétale. Associations et interactions chez les plantes. Dunod ...
 Travaux pratiques et travaux dirigés de biologie végétale
Travaux pratiques et travaux dirigés de biologie végétale
1 – Arriver à l'heure pour ne pas perturber le déroulement de la séance ;. 2 – Porter une blouse blanche propre ;. 3 – Préparer la séance de TP : lire
 Polycopié Travaux pratiques Biologie végétale 1 année LMD
Polycopié Travaux pratiques Biologie végétale 1 année LMD
Département de Biologie et Ecologie Végétale. 1. Enseignante : Le troisième TP est consacré pour l'étude des tissus végétaux.
 BIOLOGIE VEGETALE (S2)
BIOLOGIE VEGETALE (S2)
Observation et dessin des différents tissus végétaux (utilisation de lames la paroi externe est épaissie et rendue imperméable par un dépôt de cires et.
 TP N°1 : Gamétogenèse
TP N°1 : Gamétogenèse
? Etude histologique du testicule et de l'ovaire. MENAD R. Faculté des Sciences. Année universitaire: 2016/2017. TP-Biologie Animale-Alger1
 Master – Biologie Animale
Master – Biologie Animale
Le Master en Biologie animale combine des séances de cours de travaux dirigés et de travaux Préparation des comptes rendus des TP effectuées.
 TP N°01 : ETUDE MORPHOLOGIQUE DES ANGIOSPERMES
TP N°01 : ETUDE MORPHOLOGIQUE DES ANGIOSPERMES
1RE ANNEE L.M.D S.N.V (FORESTERIE). BIOLOGIE VEGETALE. Dr BARKA FATIHA. Année universitaire 2019/2020. TP N°01 : ETUDE MORPHOLOGIQUE DES ANGIOSPERMES.
 Travaux pratiques de physiologie végétale
Travaux pratiques de physiologie végétale
Tp physiologie végétale. 1. TP ? 01. Analyse du sol. Introduction si l'on tient compte de l'eau présente dans les feuilles) et broyer jusqu'à obtenir un.
 Diapositive 1
Diapositive 1
Observation microscopique de quelques tissus épithéliaux. Proposé par : • Benbaibeche H. • Maouche N. • Menad R. TP-Biologie Animale-Alger1
 Travaux Pratiques
Travaux Pratiques
pas accepté dans la salle de TP. Rédaction du Compte rendu CIV ... laboratoires de biologie végétale pour la culture de cellules de tissus et de ...
 Comment rédiger un compte rendu de Travaux Pratiques - Collège
Comment rédiger un compte rendu de Travaux Pratiques - Collège
N°3 : hypothèse(s) retenue(s). Ecrire le plus clairement possible vos idées permettant de répondre à l'objectif du TP.
 Travaux pratiques et travaux dirigés de biologie vegetale
Travaux pratiques et travaux dirigés de biologie vegetale
ensemble de travaux pratiques et de travaux dirigés de biologie végétale Il est destiné aux étudiants de tronc commun sciences de la nature et de la vie des sciences de la terre et de l’univers de l’agronomie et de foresterie
 Searches related to compte rendu tp biologie végétale
Searches related to compte rendu tp biologie végétale
Tp physiologie végétale 1 TP ? 01 Analyse du sol Introduction Les analyses physicochimiques du sol permettent aux agriculteurs d’évaluer les niveaux de fertilisations des sols et de l’adapter aux programmes de fertilisation complémentaire en fonction des besoins des sols et des cultures
Université Frère Mentouri Constantine 1
Institut de la Nutrition, Alimentation et des Technologies Agro-Alimentaires INATAA-Filière : sciences alimentaires
Département : technologie alimentaire
Promotion : 2ème année Licence
Enseignants : KEHAL F. (MAA)
BENAMARA M. (MCB)
BOUGUERRA A. (MAA)
ZERIZER H. (MCA)
Année universitaire : 2019 /2020
Travaux pratiques de physiologie végétale
Tp physiologie végétale
1TP ʋ1. Analyse du sol
Introduction
Les analyses physicochimiques du sol permettent aux agriculteurs fertilisations des sols et de laux programmes de fertilisation complémentaire en fonction des besoins demeilleur rendement au niveau de la productivité, maitriser les coûts de production et de
Préparation du sol
Séchage : pour obtenir un sol uniforme
Broyage : pour augmenter la surface de contacter entre le sol et les réactifsExpérience 01. Dosage du calcaire dans le sol
Le calcaire total correspond à la quantité de Carbonate de calcium (CaCO3) - Peser 1g de sol et verser dessus une solution de HCl (1N) ; après effervescence ajouter une et verser sur le filtre. constant. - Mesurer le pou : % de calcaire = (Pi - Pf)/Pi*100 ou : Pi : poids initial du sol ; Pf : poids final du sol. - La formule de la réaction est la suivante :CaCO3 + 2 HCl =========Î CaCl2 + H2O + CO2
Carbonate de Calcium + Acide chlorhydrique ==Î Chlorure de Calcium Expérience 02. Dosage de la matière organique dans le sol - 2O2 concentré, et remuer (le H2O2 concentré détruit la matière organique ; les produits sont dégradés en CO2, H2O et NO2 et parfoisSO2) ;
- Filtrer ; % de MO = (Pi - Pf)/Pi*100Pi : poids initial ;
Pf : poids final.
- Les sols sont répartis en trois classes :Tp physiologie végétale
2 AE Teneur faible < 4% ; Teneur modérée 4-9% ; Teneur élevée 9-30%Expérience 03. Technique de sédimentation
La méthode de sédimentation consiste à séparer les constituants du sol en fonction de leurs
poids selon la loi de stockes.1. Fraction grossière > 2 mm ;
2. Sable grossier : 2 à 0.2 mm ;
3. Sable fin : 02 à 0.04 mm ;
4. Limon : 0.04 à 0.002 mm;
5. Argile < 0.002 mm.
Selon les résultats obtenus, les sols se classent en différentes catégories :9 Sableux
9 Limoneux
9 Argileux
Expérience 04. Mesure du pH
2/3), agiter la solution
pendant une minute. Procéder à la lecture du pH. On classe les sols selon leur acidité de la manière suivante : pH <4.5 : sols très acides4.5 6 pH> 7 : sols calcaire (basique) Tp physiologie végétale
3 ʋ02. Détermination de la pression osmotique par la méthode de la plasmolyse- limite Introduction
L'osmose est un phénomène de diffusion de la matière mis en évidence lorsque des molécules
d'eau (de solvant de façon générale) traversent une membrane semi-perméable qui sépare
deux liquides dont les concentrations en produits dissous sont différentes. La différence de concentration provoque une différence de pression osmotique qui engendre un déplacement du solvant à travers la membrane. 1. Matériels et réactifs
- Bulbe d'oignon ; - Onze (11) verres de montre ; - Solution de saccharose M (1 mol.L-1) (soit 342 g/L ou 34,2%) ; - Eau distillée ; - 2 pipettes de 5 ml; - Lame-lamelles ; - Microscope optique ; - pinces fines et rasoir. 2. Méthodes
2.1 Principe
de solutions de concentration croissante, celle qui en équilibre osmotique avec les cellules. produit un faible début de plasmolyse (plasmolyse limite) est pratiquement isotonique du
milieu cellulaire. 2.2 Protocole
- Préparer une série de 11 tubes contenant des concentrations croissantes de saccharose ; - Mettre quelques millilitres de chaque solution dans 11 verres de montre posés sur une feuille de papier, sur laquelle on indiquera les concentrations correspondantes ; - Prélever d ; - Placer les morceaux d'épiderme dans les verres de montre ; Tp physiologie végétale
4 - Attendre 15 à 30 min et observer. Tableau 01.
ʋ 1 2 3 4 5 6 7 8 9 10 11
V3 de la solution de sacc.(mL) 0 0.5 1 1.5 2 2.5 3 3.5 4 4.5 5 5 4.5 4 3.5 3 2.5 2 1.5 1 0.5 0
Concentration molaire (mol.L-1) 0 0,1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1 3. Interprétation des résultats
- Les cellules sont turgescentes pour les faibles concentrations de milieu et plasmolysées pour les fortes concentrations ; - Il existe une concentration pour laquelle on observe une très légère plasmolyse (plasmolyse limite) ; - par ce mouvement (pression osmotique) est équilibrée par la pression de réaction de la paroi (pression de paroi ou pression de turgescence). - Calculer la pression osmotique du suc vacuolaire en fonction des résultats observés, Exemple :
- Si la dernière préparation turgescente correspond au verre de montre n°4 (concentration molaire en saccharose : 0.3) et la première préparation plasmolysée correspond au n°5 (concentration molaire en saccharose : 0.4) on peut écrire que la concentration molaire de la solution isotonique au suc vasculaire et par conséquent la concentration molaire m du suc vacuolaire est compris entre 03 - La pression osmotique du suc vacuolaire est donc comprise entre les valeurs : 22.4*0.3 Tp physiologie végétale
5 ʋ.Extraction et séparation des différents pigments photosynthétiques Introduction
Les organismes chlorophylliens sont capables de synthétiser des molécules organiques source d'énergie s'appelle la photosynthèse. L'utilisation de l'énergie lumineuse est rendue
d'onde lorsqu'elles sont éclairées par de la lumière blanche. Cette propriété leur donne une
couleur déterminée. Les chlorophylles sont les pigments majeurs impliqués dans la capture des photons. La chlorophylle est synthétisée et dégradée dans l'enveloppe du chloroplaste, mais elle n'est
présente et active comme pigment que dans les thylacoïdes. Les caroténoïdes accompagnent toujours les chlorophylles dans les membranes thylacoïdales où ils jouent apparemment le double rôle de pigments accessoires pour la capture de l'énergie
lumineuse et de photoprotecteurs contre les intensités lumineuses élevées. On les trouve
également associés à l'enveloppe du chloroplaste. Ils sont aussi très répandus dans de
nombreux tissus végétaux (parenchyme de Tomate, racines de Carottes, pétales, écorce
d'Orange,etc...). 1. Matériels et réactifs
Un mortier et pilon ;
sable de mer ; une éprouvette (25, 50, 100mL); un papier filtre ; un bécher (10 et 50 mL) ; erlenmeyer (10 et 50 mL) ; un entonnoir, une pipette Pasteur ; Ether de pétrole ;
Acétone ;
Dichloroéthane ;
un agitateur magnétique, une tige et un barreau (aimant) ; une bande de papier chromatographie de 2 cm de large ; papier aluminium. Tp physiologie végétale
6 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. 1) épinard ;
2) Couper le matériel végétal en petits fragments ;
3) pour obtenir un mélange acétone/eau de concentration final 80%
) et broyer jusqu'à obtenir un mélange homogène ; 4) Ajout
5) Laisser décanter quelques minutes (10min) ;
6) Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et
recueillir la solution acétonique de chlorophylles) et compléter 80% ;
7) Fermer avec du parafilm et agiter.
Remarque :
éventuellement en tamponnant le milieu avec la craie (CaCO3) ; - Ajouter de Chlorure de Calcium (CaCl2 perméabilisant la membrane chloroplastique. 2. Séparation des différents pigments photosynthétiques par chromatographie sur
papier apolaire -à--à-dire 1) Introduire dans le tube de chromatographie 10mL de solvant de migration (éther de
pétrole/acétone/dichloroéthane : 8.5/1/0.5 v/v/v) - éluant - () ; 2) Fermer hermétiquement le tube ;
3) chromatographie (afin que le dépôt ne soit pas en contact avec le solvant) ; 4) Déposer
dilué sur le trait et sécher ( Tp physiologie végétale
7 5) Introduire le chromatogramme dans le tube entouré de papier noir puis fermer le tube ;
6) Arrêter la migration quand le front du solvant aura atteint 20cm.
7) Sécher la chromatographie
2.3 Analyse des résultats
Dessiner le chromatogramme, identifier les pigments en vous aidant des formules, justifier leurs ordres de migration. a) ȕ-Carotène(C40H56) : de couleur orangé; b) Chlorophyllea (C55H72O5N4Mg): de couleur vert bleuté; c) Chlorophylleb (C55H70O6N4Mg): de couleur vert jaune; d) Xanthophylle(C40H56O2) : de couleur jaune. Tp physiologie végétale
8 Introduction
La photosynthèse est un mécanisme biochimique permettant aux végétaux supérieurs 2. siège dans des organites propres à la cellule chlorophyllienne: les chloroplastes. De
nombreuses protéines et autres molécules contribuent au mécanisme, parmi eux les pigments photosynthétiques : Chlorophylle a et b ainsi que les caroténoïdes. Ce sont les molécules
Le but de cette expérience est de quantifier par une méthode spectrophotométrique les 1. Matériels et réactifs
Spectrophotomètre ;
Deux (02) mortiers et pilons ;
Une éprouvette (25, 50, 100mL);
Un papier filtre ;
Trois (03) béchers (25 et 50 mL) ;
Deux (02) erlenmeyers (25 et 50 mL) ;
Deux (02) petits entonnoirs ;
Dix (10) pipettes Pasteur ;
Cinq (05) pipettes (1, 5 et 10ml) ;
Une poire ;
Cétone (250ml) ;
Un agitateur magnétique, une tige et un barreau (aimant) ; 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. Couper le matériel végétal en petits fragments ; pour obtenir un mélange acétone/eau de concentration final ) et broyer jusqu'à obtenir un mélange homogène ; Tp physiologie végétale
9 yer de nouveau soigneusement ; Laisser décanter quelques minutes (10min) ;
Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et recueillir la solution acétonique de chlorophylles) et compléter à 10mL avec de 80% ;
Fermer avec du parafilm et agiter.
3. Dosage des pigments totaux
3.1 Rappel
La lumière blanche est composée de différentes radiations visibles dont la longueur -800 nm (rouge foncé). Une substance colorée absorbe préférentiellement certaines radiations de la lumière blanche. Cette propriété lui donne sa
couleur. Si cette substance est un photorécepteur, les radiations absorbées peuvent être celles
qui agissent sur lui et entraînent une photo-réaction. 3.2 Protocole
- Fermer la fiole avec du parafilm et agiter ; - recommencer les opérations successivement à 6 pour chaque longueu 3.3 Interprétations des résultats
-dessous établies à partir de loi de BEER-LAMBERT permettent de calculer les concentrations en pigments : Ca = 12.7 A663 2.63 A645
Cb = 22.9 A645 4.68 A663 en mg.L-1
Ccar = 5 A460 (3.19Ca + 130.3 Cb)/200
Tp physiologie végétale
10 TP ʋ5. Germination des graines
Introduction
La germination est une phase physiologique qui correspond à la transition de la phase de vie latente de la graine sèche à la phase de développement de la plantule. Le processus de
germination commence dès que la graine sèche est hydratée. perméabilité des tégu du métabolisme, qui préparent le déclenchement de la croissance. Au cours de la période de
débutquotesdbs_dbs20.pdfusesText_26
6 pH> 7 : sols calcaire (basique) Tp physiologie végétale
3 ʋ02. Détermination de la pression osmotique par la méthode de la plasmolyse- limite Introduction
L'osmose est un phénomène de diffusion de la matière mis en évidence lorsque des molécules
d'eau (de solvant de façon générale) traversent une membrane semi-perméable qui sépare
deux liquides dont les concentrations en produits dissous sont différentes. La différence de concentration provoque une différence de pression osmotique qui engendre un déplacement du solvant à travers la membrane. 1. Matériels et réactifs
- Bulbe d'oignon ; - Onze (11) verres de montre ; - Solution de saccharose M (1 mol.L-1) (soit 342 g/L ou 34,2%) ; - Eau distillée ; - 2 pipettes de 5 ml; - Lame-lamelles ; - Microscope optique ; - pinces fines et rasoir. 2. Méthodes
2.1 Principe
de solutions de concentration croissante, celle qui en équilibre osmotique avec les cellules. produit un faible début de plasmolyse (plasmolyse limite) est pratiquement isotonique du
milieu cellulaire. 2.2 Protocole
- Préparer une série de 11 tubes contenant des concentrations croissantes de saccharose ; - Mettre quelques millilitres de chaque solution dans 11 verres de montre posés sur une feuille de papier, sur laquelle on indiquera les concentrations correspondantes ; - Prélever d ; - Placer les morceaux d'épiderme dans les verres de montre ; Tp physiologie végétale
4 - Attendre 15 à 30 min et observer. Tableau 01.
ʋ 1 2 3 4 5 6 7 8 9 10 11
V3 de la solution de sacc.(mL) 0 0.5 1 1.5 2 2.5 3 3.5 4 4.5 5 5 4.5 4 3.5 3 2.5 2 1.5 1 0.5 0
Concentration molaire (mol.L-1) 0 0,1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1 3. Interprétation des résultats
- Les cellules sont turgescentes pour les faibles concentrations de milieu et plasmolysées pour les fortes concentrations ; - Il existe une concentration pour laquelle on observe une très légère plasmolyse (plasmolyse limite) ; - par ce mouvement (pression osmotique) est équilibrée par la pression de réaction de la paroi (pression de paroi ou pression de turgescence). - Calculer la pression osmotique du suc vacuolaire en fonction des résultats observés, Exemple :
- Si la dernière préparation turgescente correspond au verre de montre n°4 (concentration molaire en saccharose : 0.3) et la première préparation plasmolysée correspond au n°5 (concentration molaire en saccharose : 0.4) on peut écrire que la concentration molaire de la solution isotonique au suc vasculaire et par conséquent la concentration molaire m du suc vacuolaire est compris entre 03 - La pression osmotique du suc vacuolaire est donc comprise entre les valeurs : 22.4*0.3 Tp physiologie végétale
5 ʋ.Extraction et séparation des différents pigments photosynthétiques Introduction
Les organismes chlorophylliens sont capables de synthétiser des molécules organiques source d'énergie s'appelle la photosynthèse. L'utilisation de l'énergie lumineuse est rendue
d'onde lorsqu'elles sont éclairées par de la lumière blanche. Cette propriété leur donne une
couleur déterminée. Les chlorophylles sont les pigments majeurs impliqués dans la capture des photons. La chlorophylle est synthétisée et dégradée dans l'enveloppe du chloroplaste, mais elle n'est
présente et active comme pigment que dans les thylacoïdes. Les caroténoïdes accompagnent toujours les chlorophylles dans les membranes thylacoïdales où ils jouent apparemment le double rôle de pigments accessoires pour la capture de l'énergie
lumineuse et de photoprotecteurs contre les intensités lumineuses élevées. On les trouve
également associés à l'enveloppe du chloroplaste. Ils sont aussi très répandus dans de
nombreux tissus végétaux (parenchyme de Tomate, racines de Carottes, pétales, écorce
d'Orange,etc...). 1. Matériels et réactifs
Un mortier et pilon ;
sable de mer ; une éprouvette (25, 50, 100mL); un papier filtre ; un bécher (10 et 50 mL) ; erlenmeyer (10 et 50 mL) ; un entonnoir, une pipette Pasteur ; Ether de pétrole ;
Acétone ;
Dichloroéthane ;
un agitateur magnétique, une tige et un barreau (aimant) ; une bande de papier chromatographie de 2 cm de large ; papier aluminium. Tp physiologie végétale
6 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. 1) épinard ;
2) Couper le matériel végétal en petits fragments ;
3) pour obtenir un mélange acétone/eau de concentration final 80%
) et broyer jusqu'à obtenir un mélange homogène ; 4) Ajout
5) Laisser décanter quelques minutes (10min) ;
6) Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et
recueillir la solution acétonique de chlorophylles) et compléter 80% ;
7) Fermer avec du parafilm et agiter.
Remarque :
éventuellement en tamponnant le milieu avec la craie (CaCO3) ; - Ajouter de Chlorure de Calcium (CaCl2 perméabilisant la membrane chloroplastique. 2. Séparation des différents pigments photosynthétiques par chromatographie sur
papier apolaire -à--à-dire 1) Introduire dans le tube de chromatographie 10mL de solvant de migration (éther de
pétrole/acétone/dichloroéthane : 8.5/1/0.5 v/v/v) - éluant - () ; 2) Fermer hermétiquement le tube ;
3) chromatographie (afin que le dépôt ne soit pas en contact avec le solvant) ; 4) Déposer
dilué sur le trait et sécher ( Tp physiologie végétale
7 5) Introduire le chromatogramme dans le tube entouré de papier noir puis fermer le tube ;
6) Arrêter la migration quand le front du solvant aura atteint 20cm.
7) Sécher la chromatographie
2.3 Analyse des résultats
Dessiner le chromatogramme, identifier les pigments en vous aidant des formules, justifier leurs ordres de migration. a) ȕ-Carotène(C40H56) : de couleur orangé; b) Chlorophyllea (C55H72O5N4Mg): de couleur vert bleuté; c) Chlorophylleb (C55H70O6N4Mg): de couleur vert jaune; d) Xanthophylle(C40H56O2) : de couleur jaune. Tp physiologie végétale
8 Introduction
La photosynthèse est un mécanisme biochimique permettant aux végétaux supérieurs 2. siège dans des organites propres à la cellule chlorophyllienne: les chloroplastes. De
nombreuses protéines et autres molécules contribuent au mécanisme, parmi eux les pigments photosynthétiques : Chlorophylle a et b ainsi que les caroténoïdes. Ce sont les molécules
Le but de cette expérience est de quantifier par une méthode spectrophotométrique les 1. Matériels et réactifs
Spectrophotomètre ;
Deux (02) mortiers et pilons ;
Une éprouvette (25, 50, 100mL);
Un papier filtre ;
Trois (03) béchers (25 et 50 mL) ;
Deux (02) erlenmeyers (25 et 50 mL) ;
Deux (02) petits entonnoirs ;
Dix (10) pipettes Pasteur ;
Cinq (05) pipettes (1, 5 et 10ml) ;
Une poire ;
Cétone (250ml) ;
Un agitateur magnétique, une tige et un barreau (aimant) ; 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. Couper le matériel végétal en petits fragments ; pour obtenir un mélange acétone/eau de concentration final ) et broyer jusqu'à obtenir un mélange homogène ; Tp physiologie végétale
9 yer de nouveau soigneusement ; Laisser décanter quelques minutes (10min) ;
Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et recueillir la solution acétonique de chlorophylles) et compléter à 10mL avec de 80% ;
Fermer avec du parafilm et agiter.
3. Dosage des pigments totaux
3.1 Rappel
La lumière blanche est composée de différentes radiations visibles dont la longueur -800 nm (rouge foncé). Une substance colorée absorbe préférentiellement certaines radiations de la lumière blanche. Cette propriété lui donne sa
couleur. Si cette substance est un photorécepteur, les radiations absorbées peuvent être celles
qui agissent sur lui et entraînent une photo-réaction. 3.2 Protocole
- Fermer la fiole avec du parafilm et agiter ; - recommencer les opérations successivement à 6 pour chaque longueu 3.3 Interprétations des résultats
-dessous établies à partir de loi de BEER-LAMBERT permettent de calculer les concentrations en pigments : Ca = 12.7 A663 2.63 A645
Cb = 22.9 A645 4.68 A663 en mg.L-1
Ccar = 5 A460 (3.19Ca + 130.3 Cb)/200
Tp physiologie végétale
10 TP ʋ5. Germination des graines
Introduction
La germination est une phase physiologique qui correspond à la transition de la phase de vie latente de la graine sèche à la phase de développement de la plantule. Le processus de
germination commence dès que la graine sèche est hydratée. perméabilité des tégu du métabolisme, qui préparent le déclenchement de la croissance. Au cours de la période de
débutquotesdbs_dbs20.pdfusesText_26
Tp physiologie végétale
3 ʋ02. Détermination de la pression osmotique par la méthode de la plasmolyse- limiteIntroduction
L'osmose est un phénomène de diffusion de la matière mis en évidence lorsque des molécules
d'eau (de solvant de façon générale) traversent une membrane semi-perméable qui sépare
deux liquides dont les concentrations en produits dissous sont différentes. La différence de concentration provoque une différence de pression osmotique qui engendre un déplacement du solvant à travers la membrane.1. Matériels et réactifs
- Bulbe d'oignon ; - Onze (11) verres de montre ; - Solution de saccharose M (1 mol.L-1) (soit 342 g/L ou 34,2%) ; - Eau distillée ; - 2 pipettes de 5 ml; - Lame-lamelles ; - Microscope optique ; - pinces fines et rasoir.2. Méthodes
2.1 Principe
de solutions de concentration croissante, celle qui en équilibre osmotique avec les cellules.produit un faible début de plasmolyse (plasmolyse limite) est pratiquement isotonique du
milieu cellulaire.2.2 Protocole
- Préparer une série de 11 tubes contenant des concentrations croissantes de saccharose ; - Mettre quelques millilitres de chaque solution dans 11 verres de montre posés sur une feuille de papier, sur laquelle on indiquera les concentrations correspondantes ; - Prélever d ; - Placer les morceaux d'épiderme dans les verres de montre ;Tp physiologie végétale
4 - Attendre 15 à 30 min et observer.Tableau 01.
ʋ 1 2 3 4 5 6 7 8 9 10 11
V3 de la solution de sacc.(mL) 0 0.5 1 1.5 2 2.5 3 3.5 4 4.5 55 4.5 4 3.5 3 2.5 2 1.5 1 0.5 0
Concentration molaire (mol.L-1) 0 0,1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 13. Interprétation des résultats
- Les cellules sont turgescentes pour les faibles concentrations de milieu et plasmolysées pour les fortes concentrations ; - Il existe une concentration pour laquelle on observe une très légère plasmolyse (plasmolyse limite) ; - par ce mouvement (pression osmotique) est équilibrée par la pression de réaction de la paroi (pression de paroi ou pression de turgescence). - Calculer la pression osmotique du suc vacuolaire en fonction des résultats observés,Exemple :
- Si la dernière préparation turgescente correspond au verre de montre n°4 (concentration molaire en saccharose : 0.3) et la première préparation plasmolysée correspond au n°5 (concentration molaire en saccharose : 0.4) on peut écrire que la concentration molaire de la solution isotonique au suc vasculaire et par conséquent la concentration molaire m du suc vacuolaire est compris entre03 - La pression osmotique du suc vacuolaire est donc comprise entre les valeurs : 22.4*0.3 Tp physiologie végétale
5 ʋ.Extraction et séparation des différents pigments photosynthétiques Introduction
Les organismes chlorophylliens sont capables de synthétiser des molécules organiques source d'énergie s'appelle la photosynthèse. L'utilisation de l'énergie lumineuse est rendue
d'onde lorsqu'elles sont éclairées par de la lumière blanche. Cette propriété leur donne une
couleur déterminée. Les chlorophylles sont les pigments majeurs impliqués dans la capture des photons. La chlorophylle est synthétisée et dégradée dans l'enveloppe du chloroplaste, mais elle n'est
présente et active comme pigment que dans les thylacoïdes. Les caroténoïdes accompagnent toujours les chlorophylles dans les membranes thylacoïdales où ils jouent apparemment le double rôle de pigments accessoires pour la capture de l'énergie
lumineuse et de photoprotecteurs contre les intensités lumineuses élevées. On les trouve
également associés à l'enveloppe du chloroplaste. Ils sont aussi très répandus dans de
nombreux tissus végétaux (parenchyme de Tomate, racines de Carottes, pétales, écorce
d'Orange,etc...). 1. Matériels et réactifs
Un mortier et pilon ;
sable de mer ; une éprouvette (25, 50, 100mL); un papier filtre ; un bécher (10 et 50 mL) ; erlenmeyer (10 et 50 mL) ; un entonnoir, une pipette Pasteur ; Ether de pétrole ;
Acétone ;
Dichloroéthane ;
un agitateur magnétique, une tige et un barreau (aimant) ; une bande de papier chromatographie de 2 cm de large ; papier aluminium. Tp physiologie végétale
6 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. 1) épinard ;
2) Couper le matériel végétal en petits fragments ;
3) pour obtenir un mélange acétone/eau de concentration final 80%
) et broyer jusqu'à obtenir un mélange homogène ; 4) Ajout
5) Laisser décanter quelques minutes (10min) ;
6) Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et
recueillir la solution acétonique de chlorophylles) et compléter 80% ;
7) Fermer avec du parafilm et agiter.
Remarque :
éventuellement en tamponnant le milieu avec la craie (CaCO3) ; - Ajouter de Chlorure de Calcium (CaCl2 perméabilisant la membrane chloroplastique. 2. Séparation des différents pigments photosynthétiques par chromatographie sur
papier apolaire -à--à-dire 1) Introduire dans le tube de chromatographie 10mL de solvant de migration (éther de
pétrole/acétone/dichloroéthane : 8.5/1/0.5 v/v/v) - éluant - () ; 2) Fermer hermétiquement le tube ;
3) chromatographie (afin que le dépôt ne soit pas en contact avec le solvant) ; 4) Déposer
dilué sur le trait et sécher ( Tp physiologie végétale
7 5) Introduire le chromatogramme dans le tube entouré de papier noir puis fermer le tube ;
6) Arrêter la migration quand le front du solvant aura atteint 20cm.
7) Sécher la chromatographie
2.3 Analyse des résultats
Dessiner le chromatogramme, identifier les pigments en vous aidant des formules, justifier leurs ordres de migration. a) ȕ-Carotène(C40H56) : de couleur orangé; b) Chlorophyllea (C55H72O5N4Mg): de couleur vert bleuté; c) Chlorophylleb (C55H70O6N4Mg): de couleur vert jaune; d) Xanthophylle(C40H56O2) : de couleur jaune. Tp physiologie végétale
8 Introduction
La photosynthèse est un mécanisme biochimique permettant aux végétaux supérieurs 2. siège dans des organites propres à la cellule chlorophyllienne: les chloroplastes. De
nombreuses protéines et autres molécules contribuent au mécanisme, parmi eux les pigments photosynthétiques : Chlorophylle a et b ainsi que les caroténoïdes. Ce sont les molécules
Le but de cette expérience est de quantifier par une méthode spectrophotométrique les 1. Matériels et réactifs
Spectrophotomètre ;
Deux (02) mortiers et pilons ;
Une éprouvette (25, 50, 100mL);
Un papier filtre ;
Trois (03) béchers (25 et 50 mL) ;
Deux (02) erlenmeyers (25 et 50 mL) ;
Deux (02) petits entonnoirs ;
Dix (10) pipettes Pasteur ;
Cinq (05) pipettes (1, 5 et 10ml) ;
Une poire ;
Cétone (250ml) ;
Un agitateur magnétique, une tige et un barreau (aimant) ; 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. Couper le matériel végétal en petits fragments ; pour obtenir un mélange acétone/eau de concentration final ) et broyer jusqu'à obtenir un mélange homogène ; Tp physiologie végétale
9 yer de nouveau soigneusement ; Laisser décanter quelques minutes (10min) ;
Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et recueillir la solution acétonique de chlorophylles) et compléter à 10mL avec de 80% ;
Fermer avec du parafilm et agiter.
3. Dosage des pigments totaux
3.1 Rappel
La lumière blanche est composée de différentes radiations visibles dont la longueur -800 nm (rouge foncé). Une substance colorée absorbe préférentiellement certaines radiations de la lumière blanche. Cette propriété lui donne sa
couleur. Si cette substance est un photorécepteur, les radiations absorbées peuvent être celles
qui agissent sur lui et entraînent une photo-réaction. 3.2 Protocole
- Fermer la fiole avec du parafilm et agiter ; - recommencer les opérations successivement à 6 pour chaque longueu 3.3 Interprétations des résultats
-dessous établies à partir de loi de BEER-LAMBERT permettent de calculer les concentrations en pigments : Ca = 12.7 A663 2.63 A645
Cb = 22.9 A645 4.68 A663 en mg.L-1
Ccar = 5 A460 (3.19Ca + 130.3 Cb)/200
Tp physiologie végétale
10 TP ʋ5. Germination des graines
Introduction
La germination est une phase physiologique qui correspond à la transition de la phase de vie latente de la graine sèche à la phase de développement de la plantule. Le processus de
germination commence dès que la graine sèche est hydratée. perméabilité des tégu du métabolisme, qui préparent le déclenchement de la croissance. Au cours de la période de
débutquotesdbs_dbs20.pdfusesText_26
22.4*0.3 Tp physiologie végétale
5 ʋ.Extraction et séparation des différents pigments photosynthétiques Introduction
Les organismes chlorophylliens sont capables de synthétiser des molécules organiques source d'énergie s'appelle la photosynthèse. L'utilisation de l'énergie lumineuse est rendue
d'onde lorsqu'elles sont éclairées par de la lumière blanche. Cette propriété leur donne une
couleur déterminée. Les chlorophylles sont les pigments majeurs impliqués dans la capture des photons. La chlorophylle est synthétisée et dégradée dans l'enveloppe du chloroplaste, mais elle n'est
présente et active comme pigment que dans les thylacoïdes. Les caroténoïdes accompagnent toujours les chlorophylles dans les membranes thylacoïdales où ils jouent apparemment le double rôle de pigments accessoires pour la capture de l'énergie
lumineuse et de photoprotecteurs contre les intensités lumineuses élevées. On les trouve
également associés à l'enveloppe du chloroplaste. Ils sont aussi très répandus dans de
nombreux tissus végétaux (parenchyme de Tomate, racines de Carottes, pétales, écorce
d'Orange,etc...). 1. Matériels et réactifs
Un mortier et pilon ;
sable de mer ; une éprouvette (25, 50, 100mL); un papier filtre ; un bécher (10 et 50 mL) ; erlenmeyer (10 et 50 mL) ; un entonnoir, une pipette Pasteur ; Ether de pétrole ;
Acétone ;
Dichloroéthane ;
un agitateur magnétique, une tige et un barreau (aimant) ; une bande de papier chromatographie de 2 cm de large ; papier aluminium. Tp physiologie végétale
6 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. 1) épinard ;
2) Couper le matériel végétal en petits fragments ;
3) pour obtenir un mélange acétone/eau de concentration final 80%
) et broyer jusqu'à obtenir un mélange homogène ; 4) Ajout
5) Laisser décanter quelques minutes (10min) ;
6) Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et
recueillir la solution acétonique de chlorophylles) et compléter 80% ;
7) Fermer avec du parafilm et agiter.
Remarque :
éventuellement en tamponnant le milieu avec la craie (CaCO3) ; - Ajouter de Chlorure de Calcium (CaCl2 perméabilisant la membrane chloroplastique. 2. Séparation des différents pigments photosynthétiques par chromatographie sur
papier apolaire -à--à-dire 1) Introduire dans le tube de chromatographie 10mL de solvant de migration (éther de
pétrole/acétone/dichloroéthane : 8.5/1/0.5 v/v/v) - éluant - () ; 2) Fermer hermétiquement le tube ;
3) chromatographie (afin que le dépôt ne soit pas en contact avec le solvant) ; 4) Déposer
dilué sur le trait et sécher ( Tp physiologie végétale
7 5) Introduire le chromatogramme dans le tube entouré de papier noir puis fermer le tube ;
6) Arrêter la migration quand le front du solvant aura atteint 20cm.
7) Sécher la chromatographie
2.3 Analyse des résultats
Dessiner le chromatogramme, identifier les pigments en vous aidant des formules, justifier leurs ordres de migration. a) ȕ-Carotène(C40H56) : de couleur orangé; b) Chlorophyllea (C55H72O5N4Mg): de couleur vert bleuté; c) Chlorophylleb (C55H70O6N4Mg): de couleur vert jaune; d) Xanthophylle(C40H56O2) : de couleur jaune. Tp physiologie végétale
8 Introduction
La photosynthèse est un mécanisme biochimique permettant aux végétaux supérieurs 2. siège dans des organites propres à la cellule chlorophyllienne: les chloroplastes. De
nombreuses protéines et autres molécules contribuent au mécanisme, parmi eux les pigments photosynthétiques : Chlorophylle a et b ainsi que les caroténoïdes. Ce sont les molécules
Le but de cette expérience est de quantifier par une méthode spectrophotométrique les 1. Matériels et réactifs
Spectrophotomètre ;
Deux (02) mortiers et pilons ;
Une éprouvette (25, 50, 100mL);
Un papier filtre ;
Trois (03) béchers (25 et 50 mL) ;
Deux (02) erlenmeyers (25 et 50 mL) ;
Deux (02) petits entonnoirs ;
Dix (10) pipettes Pasteur ;
Cinq (05) pipettes (1, 5 et 10ml) ;
Une poire ;
Cétone (250ml) ;
Un agitateur magnétique, une tige et un barreau (aimant) ; 2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. Couper le matériel végétal en petits fragments ; pour obtenir un mélange acétone/eau de concentration final ) et broyer jusqu'à obtenir un mélange homogène ; Tp physiologie végétale
9 yer de nouveau soigneusement ; Laisser décanter quelques minutes (10min) ;
Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et recueillir la solution acétonique de chlorophylles) et compléter à 10mL avec de 80% ;
Fermer avec du parafilm et agiter.
3. Dosage des pigments totaux
3.1 Rappel
La lumière blanche est composée de différentes radiations visibles dont la longueur -800 nm (rouge foncé). Une substance colorée absorbe préférentiellement certaines radiations de la lumière blanche. Cette propriété lui donne sa
couleur. Si cette substance est un photorécepteur, les radiations absorbées peuvent être celles
qui agissent sur lui et entraînent une photo-réaction. 3.2 Protocole
- Fermer la fiole avec du parafilm et agiter ; - recommencer les opérations successivement à 6 pour chaque longueu 3.3 Interprétations des résultats
-dessous établies à partir de loi de BEER-LAMBERT permettent de calculer les concentrations en pigments : Ca = 12.7 A663 2.63 A645
Cb = 22.9 A645 4.68 A663 en mg.L-1
Ccar = 5 A460 (3.19Ca + 130.3 Cb)/200
Tp physiologie végétale
10 TP ʋ5. Germination des graines
Introduction
La germination est une phase physiologique qui correspond à la transition de la phase de vie latente de la graine sèche à la phase de développement de la plantule. Le processus de
germination commence dès que la graine sèche est hydratée. perméabilité des tégu du métabolisme, qui préparent le déclenchement de la croissance. Au cours de la période de
débutquotesdbs_dbs20.pdfusesText_26
Tp physiologie végétale
5 ʋ.Extraction et séparation des différents pigments photosynthétiquesIntroduction
Les organismes chlorophylliens sont capables de synthétiser des molécules organiquessource d'énergie s'appelle la photosynthèse. L'utilisation de l'énergie lumineuse est rendue
d'onde lorsqu'elles sont éclairées par de la lumière blanche. Cette propriété leur donne une
couleur déterminée. Les chlorophylles sont les pigments majeurs impliqués dans la capture des photons. Lachlorophylle est synthétisée et dégradée dans l'enveloppe du chloroplaste, mais elle n'est
présente et active comme pigment que dans les thylacoïdes. Les caroténoïdes accompagnent toujours les chlorophylles dans les membranes thylacoïdalesoù ils jouent apparemment le double rôle de pigments accessoires pour la capture de l'énergie
lumineuse et de photoprotecteurs contre les intensités lumineuses élevées. On les trouve
également associés à l'enveloppe du chloroplaste. Ils sont aussi très répandus dans de
nombreux tissus végétaux (parenchyme de Tomate, racines de Carottes, pétales, écorce
d'Orange,etc...).1. Matériels et réactifs
Un mortier et pilon ;
sable de mer ; une éprouvette (25, 50, 100mL); un papier filtre ; un bécher (10 et 50 mL) ; erlenmeyer (10 et 50 mL) ; un entonnoir, une pipette Pasteur ;Ether de pétrole ;
Acétone ;
Dichloroéthane ;
un agitateur magnétique, une tige et un barreau (aimant) ; une bande de papier chromatographie de 2 cm de large ; papier aluminium.Tp physiologie végétale
62. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments.1) épinard ;
2) Couper le matériel végétal en petits fragments ;
3) pour obtenir un mélange acétone/eau de concentration final 80%
) et broyer jusqu'à obtenir un mélange homogène ;4) Ajout
5) Laisser décanter quelques minutes (10min) ;
6) Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et
recueillir la solution acétonique de chlorophylles) et compléter 80% ;7) Fermer avec du parafilm et agiter.
Remarque :
éventuellement en tamponnant le milieu avec la craie (CaCO3) ; - Ajouter de Chlorure de Calcium (CaCl2 perméabilisant la membrane chloroplastique.2. Séparation des différents pigments photosynthétiques par chromatographie sur
papier apolaire -à--à-dire1) Introduire dans le tube de chromatographie 10mL de solvant de migration (éther de
pétrole/acétone/dichloroéthane : 8.5/1/0.5 v/v/v) - éluant - () ;2) Fermer hermétiquement le tube ;
3) chromatographie (afin que le dépôt ne soit pas en contact avec le solvant) ;4) Déposer
dilué sur le trait et sécher (Tp physiologie végétale
75) Introduire le chromatogramme dans le tube entouré de papier noir puis fermer le tube ;
6) Arrêter la migration quand le front du solvant aura atteint 20cm.
7) Sécher la chromatographie
2.3 Analyse des résultats
Dessiner le chromatogramme, identifier les pigments en vous aidant des formules, justifier leurs ordres de migration. a) ȕ-Carotène(C40H56) : de couleur orangé; b) Chlorophyllea (C55H72O5N4Mg): de couleur vert bleuté; c) Chlorophylleb (C55H70O6N4Mg): de couleur vert jaune; d) Xanthophylle(C40H56O2) : de couleur jaune.Tp physiologie végétale
8Introduction
La photosynthèse est un mécanisme biochimique permettant aux végétaux supérieurs 2.siège dans des organites propres à la cellule chlorophyllienne: les chloroplastes. De
nombreuses protéines et autres molécules contribuent au mécanisme, parmi eux les pigmentsphotosynthétiques : Chlorophylle a et b ainsi que les caroténoïdes. Ce sont les molécules
Le but de cette expérience est de quantifier par une méthode spectrophotométrique les1. Matériels et réactifs
Spectrophotomètre ;
Deux (02) mortiers et pilons ;
Une éprouvette (25, 50, 100mL);
Un papier filtre ;
Trois (03) béchers (25 et 50 mL) ;
Deux (02) erlenmeyers (25 et 50 mL) ;
Deux (02) petits entonnoirs ;
Dix (10) pipettes Pasteur ;
Cinq (05) pipettes (1, 5 et 10ml) ;
Une poire ;
Cétone (250ml) ;
Un agitateur magnétique, une tige et un barreau (aimant) ;2. Extraction des différents pigments photosynthétiques
(papier aluminium) afin de minimiser les risques de dégradation des pigments. Couper le matériel végétal en petits fragments ; pour obtenir un mélange acétone/eau de concentration final ) et broyer jusqu'à obtenir un mélange homogène ;Tp physiologie végétale
9 yer de nouveau soigneusement ;Laisser décanter quelques minutes (10min) ;
Récupérer le surnageant dans un erlen 10mL (de préférence, filtrer sur papier filtre et recueillir la solution acétonique de chlorophylles) et compléter à 10mL avec de 80% ;Fermer avec du parafilm et agiter.
3. Dosage des pigments totaux
3.1 Rappel
La lumière blanche est composée de différentes radiations visibles dont la longueur -800 nm (rouge foncé). Une substance colorée absorbepréférentiellement certaines radiations de la lumière blanche. Cette propriété lui donne sa
couleur. Si cette substance est un photorécepteur, les radiations absorbées peuvent être celles
qui agissent sur lui et entraînent une photo-réaction.3.2 Protocole
- Fermer la fiole avec du parafilm et agiter ; - recommencer les opérations successivement à 6 pour chaque longueu3.3 Interprétations des résultats
-dessous établies à partir de loi de BEER-LAMBERT permettent de calculer les concentrations en pigments :Ca = 12.7 A663 2.63 A645
Cb = 22.9 A645 4.68 A663 en mg.L-1
Ccar = 5 A460 (3.19Ca + 130.3 Cb)/200
Tp physiologie végétale
10TP ʋ5. Germination des graines
Introduction
La germination est une phase physiologique qui correspond à la transition de la phase de vielatente de la graine sèche à la phase de développement de la plantule. Le processus de
germination commence dès que la graine sèche est hydratée. perméabilité des tégudu métabolisme, qui préparent le déclenchement de la croissance. Au cours de la période de
débutquotesdbs_dbs20.pdfusesText_26[PDF] compte rendu tp chimie minérale
[PDF] compte rendu tp chimie preparation des solutions
[PDF] compte rendu tp exemple
[PDF] compte rendu tp hacheur serie
[PDF] compte rendu tp interference
[PDF] compte rendu tp lentilles minces
[PDF] compte rendu tp optique prisme
[PDF] compte rendu tp ph métrie
[PDF] compte rendu tp redressement et filtrage
[PDF] compte rendu tp redressement simple alternance
[PDF] compte rendu tp refraction de la lumiere
[PDF] compte rendu tp saponification
[PDF] compte rendu type de réunion
[PDF] compte usager bibliothèque paris
