 Chimie des solutions
Chimie des solutions
Objectifs : Niveau CPGE PC en chimie des solutions : - Maîtriser les calculs des concentrations des espèces en solution à l'aide des données théoriques et.
 La Chimie en solution
La Chimie en solution
On pourra calculer la différence de pH observée dans deux solutions acides de même concentration en H+ (mais de force ionique différente liée à la présence ou
 République Algérienne Démocratique et Populaire COURS DE
République Algérienne Démocratique et Populaire COURS DE
LMD Licences Chimie Analytique et Chimie pharmaceutique… Il couvre en cinq chapitres les bases de la Chimie en Solution. Ce module s'inscrit dans le
 F2School
F2School
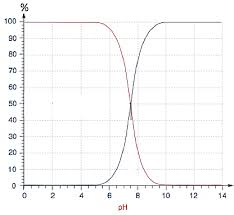
CHIMIE DES SOLUTIONS. 10. III- pH de solutions aqueuses. La mesure du pH d'une solution aqueuse permet de la classer comme solution acide ou basique. Par ...
 Cours module : CHIMIE DES SOLUTIONS- S2 -2021-2022 – Pr M
Cours module : CHIMIE DES SOLUTIONS- S2 -2021-2022 – Pr M
Le thème central est le calcul du pH d'une solution en fonction de la concentration en acide ou en base. *Définir la complexation et la solubilité d'un soluté.
 La chimie une solution pour lavion de demain ?
La chimie une solution pour lavion de demain ?
7 févr. 2020 LA CHIMIE UNE SOLUTION. POUR L'AVION DE DEMAIN ? Arnaud Charles
 Stéphane Mathé
Stéphane Mathé
Pour cette raison le premier chapitre est consacré à l'exposé des notions importantes pour la chimie des solutions. Définition : pH
 Cours et exercices de chimie des solutions
Cours et exercices de chimie des solutions
On parle ainsi d'une solution aqueuse lorsque le solvant est de l'eau. Ceci est particulièrement le cas des solutions dans tous les systèmes vivants.
 L1 Chimie
L1 Chimie
28 sept. 2023 Cette UE introduit les notions de base de la chimie générale (thermochimie et réactions en solution aqueuse). A l'issue de cet enseignement ...
 Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Département de Chimie Cours Chimie des Solutions ... La concentration molaire d'une espèce chimique en solution CA est la quantité de matière de.
 La Chimie en solution
La Chimie en solution
On pourra calculer la différence de pH observée dans deux solutions acides de même concentration en H+ (mais de force ionique différente liée à la présence ou
 Cours de chimie en solution Les acides et les bases
Cours de chimie en solution Les acides et les bases
Une solution aqueuse est toujours le siège d'un équilibre chimique appelé équilibre d'autoprotolyse de l'eau. Cet équilibre s'interprète donc comme une
 Cours et exercices de chimie des solutions
Cours et exercices de chimie des solutions
On parle ainsi d'une solution aqueuse lorsque le solvant est de l'eau. Ceci est particulièrement le cas des solutions dans tous les systèmes vivants.
 COURS DE CHIMIE GENERALE Semestre 1 SVI
COURS DE CHIMIE GENERALE Semestre 1 SVI
Force des acides et des bases. 1.5. Constantes d'acidité et de basicité. 1.6. Coefficient de dissociation d'un acide faible : 2. CALCUL DE PH DES SOLUTIONS
 La chimie une solution pour lavion de demain ?
La chimie une solution pour lavion de demain ?
LA CHIMIE UNE SOLUTION. POUR L'AVION DE DEMAIN ? Arnaud Charles
 République Algérienne Démocratique et Populaire COURS DE
République Algérienne Démocratique et Populaire COURS DE
LMD Licences Chimie Analytique et Chimie pharmaceutique… Il couvre en cinq chapitres les bases de la Chimie en Solution. Ce module s'inscrit dans le
 TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
TRAVAUX PRATIQUES DE CHIMIE DES SOLUTIONS
au cours « chimie des solutions » nécessaires à la compréhension des réactions en solution aqueuse
 COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
CHIMIE DES SOLUTIONS AQUEUSES Solution aqueuse : le solvant est l'eau . ... néiser la solution : on dit que l'eau à un caractère dispersant. Conclusion:.
 La chimie des solutions
La chimie des solutions
LA CHIMIE DES SOLUTIONS Si X est un soluté miscible en solution alors

UNIVERSITE CADI AYYAD
Faculté Polydisciplinaire
SafiDépartement de Chimie
Filière Sciences de la Matière Chimie
Cours Chimie des Solutions
Semestre 2
SMP/SMC
Préparé par :
Moulay Rachid LAAMARI
Juin 2015
1Sommaire
Chapitre I : rappels et généralités
1. Définitions
1.1. Solution
1.2. La masse volumique
1.3. La densité
1.4. Pourcentage ou Fraction
CHAPITRE II : REACTIONS ACIDO-BASIQUES
1. Définitions
1.2. Définition de BRONSTED
1.3. Couple acide-base conjugués
1.4. Force des acides et des bases
2. CALCUL DE PH DES SOLUTIONS AQUEUSES
forte2.4. Cas des bases faibles.
3. Solutions tampon.
3.1. Définition de la ST.
3.2. Propriété de la ST.
3.3. Préparation de la ST.
3.4. Calcul du pH de ST
4. Titrages acide-base.
1.1. 1.2. -REDUCTION1. Généralités.
21.1. Oxydant, réducteur, oxydation, réduction.
1.2. Réaction -réduction
2.1. Définition.
: Equation de Nernst3.1. Potentiel normal (standard)
3.2. Equation de Nernst :
4. Réaction -réduction
4.1. Définition :
4.2. 4.34.4. -réduction
5. Piles électrochimiques - Pile DANIELL.
5.1. Déscription
5.2. Calcul de la f.e.m de la pile
CHAPITRE IV : REACTIONS DE DISSOLUTION-PRECIPITATION1. Solubilité
2. Réaction de précipitation.
3. Produit de solubilité.
3.1. Définition
3.2. Conditions de précipitation.
4. Facteurs influençant la solubilité.
4.1. Influence de la température.
4.3. Influence du pH.
CHAPITRE IV : REACTIONS DE COMPLEXATION
1. Définitions
2. Coordinence et géométrie
3. Nomenclature des complexes :
4. Constante globale de formation du complexe
5. Compétition entre ligands
5.1. Compétition entre deux ligands vis-à-
35.2. Compétition entre deux cations vis-à-
Chapitre I : rappels et généralités
1. Définitions
1.1. Solution
Une solution peut être définie comme un mélange homogène dont les constituants sontdivisés et dispersés l'un dans l'autre au niveau moléculaire. Une solution est toujours constituée :
d'un solvant (constituant majoritaire), d'un ou plusieurs solutés. Les solutions liquides (dites aqueuses lorsque le solvant est l'eau).Les solutés peuvent être :
un gaz (CO2 dans les boissons gazeuses, O2 un solide : sel.1.2. :
on distingue :1.4.1. La concentration molaire
A est la quantité de matière de
cette espèce présente dans un litre de solution. (unité mol/L) Avec : nA la quantité de matière de A en solution et V le volume de la solution.Préparation des solutions aqueuses
a. Détermination de la masse de soluté à peser masse molaire M(X), à la concentration [X]= CXSoit m(X) cette masse.
4Exemple :
On donne M(NaOH)=40 g/mol.
Solution :
On a :
b. Soit V(G) le volume de gaz à dissoudre, V le volume de la solution, Vm le volume molaire des concentration molaire du gaz dans la solution. On a:On a :
donc :Exemple :
On fait dissoudre un volume de 20 cm3 de NH3
de NH3.Solution
5 c. fournie est en général appelée solution mère) On prélève un volume V0 de la solution mère de concentration C0 distillée pour obtenir une solution diluée de volume V1 et de concentration désirée C1.Détermination du volume V0 à prélever
La quantité de matière de soluté dans le volume V0 est: n(X)=C0.V0Cette quantité de matière se retrouve dans la solution après dilution. Cela traduit la conservation
de la matière, donc: n(X)=C1.V1 de conservation de la matière):C0×V0=C1×V1
Le volume à prélever est donc:
sur celle de la solution fille :Opérations à effectuer
6Exemple :
On prélève un volume V0 = 20 de cuivre II de concentration C0=5×10-2 mol.L-1 Ce volume est introduit dans une fiole jaugée de 500 au trait de jauge, puis on homogénéise. a. Comment prélève t on le volume V0 de la solution mère. b. Quelle est la concentration de la solution fille ? c. Calculer le facteur de dilution F effectué.Solution
a. Pour prélever le volume V0 de solution mère on utilise une pipette jaugée car le prélèvement est plus précis. b. Concentration de la solution filleOn sait que la concentration de la solution fille C1 et celle de la solution mère C0 sont reliée
par la relation de dilutionC0×V0=C1×V1
où V0 et V1 désignent respectivement le volume de solution mère prélevé et le volume final de
la solution fille. c. Calcul du facteur de dilution FOn rappelle que
71.4.2. La concentration massique Cm
C'est le rapport de la masse de composé X contenu dans un certain volume de solution divisée par ce volume de solution. La masse est exprimée en kg ou en g et le volume souvent exprimé en L et parfois en m3.Exemple
On dissout 5 g de sulfate de cuivre (CuSO4) dans 40 concentration massique du sulfate de cuivre ?On a :
quotesdbs_dbs2.pdfusesText_2[PDF] Chimie organique_exercices - Chimie - PCSI
[PDF] Licence de Chimie
[PDF] Chimie inorganique - Numilog
[PDF] Chimie 1ère année INTRODUCTION
[PDF] Nomenclature en chimie minérale
[PDF] Chimie MP PT
[PDF] Chimie Tout-en-un MPSI-PTSI - 2e éd
[PDF] chimie organic #259
[PDF] CHIMIE ORGANIQUE PCEM1 Isomérie - Chimie Sup
[PDF] CHM 2520 Chimie organique II
[PDF] COR 301 Chimie Organique II La Chimie du Carbonyle et des
[PDF] Chimie organique en 25 fiches - Numilog
[PDF] organique - Fides Éducation
[PDF] Science de la Matiere ChimieS5 Chimie organique fonctionnelle

