 Correction de lépreuve de chimie filière MP concours MINES
Correction de lépreuve de chimie filière MP concours MINES
Correction CHIMIE(Mines Ponts-MP/2016). Il en résulte que la réaction est totale.donc thermodynamiquement possible. t 11 -. L'évolution du produit de
 Mines MP-2016 Le béton
Mines MP-2016 Le béton
Mines MP-2016. Problème sur 34 points. Ce problème est beaucoup trop long chimie la présence d'ions carbonate dans une solution : l'eau de chaux 2+ + ...
 Mines Chimie PSI 2016 — Corrigé
Mines Chimie PSI 2016 — Corrigé
Habituellement dédié à l'étude d'un élément chimique le sujet de chimie du concours Mines-Ponts en filière PSI a cette année pour thème le béton. Les
 Mines Chimie MP 2016 — Corrigé
Mines Chimie MP 2016 — Corrigé
Habituellement dédié à l'étude d'un élément chimique le sujet de chimie du concours Mines-Ponts en filière MP a cette année pour thème le béton. Les
 Chimie Mines-Ponts PSI 2016 : Carbonatation dun béton
Chimie Mines-Ponts PSI 2016 : Carbonatation dun béton
Chimie. Mines-Ponts PSI 2016 : Carbonatation d'un béton. Q1 – La masse molaire du ciment Ca3SiO5 est de 228 g·mol−1 celle de l'eau est de 18 g·mol−1. On a
 PSI 2016
PSI 2016
Mines Chimie PSI 2016 — Corrigé. 245. Mines Chimie PSI 2016 — Corrigé. Ce concours Mines-Ponts en filière PSI a cette année pour thème le béton. Les ...
 Mines Chimie PC 2016 — Corrigé
Mines Chimie PC 2016 — Corrigé
Mines Chimie PC 2016 — Corrigé. Ce corrigé est proposé par Augustin Long (ENS Lyon); il a été relu par Claire. Besson (Docteur en chimie) et Alexandre Herault
 PC 2016 - Physique · Modélisation · Chimie
PC 2016 - Physique · Modélisation · Chimie
168. 184. Page 4. 8. Mines-Ponts. Physique 1. Le Millenium Bridge. mécanique du Mines Chimie PC 2016 — Corrigé. En remplaçant par les valeurs numériques on ...
 MP 2016 - Physique · Modélisation · Chimie
MP 2016 - Physique · Modélisation · Chimie
22 Les points donnés dans l'énoncé forment deux droites sécantes. Page 35. Mines Chimie MP 2016 — Corrigé. 175. Le béton.
 RAPPORT SUR LE CONCOURS 2016
RAPPORT SUR LE CONCOURS 2016
Le Concours Commun Mines Ponts (CCMP) organisera en 2017 intégralement (écrit et oral) le recrutement dans les filières MP PC
 DM 3 : Sujet chimie Mine-Pont 2016 - Corrigé 1 Prise dun béton 2
DM 3 : Sujet chimie Mine-Pont 2016 - Corrigé 1 Prise dun béton 2
DM 3 : Sujet chimie Mine-Pont 2016 - Corrigé. 1 Prise d'un béton. On considère la réaction chimique : 2 [Ca3SiO5](s) +6H2O(l) = [Ca3Si2O7
 Correction de lépreuve de chimie filière MP concours MINES
Correction de lépreuve de chimie filière MP concours MINES
Correction de l'épreuve de chimie filière MP concours MINES PONTS session 2016 concours MINES PONTS session 2016. EL FILALI SAID. CPGE BENI MELLAL.
 RAPPORT SUR LE CONCOURS 2016
RAPPORT SUR LE CONCOURS 2016
Le but de l'oral du Concours Commun Mines-Ponts n'est pas d'éliminer mais de Le sujet de l'épreuve de chimie 2016 de la filière PC comportait deux ...
 Chimie Mines-Ponts PSI 2016 : Carbonatation dun béton
Chimie Mines-Ponts PSI 2016 : Carbonatation dun béton
Chimie. Mines-Ponts PSI 2016 : Carbonatation d'un béton. Q1 – La masse molaire du ciment Ca3SiO5 est de 228 g·mol?1 celle de l'eau est de 18 g·mol?1.
 MP 2016 - Physique · Modélisation · Chimie
MP 2016 - Physique · Modélisation · Chimie
Mines PSI Chimie. Mines PC Chimie CCP Physique et Chimie MP 2016 — Corrigé ... concours Mines-Ponts en filière MP a cette année pour thème le béton.
 Le Millenium Bridge – Mines-Ponts MP I 2016 - Corrigé
Le Millenium Bridge – Mines-Ponts MP I 2016 - Corrigé
Le Millenium Bridge – Mines-Ponts MP I 2016 - Corrigé. I) Oscillateur simple C'est ce qui s'est produit en 1940 pour le pont de Tacoma.
 Mines Chimie PSI 2016 — Corrigé
Mines Chimie PSI 2016 — Corrigé
Habituellement dédié à l'étude d'un élément chimique le sujet de chimie du concours Mines-Ponts en filière PSI a cette année pour thème le béton.
 Mines Chimie PC 2016 — Corrigé
Mines Chimie PC 2016 — Corrigé
Publié dans les Annales des Concours. 1/22. Mines Chimie PC 2016 — Corrigé. Ce corrigé est proposé par Augustin Long (ENS Lyon); il a été relu par Claire.
 PC 2016 - Physique · Modélisation · Chimie
PC 2016 - Physique · Modélisation · Chimie
Mines-Ponts. Physique 1. Le Millenium Bridge. Mines PC Chimie. Mines MP Chimie ... CCP Modélisation de systèmes physiques ou chimiques PC 2016 — Corrigé.
 laPHYSIQUE-CHIMIE
laPHYSIQUE-CHIMIE
laPHYSIQUE-CHIMIE 13.3 Refroidissement d'un capteur (Mines-Ponts 2016) . ... pour pouvoir faire un vrai sujet de concours mais ce n'est pas le cas.
 Mines Chimie MP 2016 — Corrigé
Mines Chimie MP 2016 — Corrigé
Mines Chimie MP 2016 — Corrigé Ce corrigé est proposé par Alexandre Herault (Professeur en CPGE); il a été relu par Vincent Wieczny (ENS Lyon) et Stéphane Ravier (Professeur en CPGE) Habituellement dédié à l’étude d’un élément chimique le sujet de chimie du concours Mines-Ponts en ?lière MP a cette année pour thème le
 Correction de l’épreuve de chimie filière MP concours MINES
Correction de l’épreuve de chimie filière MP concours MINES
C P G E/Béni Mellal Correction CHIMIE(Mines Ponts-MP/2016) Avant l’équivalence ?av = 2 Co 2 ?(Ca2+) + cv Vo ?(Cl?)+(C o ? cv Vo)?(OH?) Donc la pente avant l’équivalence pav = c Vo [?(Cl?) ??(OH?)] A N GGGGGGGGGGA pav = ?61000 Après l’équivalence ?av = 2 Co 2 ?(Ca2+) + cv Vo ?(Cl?)+(C o ? cv Vo)?(OH?
Correction de l"épreuve de chimie filière MPCorrection de l"épreuve de chimie filière MPconcours MINES PONTS session 2016concours MINES PONTS session 2016
EL FILALI SAID
CPGE BENI MELLAL
MAROC = elfilalisaid@yahoo.fr =LE BÉTON
A -Prise d"un béton
o1-Le réactif limitant : ?Calculons le nombre de moles initiales : no(Ca3SiO5) =m(Ca3SiO5)M(Ca3SiO5)A.NGGGGGGGGGGA no(Ca3SiO5) = 1mol no(H2O) =m(H2O)M(H2O)A.NGGGGGGGGGGA no(H2O) = 5molPuisque
n(Ca3SiO5)2(= 0,5) sente le réactif limitant. ?Les quantités de matières des espèces : n(Ca3SiO5) = 0(réactif limitant)
n(H2O) =no(H2O)-3no(Ca3SiO5)A.NGGGGGGGGGGA n(H2O) = 2mol n(Ca3Si2O7) =12no(Ca3SiO5)A.NGGGGGGGGGGA n(Ca3Si2O7) = 0,5mol n(Ca(OH)2) =32no(Ca3SiO5)A.NGGGGGGGGGGA n(Ca(OH)2) = 1,5molo2-La valeur de l"enthalpie standard de réaction
ΔrHo= [3Cp(Ca(OH)2) +Cp(Ca3Si2O7)-6Cp(Ca(OH)2)]ΔθA.NGGGGGGGGGGA ΔrHo=-5550J B -Basicité d"un béton
o3-La réaction de titrage : H++ OH---??--H2O =?K=1KeA.NGGGGGGGGGGA K= 1014
N.B : Si on écrit la réaction du dosage comme suit : Ca(OH)2+ 2(H3O+,Cl-)--??--4H2O + Ca2+,2Cl-=?K=1K2eA.NGGGGGGGGGGA K= 1028 Mai 2016 Page -1/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) o4-Le pH de la solution prélevée à la surface du béton : A l"équivalence on a :
CbVo=CVe=?Cb=CVeVoA.NGGGGGGGGGGA Cb= 5 10-3molL-1
Et comme la base OH-est une base forte alors
pH= 14 + log[OH-]A.NGGGGGGGGGGA pH= 11,7 o5-Justification de l"allure de la courbe conductimétrique : Commeλ(H+)est plus grande suivie deλ(OH-)alors avant l"équivalence H+réagit avec OH -donc la concentration de H+diminue et par conséquent la conductivité de la solution diminue; après l"équivalence H +ne reste que des traces par contre la concentration de OH -augmente et par conséquent la conductivité de la solution augmente. o6-Pentes des deux droites : Remarque importante
Afin de comparer les pentes on doit travailler dans le même système d"unité (interna- tional) Le volume en m
3donc la concentration en molm-3
?Avant l"équivalence pav=0,06-0,12510-6=?pav=-65000 ?Après l"équivalence pap=0,23-0,061,8-1=?pap= 212500 Vérification:
Remarquons queVo?v=?Vo+v?Vo.
Ca2+OH-H+Cl-
avant éqCo/2CoVo-cv Vo/cv Vo après éqCo/2/cv-CoVo Vo cv Vo Mai 2016 Page -2/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) ?Avant l"équivalence av= 2Co 2λ(Ca2+) +cvVoλ(Cl-) + (Co-cvVo)λ(OH-)
Donc la pente avant l"équivalence
pav=cVo[λ(Cl-)-λ(OH-)]A.NGGGGGGGGGGA pav=-61000 ?Après l"équivalence av= 2Co 2λ(Ca2+) +cvVoλ(Cl-) + (Co-cvVo)λ(OH-)
Donc la pente avant l"équivalence
pav=cVo[λ(Cl-) +λ(H+)]A.NGGGGGGGGGGA pav= 213000 On retrouve presque les même valeurs.
o7-L"allure de la courbe qui aurait été obtenue à l"occasion d"unsuivi pH-métrique : pH 012345678910111213
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14vAmL
?E C -Carbonatation d"un béton
o8-Les règles générales permettant d"établir la configuration électronique d"un atome dans l"état fondamental : Mai 2016 Page -3/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) -/Règle (principe) d"exclusion de Pauli : "Dans un atome ,deux électrons quelconques ne peuvent pas avoir les quatres nombres quantiques identiques» Règle de Klechkovsky :
" Les sous-couches se remplissent par énergie croissante : Les niveaux d"énergieE(n,?)augmentent avec (n+?). E (n,?)qui ont même valeur de (n+?) ,augmente avecn» Règle de Hund:
"Lorsque des électrons sont dans des orbitales dégénérées (demême énergie) la configu-
ration la plus stable est celle pour laquelle le nombre quantique magnétique total de spin M sest maximal.» ?Le vanadium appartient à la quatrième ligne doncn= 4et la colonne 5 donc la confi- guration externe est4s23d3ce qui donne 20Ca : 1s22s22p63s23p64s2
?Pour que le calcium se comporte comme un gaz rare (le plus proche),il perd ces deux électrons de valence (4s2) et devient Ca+2
o9-Le diagramme de prédominance des espèces On rappelle que pour l"équilibre acide-base A
--??--H++B on a : pH=pKA+ log[B] [A] PourpH PourpH>pKA=?la base B prédomine.
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14pH
H2CO3HCO-
3CO2 -
3 En cas du béton dont lepH>10,4le CO2se trouve sous la forme des ions carbonates CO 2 - 3 o10-Montrons que la carbonatation du béton est thermodynamiquementfavorisée. Ca 2++CO3 ---??--CaCO3
Pour cela calculons la constante d"équilibre.
On rappelle queK=e-ΔrGo
RTainsiΔrGo=ΔrHo-TΔrSo
ΔrHo=ΔfHo(CaCO3)-ΔfHo(Ca2+)-ΔfHo(CO3-)A.NGGGGGGGGGGA ΔrHo= 13kJmol-1 ΔrSo=So(CaCO3)-So(Ca2+)-So(CO3-)A.NGGGGGGGGGGA ΔrSo= 203JK-1mol-1 Ce qui donne
ΔrGo=-47494Jmol-1=?K= 211×106?1
Mai 2016 Page -4/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) Il en résulte que la réaction est totale.,donc thermodynamiquement possible. o11-L"évolution du produit de solubilité de la calcite avec la température : On rappelle que :dlnKs
dT=ΔrHosRT2 Pour la réaction : Ca
2++CO3 ---??--CaCO3
?Pour le sens direct la constante d"équilibre vaut1Kset la variation d"enthalpie vaut : rHo. ?Pour le sens indirect la constante d"équilibre vautKset la variation d"enthalpie vaut : -ΔrHo. On suppose queΔrHo=cte(Approximation d"Ellinghamm) PuisqueΔrHo>0alorsdlnKs
dT=-ΔrHoRT2<0c"est à dire quelnKsest une fonction dé- croissante de la température. Et puisque la fonctonlnest bijective alorsKsest une fonction décroissante de la tempéra- ture. Ce qui prouve que la calcite est plus soluble à froid. o12-L"ordre de grandeur du produit de solubilité de la calcite : On a :
Ks=1KA.NGGGGGGGGGGA Ks?4,7×10-9
o13-Exemple d"utilisation en chimie de la faible solubilité du carbonate de calcium par rapport à son hydroxyde : la mise en évidence des ions Ca 2+(soluble dans une solution
sous forme de Ca 2+ 2OH-) en soufflant à la bouche ( on dégage le CO2) on précipite le
carbonate de calcium (moins soluble que l"hydroxyde). o14-Schéma de Lewis de l"ion carbonate. O C O? O? L"ion carbonate présente un hybride de résonance : Donc toute les liaisons sont identiques et par conséquent présentent le même moment dipolaire-→μet puisque les trois angles sont identiques (θ= 120o)alors le moment dipolaire
présente les composantes suivantes dans le repère (Oxy) Mai 2016 Page -5/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) xy μ1 3 -→μ2 2 x=μo-2μocos(θ/2) = (1-2×1 2)μo= 0
y= 0-μosin(θ/2) +μosin(θ/2) = 0 Par conséquent l"ion carbonate ne présente pas un moment dipolaire permanent. o15-Calcul du volume formulaire : On a :N
NA=mM=?m=NMNA
Donc :ρ=m
V=?ρ=NMVNAet par conséquent
V1=VN=MρNAA.NGGGGGGGGGGA V1= 6,1710-29m3
o16-Calcul du volume formulaire de la portlandite. V=a2csin120oA.NGGGGGGGGGGA V= 5,53 10-29m3
La transformation en calcite se fait en augmentation du volume (puisque on a passivation) Un métal est passivé lorsque l"oxyde qui se développe à sa surface peutformer une couche protectrice continue : il faut pour cela que le volume molaire de l"oxyde soit supérieur au volume molaire du métal. RemarquePassivation
D -Corrosion d"un béton armé
o17-Les degrés d"oxydation du fer dans les solides considérés : XFeFe2+Fe3+FeOOHFe3O4
n.o0+II+III+IIIVIII/III Mai 2016 Page -6/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) Remarque
Le fer dans Fe3O4len.odu fer est fractionné c"est à dire que le fer présente deux nombres d"oxydation. Remarquons que Fe
3O4=FeO + Fe2O3et par conséquent lesn.odu fer sont +II et +III
et VIII/III est une valeur moyenne. o18-Attribution : Sachant que le pouvoir oxydant augmente avec le nombre d"oxydation alors : XFeFe2+Fe3+Fe3O4FeOOH
DomaineABDCE
o19-L"équation-bilan de la réaction : 3Fe + 4H2O--??--4H2+ Fe3O4
o20-Le phénomène ainsi observé est la passivation : La formation de Fe
3O4solide empêche la réaction du fer avec l"eau puisqu"ils sont stables
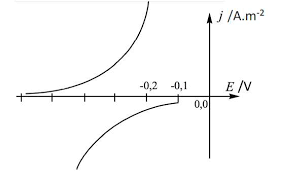
o21-La figure Fe-→Fe2+
H 2←-H2O
Ecor=-0,3(V)|jc|
-|jc| Les demi-équations d"oxydoréduction :
Fe--??--Fe2++2e-
2H 2O=2e---??--H2+2OH-
o22-Construction graphique : Mai 2016 Page -7/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) -0,1 -0,2 -0,3 -0,4 -0,5 -0,6 -0,7 log|j|E(V) E corlog|jc| D 1D 2 ?La droite (D1) de pente positive correspond à une oxydation. ?La droite (D2) de pente négative correspond à une réduction. ?Les deux droites ( droites de Tafel) se coupent au point C (point de fonctionnement) dont les coordonnées sont : Ecpotentiel de corrosion.
log|jc|avec|jc|la densité de courant de corrosion. D"après la courbe on déduitque : Ecor=-0,37V ,log|j|=-5,14 =? |j|= 10-5,14A.m-2
Mai 2016 Page -8/ 8- elfilalisaid@yahoo.fr
quotesdbs_dbs20.pdfusesText_26
n(Ca3SiO5) = 0(réactif limitant)
n(H2O) =no(H2O)-3no(Ca3SiO5)A.NGGGGGGGGGGA n(H2O) = 2mol n(Ca3Si2O7) =12no(Ca3SiO5)A.NGGGGGGGGGGA n(Ca3Si2O7) = 0,5moln(Ca(OH)2) =32no(Ca3SiO5)A.NGGGGGGGGGGA n(Ca(OH)2) = 1,5molo2-La valeur de l"enthalpie standard de réaction
ΔrHo= [3Cp(Ca(OH)2) +Cp(Ca3Si2O7)-6Cp(Ca(OH)2)]ΔθA.NGGGGGGGGGGA ΔrHo=-5550JB -Basicité d"un béton
o3-La réaction de titrage :H++ OH---??--H2O =?K=1KeA.NGGGGGGGGGGA K= 1014
N.B : Si on écrit la réaction du dosage comme suit : Ca(OH)2+ 2(H3O+,Cl-)--??--4H2O + Ca2+,2Cl-=?K=1K2eA.NGGGGGGGGGGA K= 1028Mai 2016 Page -1/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) o4-Le pH de la solution prélevée à la surface du béton :A l"équivalence on a :
CbVo=CVe=?Cb=CVeVoA.NGGGGGGGGGGA Cb= 5 10-3molL-1
Et comme la base OH-est une base forte alors
pH= 14 + log[OH-]A.NGGGGGGGGGGA pH= 11,7 o5-Justification de l"allure de la courbe conductimétrique : Commeλ(H+)est plus grande suivie deλ(OH-)alors avant l"équivalence H+réagit avec OH -donc la concentration de H+diminue et par conséquent la conductivité de la solution diminue; après l"équivalence H +ne reste que des traces par contre la concentration de OH -augmente et par conséquent la conductivité de la solution augmente. o6-Pentes des deux droites :Remarque importante
Afin de comparer les pentes on doit travailler dans le même système d"unité (interna- tional)Le volume en m
3donc la concentration en molm-3
?Avant l"équivalence pav=0,06-0,12510-6=?pav=-65000 ?Après l"équivalence pap=0,23-0,061,8-1=?pap= 212500Vérification:
Remarquons queVo?v=?Vo+v?Vo.
Ca2+OH-H+Cl-
avant éqCo/2CoVo-cv Vo/cv Vo après éqCo/2/cv-CoVo Vo cv VoMai 2016 Page -2/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) ?Avant l"équivalence av= 2Co2λ(Ca2+) +cvVoλ(Cl-) + (Co-cvVo)λ(OH-)
Donc la pente avant l"équivalence
pav=cVo[λ(Cl-)-λ(OH-)]A.NGGGGGGGGGGA pav=-61000 ?Après l"équivalence av= 2Co2λ(Ca2+) +cvVoλ(Cl-) + (Co-cvVo)λ(OH-)
Donc la pente avant l"équivalence
pav=cVo[λ(Cl-) +λ(H+)]A.NGGGGGGGGGGA pav= 213000On retrouve presque les même valeurs.
o7-L"allure de la courbe qui aurait été obtenue à l"occasion d"unsuivi pH-métrique : pH012345678910111213
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14vAmL
?EC -Carbonatation d"un béton
o8-Les règles générales permettant d"établir la configuration électronique d"un atome dans l"état fondamental :Mai 2016 Page -3/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) -/Règle (principe) d"exclusion de Pauli : "Dans un atome ,deux électrons quelconques ne peuvent pas avoir les quatres nombres quantiques identiques»Règle de Klechkovsky :
" Les sous-couches se remplissent par énergie croissante : Les niveaux d"énergieE(n,?)augmentent avec (n+?). E (n,?)qui ont même valeur de (n+?) ,augmente avecn»Règle de Hund:
"Lorsque des électrons sont dans des orbitales dégénérées (demême énergie) la configu-
ration la plus stable est celle pour laquelle le nombre quantique magnétique total de spin M sest maximal.» ?Le vanadium appartient à la quatrième ligne doncn= 4et la colonne 5 donc la confi- guration externe est4s23d3ce qui donne20Ca : 1s22s22p63s23p64s2
?Pour que le calcium se comporte comme un gaz rare (le plus proche),il perd ces deuxélectrons de valence (4s2) et devient Ca+2
o9-Le diagramme de prédominance des espècesOn rappelle que pour l"équilibre acide-base A
--??--H++B on a : pH=pKA+ log[B] [A]PourpH PourpH>pKA=?la base B prédomine.
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14pH
H2CO3HCO-
3CO2 -
3 En cas du béton dont lepH>10,4le CO2se trouve sous la forme des ions carbonates CO 2 - 3 o10-Montrons que la carbonatation du béton est thermodynamiquementfavorisée. Ca 2++CO3 ---??--CaCO3
Pour cela calculons la constante d"équilibre.
On rappelle queK=e-ΔrGo
RTainsiΔrGo=ΔrHo-TΔrSo
ΔrHo=ΔfHo(CaCO3)-ΔfHo(Ca2+)-ΔfHo(CO3-)A.NGGGGGGGGGGA ΔrHo= 13kJmol-1 ΔrSo=So(CaCO3)-So(Ca2+)-So(CO3-)A.NGGGGGGGGGGA ΔrSo= 203JK-1mol-1 Ce qui donne
ΔrGo=-47494Jmol-1=?K= 211×106?1
Mai 2016 Page -4/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) Il en résulte que la réaction est totale.,donc thermodynamiquement possible. o11-L"évolution du produit de solubilité de la calcite avec la température : On rappelle que :dlnKs
dT=ΔrHosRT2 Pour la réaction : Ca
2++CO3 ---??--CaCO3
?Pour le sens direct la constante d"équilibre vaut1Kset la variation d"enthalpie vaut : rHo. ?Pour le sens indirect la constante d"équilibre vautKset la variation d"enthalpie vaut : -ΔrHo. On suppose queΔrHo=cte(Approximation d"Ellinghamm) PuisqueΔrHo>0alorsdlnKs
dT=-ΔrHoRT2<0c"est à dire quelnKsest une fonction dé- croissante de la température. Et puisque la fonctonlnest bijective alorsKsest une fonction décroissante de la tempéra- ture. Ce qui prouve que la calcite est plus soluble à froid. o12-L"ordre de grandeur du produit de solubilité de la calcite : On a :
Ks=1KA.NGGGGGGGGGGA Ks?4,7×10-9
o13-Exemple d"utilisation en chimie de la faible solubilité du carbonate de calcium par rapport à son hydroxyde : la mise en évidence des ions Ca 2+(soluble dans une solution
sous forme de Ca 2+ 2OH-) en soufflant à la bouche ( on dégage le CO2) on précipite le
carbonate de calcium (moins soluble que l"hydroxyde). o14-Schéma de Lewis de l"ion carbonate. O C O? O? L"ion carbonate présente un hybride de résonance : Donc toute les liaisons sont identiques et par conséquent présentent le même moment dipolaire-→μet puisque les trois angles sont identiques (θ= 120o)alors le moment dipolaire
présente les composantes suivantes dans le repère (Oxy) Mai 2016 Page -5/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) xy μ1 3 -→μ2 2 x=μo-2μocos(θ/2) = (1-2×1 2)μo= 0
y= 0-μosin(θ/2) +μosin(θ/2) = 0 Par conséquent l"ion carbonate ne présente pas un moment dipolaire permanent. o15-Calcul du volume formulaire : On a :N
NA=mM=?m=NMNA
Donc :ρ=m
V=?ρ=NMVNAet par conséquent
V1=VN=MρNAA.NGGGGGGGGGGA V1= 6,1710-29m3
o16-Calcul du volume formulaire de la portlandite. V=a2csin120oA.NGGGGGGGGGGA V= 5,53 10-29m3
La transformation en calcite se fait en augmentation du volume (puisque on a passivation) Un métal est passivé lorsque l"oxyde qui se développe à sa surface peutformer une couche protectrice continue : il faut pour cela que le volume molaire de l"oxyde soit supérieur au volume molaire du métal. RemarquePassivation
D -Corrosion d"un béton armé
o17-Les degrés d"oxydation du fer dans les solides considérés : XFeFe2+Fe3+FeOOHFe3O4
n.o0+II+III+IIIVIII/III Mai 2016 Page -6/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) Remarque
Le fer dans Fe3O4len.odu fer est fractionné c"est à dire que le fer présente deux nombres d"oxydation. Remarquons que Fe
3O4=FeO + Fe2O3et par conséquent lesn.odu fer sont +II et +III
et VIII/III est une valeur moyenne. o18-Attribution : Sachant que le pouvoir oxydant augmente avec le nombre d"oxydation alors : XFeFe2+Fe3+Fe3O4FeOOH
DomaineABDCE
o19-L"équation-bilan de la réaction : 3Fe + 4H2O--??--4H2+ Fe3O4
o20-Le phénomène ainsi observé est la passivation : La formation de Fe
3O4solide empêche la réaction du fer avec l"eau puisqu"ils sont stables
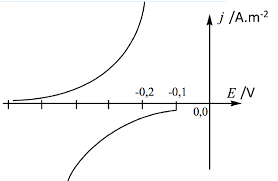
o21-La figure Fe-→Fe2+
H 2←-H2O
Ecor=-0,3(V)|jc|
-|jc| Les demi-équations d"oxydoréduction :
Fe--??--Fe2++2e-
2H 2O=2e---??--H2+2OH-
o22-Construction graphique : Mai 2016 Page -7/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) -0,1 -0,2 -0,3 -0,4 -0,5 -0,6 -0,7 log|j|E(V) E corlog|jc| D 1D 2 ?La droite (D1) de pente positive correspond à une oxydation. ?La droite (D2) de pente négative correspond à une réduction. ?Les deux droites ( droites de Tafel) se coupent au point C (point de fonctionnement) dont les coordonnées sont : Ecpotentiel de corrosion.
log|jc|avec|jc|la densité de courant de corrosion. D"après la courbe on déduitque : Ecor=-0,37V ,log|j|=-5,14 =? |j|= 10-5,14A.m-2
Mai 2016 Page -8/ 8- elfilalisaid@yahoo.fr
quotesdbs_dbs20.pdfusesText_26
PourpH>pKA=?la base B prédomine.
0 1 2 3 4 5 6 7 8 9 10 11 12 13 14pH
H2CO3HCO-
3CO2 -
3 En cas du béton dont lepH>10,4le CO2se trouve sous la forme des ions carbonates CO 2 - 3 o10-Montrons que la carbonatation du béton est thermodynamiquementfavorisée. Ca2++CO3 ---??--CaCO3
Pour cela calculons la constante d"équilibre.
On rappelle queK=e-ΔrGo
RTainsiΔrGo=ΔrHo-TΔrSo
ΔrHo=ΔfHo(CaCO3)-ΔfHo(Ca2+)-ΔfHo(CO3-)A.NGGGGGGGGGGA ΔrHo= 13kJmol-1 ΔrSo=So(CaCO3)-So(Ca2+)-So(CO3-)A.NGGGGGGGGGGA ΔrSo= 203JK-1mol-1Ce qui donne
ΔrGo=-47494Jmol-1=?K= 211×106?1
Mai 2016 Page -4/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) Il en résulte que la réaction est totale.,donc thermodynamiquement possible. o11-L"évolution du produit de solubilité de la calcite avec la température :On rappelle que :dlnKs
dT=ΔrHosRT2Pour la réaction : Ca
2++CO3 ---??--CaCO3
?Pour le sens direct la constante d"équilibre vaut1Kset la variation d"enthalpie vaut : rHo. ?Pour le sens indirect la constante d"équilibre vautKset la variation d"enthalpie vaut : -ΔrHo. On suppose queΔrHo=cte(Approximation d"Ellinghamm)PuisqueΔrHo>0alorsdlnKs
dT=-ΔrHoRT2<0c"est à dire quelnKsest une fonction dé- croissante de la température. Et puisque la fonctonlnest bijective alorsKsest une fonction décroissante de la tempéra- ture. Ce qui prouve que la calcite est plus soluble à froid. o12-L"ordre de grandeur du produit de solubilité de la calcite :On a :
Ks=1KA.NGGGGGGGGGGA Ks?4,7×10-9
o13-Exemple d"utilisation en chimie de la faible solubilité du carbonate de calcium par rapport à son hydroxyde : la mise en évidence des ions Ca2+(soluble dans une solution
sous forme de Ca 2+2OH-) en soufflant à la bouche ( on dégage le CO2) on précipite le
carbonate de calcium (moins soluble que l"hydroxyde). o14-Schéma de Lewis de l"ion carbonate. O C O? O? L"ion carbonate présente un hybride de résonance : Donc toute les liaisons sont identiques et par conséquent présentent le même momentdipolaire-→μet puisque les trois angles sont identiques (θ= 120o)alors le moment dipolaire
présente les composantes suivantes dans le repère (Oxy)Mai 2016 Page -5/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) xy μ1 3 -→μ2 2 x=μo-2μocos(θ/2) = (1-2×12)μo= 0
y= 0-μosin(θ/2) +μosin(θ/2) = 0 Par conséquent l"ion carbonate ne présente pas un moment dipolaire permanent. o15-Calcul du volume formulaire :On a :N
NA=mM=?m=NMNA
Donc :ρ=m
V=?ρ=NMVNAet par conséquent
V1=VN=MρNAA.NGGGGGGGGGGA V1= 6,1710-29m3
o16-Calcul du volume formulaire de la portlandite.V=a2csin120oA.NGGGGGGGGGGA V= 5,53 10-29m3
La transformation en calcite se fait en augmentation du volume (puisque on a passivation) Un métal est passivé lorsque l"oxyde qui se développe à sa surface peutformer une couche protectrice continue : il faut pour cela que le volume molaire de l"oxyde soit supérieur au volume molaire du métal.RemarquePassivation
D -Corrosion d"un béton armé
o17-Les degrés d"oxydation du fer dans les solides considérés :XFeFe2+Fe3+FeOOHFe3O4
n.o0+II+III+IIIVIII/IIIMai 2016 Page -6/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016)Remarque
Le fer dans Fe3O4len.odu fer est fractionné c"est à dire que le fer présente deux nombres d"oxydation.Remarquons que Fe
3O4=FeO + Fe2O3et par conséquent lesn.odu fer sont +II et +III
et VIII/III est une valeur moyenne. o18-Attribution : Sachant que le pouvoir oxydant augmente avec le nombre d"oxydation alors :XFeFe2+Fe3+Fe3O4FeOOH
DomaineABDCE
o19-L"équation-bilan de la réaction :3Fe + 4H2O--??--4H2+ Fe3O4
o20-Le phénomène ainsi observé est la passivation :La formation de Fe
3O4solide empêche la réaction du fer avec l"eau puisqu"ils sont stables
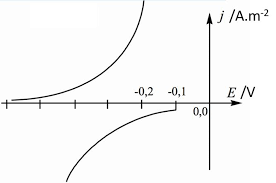
o21-La figureFe-→Fe2+
H2←-H2O
Ecor=-0,3(V)|jc|
-|jc|Les demi-équations d"oxydoréduction :
Fe--??--Fe2++2e-
2H2O=2e---??--H2+2OH-
o22-Construction graphique :Mai 2016 Page -7/ 8- elfilalisaid@yahoo.fr
CPGE BENI MELLAL- EL FILALI SAID-CPGE BENI MELLAL-EL FILALI SAID C.P.G.E/Béni.Mellal Correction CHIMIE(Mines Ponts-MP/2016) -0,1 -0,2 -0,3 -0,4 -0,5 -0,6 -0,7 log|j|E(V) E corlog|jc| D 1D 2 ?La droite (D1) de pente positive correspond à une oxydation. ?La droite (D2) de pente négative correspond à une réduction. ?Les deux droites ( droites de Tafel) se coupent au point C (point de fonctionnement) dont les coordonnées sont :Ecpotentiel de corrosion.
log|jc|avec|jc|la densité de courant de corrosion. D"après la courbe on déduitque :Ecor=-0,37V ,log|j|=-5,14 =? |j|= 10-5,14A.m-2
Mai 2016 Page -8/ 8- elfilalisaid@yahoo.fr
quotesdbs_dbs20.pdfusesText_26[PDF] corrigé note administrative saenes
[PDF] corrigé note de synthèse
[PDF] corrigé note de synthèse avec proposition
[PDF] corrigé note de synthèse concours attaché territorial
[PDF] corrigé note de synthèse concours rédacteur territorial 2015
[PDF] corrigé nouvelle calédonie 2017 maths
[PDF] corrigé nouvelle calédonie 2017 maths es
[PDF] corrigé organisation et gestion de la pme 2016
[PDF] corrigé organisation et gestion de la pme 2017
[PDF] corrigé physique 2014 metropole
[PDF] corrigé physique amerique du nord 2017
[PDF] corrigé point de mire secondaire 1
[PDF] corrigé pondichéry 2016 maths es
[PDF] corrigé pondichéry 2017 maths brevet
