 Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Cette entropie est appelé ”entropie de mélange”. Le processus de mélange Dans une évolution isobare la pression reste constante. La loi des gaz parfaits ...
 Thermodynamique
Thermodynamique
Isobare. Isotherme. nR. −1 ln. T f. Ti. nR. −1 ln. T f. Ti. nRln. V f. V i. S=S créée L'entropie est une variable d'état : sa valeur ne dépend pas ...
 LES DIAGRAMMES THERMODYNAMIQUES
LES DIAGRAMMES THERMODYNAMIQUES
Le diagramme entropique est le diagramme (T-S). Tout particulièrement approprié pour l'étude des évolutions isobares et isentropes il est très employé dans les
 TD 22 (Chap. 21) – Deuxi`eme principe de la thermodynamique
TD 22 (Chap. 21) – Deuxi`eme principe de la thermodynamique
alors une isobare est de la forme T ⇠ eS/Cp . App8. Cycle moteur. 1. 2. Variation d'entropie d'un gaz parfait ∆S
 Chapitre 21 Deuxième principe bilan dentropie
Chapitre 21 Deuxième principe bilan dentropie
Représenter (en les justifiant) les transformations isotherme isobare
 Chapitre 7-Changement d état des corps purs. Cas particulier de l
Chapitre 7-Changement d état des corps purs. Cas particulier de l
d'état de manière isobare (et donc isotherme puisque p = f(T)). Entre les d'entropie. b. Formule de Clapeyron: Considérons un corps pur sous deux phases ...
 «EXERCICES ET PROBLEMES CORRIGES DE
«EXERCICES ET PROBLEMES CORRIGES DE
- L'entropie molaire standard de formation …………………… - La variation d'entropie d'une réaction chimique …………… B. L'enthalpie libre …………
 MariePaule Bassez http://chemphys.ustrasbg.fr/mpb
MariePaule Bassez http://chemphys.ustrasbg.fr/mpb
H ~ 0 la réaction évolue dans le sens d'une augmentation de l'entropie. ○ Si (coefficient d'expansion thermique isobare ou de dilatation isobare).. T.
 UNIVERSITE BADJI MOKHTAR - ANNABA2016/2017 1 Année LMD
UNIVERSITE BADJI MOKHTAR - ANNABA2016/2017 1 Année LMD
Exercice 2: Entropie d'un mélange / Entropie lors d'un changement d'état. 1- 2Kg d'eau à 90°C sont mélangés à 3Kg d'eau à 10°Cde façon adiabatique puis isobare.
 Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Variation d'entropie : dS = ?Q/T. Evolutions isobare et isochore. Dans une évolution isobare la pression reste constante. La loi des gaz parfaits permet.
 Entropie et deuxième principe de la thermodynamique
Entropie et deuxième principe de la thermodynamique
V. Entropie et deuxième principe de la thermodynamique La variation d'entropie est donnée par : ... c) Transformation isobare :.
 Thermodynamique
Thermodynamique
Variation d'entropie (plus facile à évaluer) : d S= Q. T. Transformation réversibles gaz parfait. ?S. Adiabatique. 0. Isocore. Isobare. Isotherme.
 LES DIAGRAMMES THERMODYNAMIQUES
LES DIAGRAMMES THERMODYNAMIQUES
2.3 Isobares et isochores (point L) puis l'évolution isotherme-isobare LV c'est-à-dire la ... Le diagramme entropique est le diagramme (T-S).
 Chapitre 7-Changement d état des corps purs. Cas particulier de l
Chapitre 7-Changement d état des corps purs. Cas particulier de l
L'entropie croît dans une transition liquide-vapeur. 2. Zone d'existence des différentes Diagramme pV (de Clapeyron). Diagramme entropique T
 Chapitre VIII. Les diagrammes thermodynamiques
Chapitre VIII. Les diagrammes thermodynamiques
VIII.1.1 Représentation des isobares et isochores : Isobare (P=cte) ... diagramme de Clapeyron et celle mesurée sur le diagramme entropique.
 Second principe de la thermodynamique. Bilans entropiques I
Second principe de la thermodynamique. Bilans entropiques I
L'entropie S a les dimensions d'une énergie divisée par une température. La transformation étant isobare Q = ?H = h2(T) ? h1(T) = ?h1?2(T). La.
 Concours dentrée- juin 2020 Epreuve de Thermodynamique
Concours dentrée- juin 2020 Epreuve de Thermodynamique
Déterminer la variation d'entropie pour une évolution isobare d'une mole d'oxygène entre 0 et 100 degrés Celsius (en J/K.mole). (1 pt).
 COURS DE THERMODYNAMIQUE
COURS DE THERMODYNAMIQUE
thermodynamique les notions et les différentes expressions de l'entropie
 UNIVERSITE BADJI MOKHTAR - ANNABA2016/2017 1 Année LMD
UNIVERSITE BADJI MOKHTAR - ANNABA2016/2017 1 Année LMD
Exercice 1 : Variation d'entropie d'un gaz parfait 1- 2Kg d'eau à 90°C sont mélangés à 3Kg d'eau à 10°Cde façon adiabatique puis isobare.
 University of California Berkeley
University of California Berkeley
University of California Berkeley
 Handout 7 Entropy - Stanford University
Handout 7 Entropy - Stanford University
3 Boltzmann’s entropy expression S;V;N;Eare all state functions in thermodynamics Furthermore Sis a function of (N;V;E) S(N;V;E) is a material speci c equation of state
 6 Thermodynamik - Heidelberg University
6 Thermodynamik - Heidelberg University
Die Entropie Sist ein Maß für die Wahrscheinlichkeit ?S der Entropieunterschied zwischen dem Ausgangs- und dem Endzustand entscheidet mit darüber ob eine Reaktion ablaufen kann Eine „exotherme Reaktion“ (?H < 0) kann nicht schon alleine nur deswegen ablaufen weil sie exotherm ist
 Chapitre VIII Diagrammes thermodynamiques
Chapitre VIII Diagrammes thermodynamiques
VIII 2 4 : Représentation de l’isobare et de l’isochore sur le diagramme (T S) Plaçons nous en un point M du diagramme (T S) et cherchons à situer l’isobare (l’isochore) en ce point Soient V dS P dT et dS dT les pentes des tanjentes à l’isobare et à l’isochore du point M arbitraire du diagramme (T S)
 Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
L’entropie étant une fonction d’état sa variation ne dépend que de l’état initial et de l’état?nal Considérons donc la transformation isobare {P1V1}? 1 2 suivi de la transformation isochore {P1V2}? 2 2 Dans la première transformation la variation d’entropie est?S1 = nCpln ³ V2 V1 ´ Lors
 1 Introduction 2 Entropy - CMU School of Computer Science
1 Introduction 2 Entropy - CMU School of Computer Science
Example 2 1 Let us de ne X as follows: X = 8 >> < >>: red with probability 1 2 green with probability 1 4 blue with probability 1 8 yellow with probability 1 8 Note we use colors as the discrete values to avoid confusion with numbers
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 80
Chapitre VIII. Les diagrammes thermodynamiques
Introduction.
Tout fluide (liquide ou gaz) à son état d'équilibre est caractérisé par des
grandeurs thermodynamiques (variables d'état ou fonctions d'état) (P, V, T, U, H, S).Equation caractéristique d'un fluide.
Soit f(x, y, z) = 0 avec x, y, z variables d'état. On peut mettre sous la forme z=f(x, y). Donc dans le plan (x, y), on peut tracer des courbes d'équation z = cte.VIII.1 : Diagramme de Clapyron (P, V).
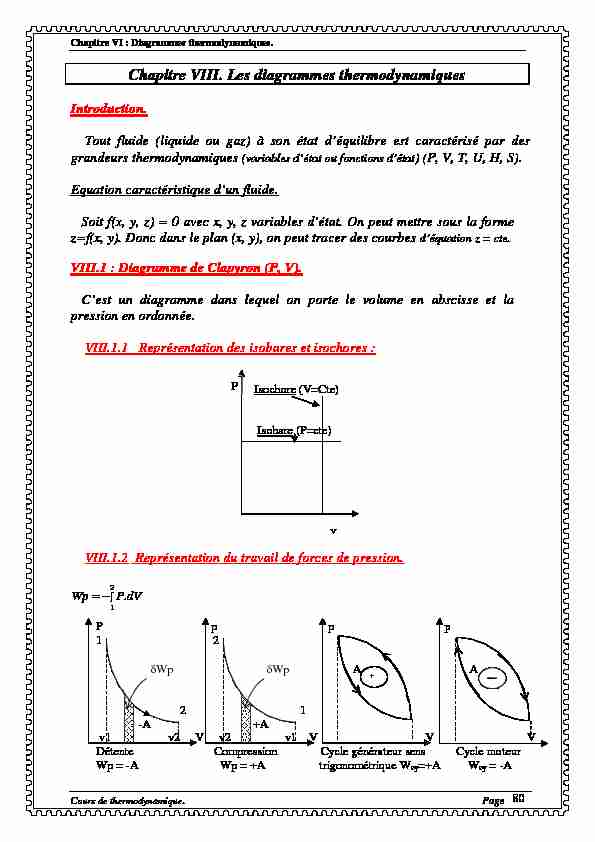
C'est un diagramme dans lequel on porte le volume en abscisse et la pression en ordonnée. VIII.1.1 Représentation des isobares et isochores : VIII.1.2 Représentation du travail de forces de pression. 21.dVPWp
Isochore (V=Cte)
Isobare (P=cte)
P vP p p p
1 2
Wp Wp A A 2 1 -A +Av1 v2 V v2 v1 V V V
Détente Compression Cycle générateur sens Cycle moteurWp = -A Wp = +A trigonométrique Wcy=+A Wcy = -A
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 81
VIII.1.3 : Représentation des isothermes et adiabatiques réversibles : Les isothermes sont représentées par des courbes d'équation P.V = cte ouP = Cte /V.
Ce sont des hyperboles équilatères. Les adiabatiques sont représentées par des courbes d'équation P .V = cte (voir chapitre gaz parfait). TV P : Pente au point M de la courbe qui représente la transformation isotherme. QV P : Pente au point M de la courbe qui représente la transformation adiabatique QV P TV P avec > 1 QV P TV P : Fluide monophasique.Remarque :
Les adiabatiques réversibles ont une forme compliquée à tracer, particulièrement pour des grandes variations de pression et de volume. Exemple : Turbine à vapeur ( Pression à l'admission 20 Bars, Pression à l'échappement 0,02 Bars. VIII.1.4 : Cas de la vapeur d'eau (fluide diphasique (Liq + Vap)Permet de calculer le titre
en vapeurConclusion :
Le diagramme de ClapyRon est commode à utiliser pour des considérations etétudes théoriques.
Pour lire des valeurs numériques et faire des calculs on utilisera les diagrammes Entropique et EnthalpiqueP Adiabatique (Q = 0)
QV P TV PIsotherme
VP C : point critique
Isotherme
C critique (Tc)
liq+ vapLiq Vap
Courbe de saturation
VIsotherme T Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 82
VIII.2 : Diagramme entropique (T, S)
Abscisse Entropie
Ordonnée température.
VIII.2.1 : Représentation des isothermes et isentropiques (adiabatiques et réversibles) VIII.2.2 : Quantité de chaleur échangée
A A dSTQ dSTQ iST QdS B A rev rev rev Q Q A B B A A B de réversibletion Transforma
BA de réversibletion Transforma
0 Remarque :
Analogie entre
2 1 .dvPWdans le diagramme (p, v) et B A revdSTQ. dans le diagramme (T,S). Cas d'un cycle :
Qrev = + A si le cycle est
parcouru dans le sens d'une aiguille d'une montre. Qrev = - A si le cycle est parcouru
dans le sens trigonométrique. T T
Isotherme T=cte T1 B C Cycle de Carnot
T2 A D
0 S S1 S2 S
Isentropique
S= cte T B TB TA A S T T
B B
+A -Aquotesdbs_dbs2.pdfusesText_2
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 82
VIII.2 : Diagramme entropique (T, S)
Abscisse Entropie
Ordonnée température.
VIII.2.1 : Représentation des isothermes et isentropiques (adiabatiques et réversibles)VIII.2.2 : Quantité de chaleur échangée
A A dSTQ dSTQ iST QdS B A rev rev rev Q Q A B B AA B de réversibletion Transforma
BA de réversibletion Transforma
0Remarque :
Analogie entre
2 1 .dvPWdans le diagramme (p, v) et B A revdSTQ. dans le diagramme (T,S).Cas d'un cycle :
Qrev = + A si le cycle est
parcouru dans le sens d'une aiguille d'une montre.Qrev = - A si le cycle est parcouru
dans le sens trigonométrique.T T
Isotherme T=cte T1 B CCycle de Carnot
T2A D
0 S S1 S2 S
Isentropique
S= cte T B TB TA A ST T
B B
+A -Aquotesdbs_dbs2.pdfusesText_2[PDF] torseur de cohésion exercice corrigé pdf
[PDF] enthalpie libre standard
[PDF] entropie
[PDF] enthalpie de dissolution formule
[PDF] exercice corrigé flexion charge repartie
[PDF] enthalpie libre unité
[PDF] comment faire un folioscope
[PDF] fiche fabrication zootrope
[PDF] bandes zootrope
[PDF] folioscope facile a faire
[PDF] les mots d'origine étrangère exercices
[PDF] leçon origine des mots cycle 3
[PDF] flocon de von koch exercice
[PDF] réaction inflammatoire pdf
