 Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude dune réaction : titrage des ions fer II par les ions permanganate
Solution de permanganate de potassium. K+(aq) + MnO4. -(aq). Concentration [MnO4. -]. Volume équivalent Véq à déterminer ? Solution acidifiée de sel de Mohr.
 TP N.04 Dosage doxydoréduction - Suivi potentiométrique 1
TP N.04 Dosage doxydoréduction - Suivi potentiométrique 1
Écrire l'équation de dissolution du sel de Mohr; préciser les esp`eces présentes dans la solution? Pourquoi doit-on acidifier la solution de permanganate de ...
 UNIVERSITE PARIS 12
UNIVERSITE PARIS 12
Pour éviter ce problème on utilisera le sel de Mohr
 Le but du dosage à réaliser est de déterminer la concentration en
Le but du dosage à réaliser est de déterminer la concentration en
solution de sel de Mohr connaissant la concentration d'une solution de permanganate de potassium acidifiée constituée d'ions permanganate MnO4. -. S Maret.
 Dosage doxydoréduction - Suivi potentiométrique - CORRECTION
Dosage doxydoréduction - Suivi potentiométrique - CORRECTION
Dans ce TP on réalise le dosage d'une solution de sel de Mohr (ions. ) par une solution de permanganate ( 0 ). La réaction de dosage est une réaction
 Dosage potentiométrique
Dosage potentiométrique
solution de permanganate de potassium à la concentration C1 = 20.10-2 mol.L-1. La solution d'ions fer II est préparée avec du sel de Mohr : Le sel de Mohr
 - est réduit en MnO2 insoluble de couleur brune qui empêche la
- est réduit en MnO2 insoluble de couleur brune qui empêche la
DOSAGE des IONS FER (II) contenus dans le SEL de MOHR. I- PRÉPARATION de la • Préparer la burette la remplir de la solution de permanganate de potassium.
 TP Dosage volumétriques doxydoréduction 1. Préparation dune
TP Dosage volumétriques doxydoréduction 1. Préparation dune
Boucher agiter et compléter avec l'eau déminéralisée. 2. Dosage du sel deMohr avec la solution de permanganate de potassium. Placer dans la burette une
 Le dosage de léthanol dans un vin
Le dosage de léthanol dans un vin
Le reste de permanganate est ensuite dosé par une solution de sel de Mohr en milieu permanganate de potassium 025 M (KMnO4):. Il faut introduire dans le ...
 TP 13 DOSAGE des IONS FER (II) contenus dans le SEL de MOHR
TP 13 DOSAGE des IONS FER (II) contenus dans le SEL de MOHR
(V ) = volume de solution de permanganate de potassium verséàl'équivalence. avancement. 8H+. + 5 Fe2+ + MnO4. -. ? 5 Fe.
 Étude dune réaction : titrage des ions fer II par les ions permanganate
Étude dune réaction : titrage des ions fer II par les ions permanganate
Solution de permanganate de potassium. K+(aq) + MnO4. -(aq). Concentration [MnO4. -]. Volume équivalent Véq à déterminer ? Solution acidifiée de sel de Mohr.
 UNIVERSITE PARIS 12
UNIVERSITE PARIS 12
Première partie : préparation d'une solution étalon de Fe2+ et dosage d'une Le permanganate de potassium KMnO4 sel soluble et totalement dissocié
 DOSAGE DU FER (II) DANS LE SEL DE MOHR PAR LE
DOSAGE DU FER (II) DANS LE SEL DE MOHR PAR LE
On dose une solution de fer (II) de concentration (C2) par une solution de permanganate de potassium de concentration (C1 = 002 mol.L-1) en milieu acide. Le
 Détermination de la formule du sel de Mohr
Détermination de la formule du sel de Mohr
On réalise le dosage des ions Fe2+ d'une solution S1 obtenue par dilution de S0 par une solution de permanganate de potassium de concentration Co= 300.10-2 mol
 TRAVAUX PRATIQUES DE CHIMIE
TRAVAUX PRATIQUES DE CHIMIE
En milieu acide fort le permanganate de potassium (solution oxydante) peut être Mesure 2 : Doser 10mL de sel de Mohr par la solution de permanganate en.
 Synthèse et analyse dun complexe : loxalate de fer II
Synthèse et analyse dun complexe : loxalate de fer II
Dissoudre 8 g de sel de Mohr dans 25 mL d'eau acidifiée par 1 mL d'H2SO4 2 mol. réactif titrant dans une burette : solution de permanganate de potassium.
 Dosage de léthanol dans un vin blanc
Dosage de léthanol dans un vin blanc
acide éthanoïque par un excès de permanganate de potassium en milieu acide. Le permanganate en excès est dosé par une solution étalonnée de sel de Mohr.
 E 1 FICHE GENERALE
E 1 FICHE GENERALE
Pour déterminer la concentration de la solution à doser cS on connaît : ETALONNAGE DU PERMANGANATE DE. POTASSIUM ... DE POTASSIUM PAR LE SEL DE MOHR.
 Le dosage de léthanol dans un vin
Le dosage de léthanol dans un vin
Le reste de permanganate est ensuite dosé par une solution de sel de Mohr en 50 ml préparer une solution A de permanganate de potassium 025 M (KMnO4):.
N° 785
Synthèse et analyse d"un complexe :
l"oxalate de fer II par Jérôme GIRARDUniversité Paul Sabatier - 31000 Toulouse
et Florence MICHAUDTA Académie de Toulouse
La synthèse (fort simple) de ce complexe sera suivie de son analyse par deux méthodes afin de déterminer sa stoechiométrie.La réaction de synthèse peut s"écrire :
Fe 2 + + x C 2 O 4 2 - + y H 2O ® Fe(C
2 O 4 x (H 2 O) y L"analyse permettra de vérifier que x = 1 (électroneutralité respec- tée) et de déterminer y. Enfin nous discuterons de la structure de ce complexe.A - Synthèse du complexe [1]
1 - Réactifs
- Sel de Mohr : Fe SO 4 (NH 4 2 SO 4 ,6H 2O M = 392,13 g.mol
- 1 H 2 SO 4 (2 mol.L - 1 - Acide oxalique : H 2 C 2 O 4 , 2H 2O M = 126,07 g.mol
- 1 - Acétone.2 - Mode opératoire
- Dissoudre de sel de Mohr dans 25 mL d"eau acidifiée par 1 mL d" H 2 SO 42 mol.L
- 1 - Préparer une solution d"acide oxalique : dans 30 mL d"eau. - Ajouter la totalité de cette solution à celle de sel de Mohr et chauffer lentement jusqu"à ébullition. Un précipité jaune apparaît.BULLETIN DE L"UNION DES PHYSICIENS 1125
Vol. 90 - Juin 1996 J. GIRARD...
- Filtrer ce précipité sur Büchner ou verre fritté. Le laver avec 30 mL d"eau chaude (60°C) puis avec 30 mL d"acétone. Laisser l"aspiration se poursuivre cinq minutes. - Recueillir le produit dans une boîte de Pétri préalablement pesée. Sécher à l"étuve (60°C) ou à défaut à l"air libre pendant quelques jours. - Déterminer la masse d"oxalate de fer II sec obtenu.B - Analyse du complexe : dosage des ions
Fe 2 + et C 2 O 4 2 [1]1.PREMIÈRE MÉTHODE : POTENTIOMÉTRIE
1 - Expérience
Dissoudre, dans 20 mL d"
H 2 SO 42 mol.L
- 1 , environ 120 mg de complexe sec (masse m pesée avec précision). Chauffer légèrement pour le dissoudre. Attention : si on chauffe trop, on risque de favoriser l"oxydation de Fe 2 + en Fe 3 + Réaliser le montage potentiométrique suivant : - électrodes : calomel saturée, platine, - réactif titrant dans une burette : solution de permanganate de potassium KMnO 4 (C = 0.0200 mol.L - 1 Au début du dosage, la couleur du permanganate disparaît instanta- nément et le potentiel prend rapidement une valeur stable. Puis après un premier saut de potentiel, (observé pour un volume V 1 ) la décoloration est plus lente et le potentiel, après avoir augmenté, diminue assez rapidement. Dans cette partie, on notera le potentiel maximal obtenu après l"ajout, puis le potentiel trente secondes et une minute après.Après un deuxième saut de potentiel (volume
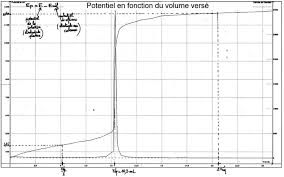
V 2 ) le potentiel prend, après chaque ajout, une valeur stable et la couleur du permanganate persiste. Poursuivre le titrage 5 mL au-delà de l"équivalence.Tracer la courbe D
E = E platine - E calomel = f (V MnO 4 ) sur une feuille de papier millimétré.1126 BULLETIN DE L"UNION DES PHYSICIENS
Synthèse et analyse d"un complexe... B.U.P. n° 785Déterminer sur la courbe V
1 et V 2 . La méthode des tangentes n"est pas valable ici; nous avons fait une détermination à vue de nez. (Exemple de courbe obtenue en annexe).2 - Interprétation
On donne :
H 2 C 2 O 4 pKa 1 = 1,2 pKa 2 = 4,3 E 0 (Fe 3 + Fe 2 + ) = + 0,77 V E 0 (CO 2 1 2 H 2 C 2 O 4 ) = - 0,49 V E 0 (MnO 4 - Mn 2 + ) = + 1,49 VA la lecture de ces potentiels, MnO
4 - devrait oxyder H 2 C 2 O 4 puis Fe 2 + Or c"est le contraire qui se produit. Il faut tenir compte de la cinétique de ces réactions : le système Fe 3 + Fe 2 + est un système rapide et le système CO 2 1 2 H 2 C 2 O 4 est un système lent. Ainsi MnO 4 - réagit d"abord avec Fe 2 + (entre les volumes V = 0 et V 1 ) puis avec H 2 C 2 O 4 (entre V 1 et V 2 ) avec une évolution lente du potentiel car les ions MnO 4 - ne sont réduits en Mn 2 + que petit à petit.3 - Détermination de la stoechiométrie
Entre V = 0 et
V 1 la réaction de dosage est : MnO 4 + 8 H 3 O + 5 Fe 2 +® Mn
2 + + 12 H 2O + 5 Fe
3 + donc il faut une mole de MnO 4 pour oxyder cinq moles de Fe 2 + n Fe2 + = 5 C V
1 masse de Fe 2 + dans l"échantillon (en g) : m Fe2 + = n
Fe 2 + M Fe2 + = 5 . 55,8 C V
· Entre V
1 et V 2 MnO 4 - + 5 2 H 2 C 2 O 4 + 3 H 3 O® Mn
2 + + 7 H 2O + 5 CO
2BULLETIN DE L"UNION DES PHYSICIENS 1127
Vol. 90 - Juin 1996 J. GIRARD...
donc il faut une mole de MnO 4 - pour oxyder deux moles et demi de H 2 C 2 O 4 n H 2 C 2 O 4 = 52 C (V
2 - V 1 masse de C 2 O 4 2 dans l"échantillon : m C 2 O 42 - = n
H 2 C 2 O 4 M C 2 O 4 2 - = 52 . 88 C (V
2 - V 1 · Par simple différence, on peut en déduire la masse d"eau dans l"échantillon : m H 2 O = m - aeèm Fe2 + + m
C 2 O 4 2 - et le nombre de moles d"eau : n H 2 O = m H 2 O M H 2 O = m H 2 O 18· Calcul de x :x = n
C 2 O 4 2 - n Fe 2 +· Calcul de y :y = n
H 2 O n Fe 2 +2.DEUXIÈME MÉTHODE : VOLUMÉTRIE
1 - Expérience
Dissoudre, dans 20 mL de
H 2 SO 42 mol.L
- 1 , environ 120 mg de complexe sec (masse m pesée avec précision). Chauffer légèrement pour le dissoudre. Attention : si on chauffe trop, on risque de favoriser l"oxydation de Fe 2 + en Fe 3 + Titrer avec une solution de permanganate de potassium KMnO 4 (C = 0,0200 mol.L - 1 ). Quand la couleur du permanganate est lente à disparaître, chauffer la solution à 60°C environ, et continuer la titration jusqu"à la persistance de la couleur du permanganate. On note le volume V 3 Ajouter lentement environ de poudre de zinc puis faire bouillir la solution pendant vingt minutes.1128 BULLETIN DE L"UNION DES PHYSICIENS
Synthèse et analyse d"un complexe... B.U.P. n° 785 · Tester une goutte de solution avec une solution de thiocyanate de potassium KSCN (quotesdbs_dbs50.pdfusesText_50[PDF] dosage ph métrique tp
[PDF] dosage potentiométrique d'une solution de sel de mohr
[PDF] dosage potentiometrique equivalence
[PDF] dosage sulfate ferreux par permanganate de potassium
[PDF] dose mais par hectare
[PDF] dose toxique aspirine
[PDF] dossier a fournir campus france guinee
[PDF] dossier a fournir pour le crem
[PDF] dossier a fournir visa france en cote d'ivoire
[PDF] dossier art appliqué bac pro commerce
[PDF] dossier art appliqué bac pro exemple 2012
[PDF] dossier art appliqué bac pro exemple coca cola
[PDF] dossier art appliqué bac pro pdf
[PDF] dossier art appliqué bac pro terminal 2015
