 RÉALISATION ET INTÉGRATION LES TESTS DE
RÉALISATION ET INTÉGRATION LES TESTS DE
dissolution des comprimés. L'élève en apprendra aussi sur différentes professions du secteur des produits pharmaceutiques et biotechnologiques en cherchant ...
 Modélisation de la cinétique de dissolution des comprimes obtenus
Modélisation de la cinétique de dissolution des comprimes obtenus
fond du récipient à distance de la palette. Fig2 Appareil à palettes tournantes Pharma Test PTMS300. 2 . Essai de dissolution. L'essai de dissolution de
 THÈSE
THÈSE
proposer différentes stratégies novatrices de contrôle du test de dissolution de comprimés pharmaceutiques sur la base des principes du QbD. • apporter un
 Sous-traitance et développement pharmaceutique dun médicament
Sous-traitance et développement pharmaceutique dun médicament
9 oct. 2015 Test de dissolution comprimé princeps versus comprimé Physica Pharma ... dissolution des comprimés développés est proche du profil de dissolution ...
 Sécabilité des comprimés et impact sur luniformité de masse
Sécabilité des comprimés et impact sur luniformité de masse
2.6.5 Essai de dissolution Selon la pharmacopée Européenne 7.8 Les comprimés doivent répondre au test de l'uniformité de masse présenté au chapitre 2.9.5 ...
 Etude comparative de la cinétique de dissolution de deux
Etude comparative de la cinétique de dissolution de deux
63789%20%20;%207='%20%20mg%20et%20SOLIAN%20%20200%20mg..pdf
 Présentation PowerPoint
Présentation PowerPoint
6 avr. 2019 • Les tests de dissolution sont indispensables pour caractériser les ... ❖ Plus de 50% des formes sont des comprimés. ❖ L'appareil à palettes ...
 Formulation et caractérisation dune forme buccale mucoadhésive
Formulation et caractérisation dune forme buccale mucoadhésive
dissolution ne sont mentionnés que dans une seule monographie celle du comprimé polymeric systems is complex and it can also depend on the dissolution test ...
 Mémoire Thème
Mémoire Thème
L'essai de dissolution a été fait sur 6 comprimés de chaque lot contrôlé. Pour le test d'uniformité de masse un seul comprimé parmi les comprimés testés s ...
 Optimisation dune formule de comprimés effervescents à base d
Optimisation dune formule de comprimés effervescents à base d
27 août 2021 ... comprimés ou du principe actif lors de la ... Design and evaluation of a rotating filter-stationnary basket in vitro dissolution test.
 Contrôle de Qualité des Comprimés non enrobés : Cas dun
Contrôle de Qualité des Comprimés non enrobés : Cas dun
MOTS CLES: Comprimé non enrobé – Contrôle – Qualité – Test de dissolution – CHAPITRE I: GENERALITES SUR LES COMPRIMES NON ENROBES ET LA ...
 Essais de dissolution et lyodisponibilité Dr. OUAHAB Ammar
Essais de dissolution et lyodisponibilité Dr. OUAHAB Ammar
Dans l'industrie pharmaceutique les tests de dissolution de médicaments sont ont un rôle galénique car ils facilitent la fabrication des comprimés.
 RÉALISATION ET INTÉGRATION LES TESTS DE
RÉALISATION ET INTÉGRATION LES TESTS DE
Au cours de l'activité Les tests de désintégration et de dissolution l'élève sera et ses liens avec la désintégration et la dissolution des comprimés.
 THÈSE
THÈSE
22 juil. 2014 proposer différentes stratégies novatrices de contrôle du test de dissolution de comprimés pharmaceutiques sur la base des principes du QbD.
 THÈSE
THÈSE
proposer différentes stratégies novatrices de contrôle du test de dissolution de comprimés pharmaceutiques sur la base des principes du QbD.
 Pour lObtention du Doctorat en Pharmacie
Pour lObtention du Doctorat en Pharmacie
ANNEE: 2010. THESE N°: 67. Optimisation du test de dissolution a l'aide de la methodologie des plans d'experiences. Cas de l'amlodipine comprimes. THESE.
 Sécabilité des comprimés et impact sur luniformité de masse
Sécabilité des comprimés et impact sur luniformité de masse
2.6 Les tests de la Pharmacopée Européenne pour les comprimés . 2.6.5 Essai de dissolution . ... désagrégation ou dissolution du principe actif.
 APPLICATION DE CERTAINES APPROCHES STATISTIQUES AU
APPLICATION DE CERTAINES APPROCHES STATISTIQUES AU
comprimés à dissolution orale les comprimés à croquer
 Mémoire Thème
Mémoire Thème
2.4 Test de dissolution. Cet essai est destiné à déterminer l'aptitude des comprimés ou capsules à libérer le principe actif dans le milieu liquide de
 Influence des conditions de compression sur les propriétés physico
Influence des conditions de compression sur les propriétés physico
11 août 2006 Dissolution des comprimés des aspirines avec 10 % d'amidon CS. ... un appareil industriel dédié à des tests de dissolution de comprimés.
 [PDF] LES TESTS DE DÉSINTÉGRATION ET DE DISSOLUTION GUIDE
[PDF] LES TESTS DE DÉSINTÉGRATION ET DE DISSOLUTION GUIDE
Ce test analyse en respectant un délai de temps précis si vos comprimés se dégradent complètement lorsqu'ils sont plongés dans une solution semblable à celle
 [PDF] Sécabilité des comprimés et impact sur luniformité de masse
[PDF] Sécabilité des comprimés et impact sur luniformité de masse
Leur teneur en principe actif doit être uniformément répartie dans tout le comprimé et doit répondre à plusieurs tests de la Pharmacopée Européenne Le test d'
 TP 1 Dissolution PDF Spectrophotométrie Médicament générique
TP 1 Dissolution PDF Spectrophotométrie Médicament générique
L'essai de dissolution est un test pharmaco-technique destiné à déterminer le temps que met un comprimé une gélule ou toute autre forme galénique pour
 [PDF] Essais de dissolution et lyodisponibilité Dr OUAHAB Ammar
[PDF] Essais de dissolution et lyodisponibilité Dr OUAHAB Ammar
L'essai de dissolution est un test pharmacotechnique destinée a déterminer la plus au moins grande aptitude des formes galéniques à laisser passer en solution
 [PDF] MEBEVERINE-SAIDAL® comprimé enrobé à 100 mg
[PDF] MEBEVERINE-SAIDAL® comprimé enrobé à 100 mg
Définition : Le dissolutest est un appareil utilisé pour réaliser le test de dissolution in vitro des formes pharmaceutiques orales solides Les pharmacopées
 [PDF] ESSAIS DE DISSOLUTION Et LYODISPONIBILITÉ
[PDF] ESSAIS DE DISSOLUTION Et LYODISPONIBILITÉ
e- Conduite des essais de dissolution e- Les normes de dissolution Comprimés Gélules Granulés L'essai de dissolution est un test pharmacotechnique
 [PDF] Techniques danalyse et contrôle qualité microbiologique et physico
[PDF] Techniques danalyse et contrôle qualité microbiologique et physico
Cet essai est destiné à déterminer l'aptitude des comprimés ou capsules à libérer le principe actif dans le milieu liquide de dissolution et dans les conditions
 [PDF] Etude comparative de la cinétique de dissolution de deux
[PDF] Etude comparative de la cinétique de dissolution de deux
63789%2520%2520%3B%25207%3D'%2520%2520mg%2520et%2520SOLIAN%2520%2520200%2520mg..pdf
 [PDF] Modélisation de la cinétique de dissolution des comprimes - IPCO
[PDF] Modélisation de la cinétique de dissolution des comprimes - IPCO
comprimes obtenus à partir de trois granulométries différentes de PA Un contrôle biopharmaceutique (test de dissolution) a été réalisé Il a
 [PDF] Place des essais de dissolution dans les études de bioéquivalence
[PDF] Place des essais de dissolution dans les études de bioéquivalence
6 avr 2019 · Les tests de dissolution sont indispensables pour caractériser les Plus de 50 des formes sont des comprimés
Comment se dissout un médicament ?
Un test de dissolution utilise un appareil avec des conditions de test spécifiques en combinaison avec des critères d'acceptation pour évaluer la performance du produit . Chapitre général <711> Dissolution comprend 4 appareils standardisés : panier, palette, cylindre alternatif et cellule à circulation.Qu'est-ce qu'un appareil de test de dissolution?
La voie digestive ou entérale correspond à la voie orale. Lorsqu'on avale un comprimé, il arrive dans l'estomac et sa digestion va commencer : le comprimé se délite, se désagrège et se dissout.- Les appareils de dissolution sont utilisés tout au long du cycle de vie du développement du produit, de la sortie du produit aux tests de stabilité et à l'étude des données du produit d'un produit à l'autre . Puis après passage ou approbation du contrôle qualité et de l'assurance qualité, les médicaments sont envoyés sur les marchés.
- La quantité cumulée de médicament libérée sur le graphique temporel représente la libération d'ordre zéro et l'équation est exprimée sous la forme C = K0 t , où K0 est la constante de vitesse d'ordre zéro et t est le temps (en h).
THÈSE
Présentée pour O·RNPHQPLRQ GX grade de :
G2F7(85 G( I·81H9(56ITÉ DE MONTPELLIER 1
ÉCOLE DOCTORALE SCIENCE DES PROCEDES ² SCIENCE DES ALIMENTS UNITE DE RECHERCHE INSTITUT CHARLES GERHARDT DE MONTPELLIERSpécialité : Génie des Procédés
et PHILOSOPHIAE DOCTOR DE L·81H9(56H7e G( 6+(5%ROOKEDEPARTEMENT DE GENIE CHIMIQUE ET BIOTECHNOLOGIQUE
Spécialité : Génie Chimique
parKétsia Yekpe
RELIER LES ATTRIBUTS DE MATÉRIAUX ET LES
PARAMÈTRES DE PROCÉDÉS DE FABRICATION À UN TESTDE CONTRÔLE QUALITÉ,
UNE APPLICATION DU CONCEPT DU QUALITY BY
DESIGN
Soutenue publiquement le 22 Juillet 2014 devant le jury composé de : M. Nadi Braidy, Professeur, UdeS Président du jury M. François Gitzhofer, Professeur, UdeS Rapporteur interne UdeS M. Kamel Daoud, Professeur, USTHB Rapporteur externe M. Michel Perrier, Professeur, Polytechnique Montréal Rapporteur externeM. Nicolas Abatzoglou, Professeur, UdeS Directeur
M. Bernard Bataille, Professeur, UM1 Directeur
M. Ryan Gosselin, Professeur, UdeS Examinateur
M. Xavier Guarric, Professeur, UM1 Examinateur
M. Tahmer Sharkawi, Maître de Conférences, UM1 Examinateur M. Antoine Cournoyer, Superviseur industriel, Pfizer Montréal Membre invité 2Je dédie cette thèse à mes parents
Suzanne et Hermann Yekpe
3Résumé
permettre une libération en temps réel des lots commerciaux. Le QbD propose que la qualitésoit construite dès la conception initiale du médicament plutôt que d'être évaluée à la fin de sa
réalisés après la fabrication des comprimés, peuvent être éliminés si les paramètres qui les
influencent sont contrôlés.En effet, ces tests de contrôle qualité dits traditionnels requièrent en général plusieurs heures
pour leurs préparations et leurs réalisations. Tel est le cas du test de dissolution. Ce test est très
consommateur de ressources matérielles et humaines. La réalisation de stratégies de contrôle
pour les tests de dissolution basée sur une approche QbD pourrait être bénéfique pour
l'industrie pharmaceutique.À travers ce travail, nous avons pu :
proposer différentes stratégies novatrices de contrôle du test de dissolution de comprimés pharmaceutiques sur la base des principes du QbD, apporter un nouvel éclairage sur la compréhension des phénomènes impliqués dans la dissolution de comprimés pharmaceutiques. Les résultats de ce projet de recherche ont permis 1) la mise en évidence des paramètrespréalablement conçu, 3) la corrélation du test de dissolution à des paramètres critiques de
procédés. Imagerie proche infrarouge, Libération en temps réel, Industrie pharmaceutique 4Abstract
With the introduction in 2002 of the concept of Quality by Design (QbD) by the Food and Drug Administration, the pharmaceutical industry intensified efforts and investments to reach real time release of commercial batches, reducing time between manufacturing and availability to the patient. QbD proposes that quality should be built in the initial design of a product rather than being assessed at the end of the tablet manufacturing. Thus, with the QbD initiative, quality control tests of tablets like dissolution testing performed after manufacturing could be removed if the parameters impacting them are controlled. Indeed, quality control tests such as traditional dissolution tests generally require several hours for their preparation and their realizations. Dissolution tests are time consuming, require large amounts of material and human resources. The elimination of these tests through a QbD approach could be beneficial for the pharmaceutical industry.Thanks to this work, it was possible to :
propose different innovative strategies to control the dissolution test of pharmaceutical tablets based on the principles of Quality by Design, have a better understanding of this quality control test. The main results relies on 1) the identification of critical parameters influencing the dissolution test, 2) the development and evaluation of statistical models for the combination of variation of parameters according to an experimental design, 3) the correlation of dissolution test to critical manufacturing process parameters and attributes of materials through process analysis technology. Key words: Quality by Design, Process Analytical Technology, Dissolution Testing, Near Infrared Imaging, Real time release, Pharmaceutical Industry 5Remerciements
Je dédie les premières pages de ma thèse à toutes les personnes qui, de près ou de loin, ont
participé à cette riche aventure. Je remercie tout particulièrement mes directeurs de thèse Pr. Nicolas Abatzoglou, Pr. Bernard avez su trouver un équilibre parfait entre des visions complémentaires. Merci pour votre aide, Je tiens à remercier également mes co-directeurs de thèse Pr. Ryan Gosselin et Pr. TahmerSharkawi pour leur disponibilité, leur grande contribution à ce travail et leurs conseils,
réaliser ma thèse au sein de son équipe. Antoine, merci pour ta supervision, ta disponibilité, tes conseils et nos discussionsAnne-Marie Demers" 0HUŃL à tous !
Un grand merci aux superviseurs, analystes et techniciens du laboratoire de contrôle qualité du
site de Pfizer Montréal pour leur aide, leur gentillesse et leur disponibilité et nos discussions
intéressantes sur le test de dissolution et le Quality by Design ! Je pense particulièrement à
Audrey Massicotte, Marie-France Marcotte, Cathy Gagnon, Marie-Ève Gagnon et Sophie St-Amand.
I would like to thank Fiona Clarke, Lucy Marks and Debbie Hooper from Pfizer Sandwich, UK for your help and support for NIR Imaging analysis. Pharmaceutique de la Faculté de Pharmacie de Montpellier. Merci à Émilie, ma voisine debureau durant mon séjour, pour son aide et nos discussions toujours intéressantes sur le génie
expertise en pharmacie galénique. Merci à Michelle, Jacqueline et Nadine pour leur 6 particulière dans mes souvenirs).relatives à ma cotutelle de thèse. Je pense particulièrement à Mesdames Auclair, Chapdelaine,
Merci à tous les doctorants et maintenant docteurs pour certains rencontrés durant ces quatreannées. Merci pour leur passion qui a su briser tous mes préjugés et me faire comprendre que
chaque doctorat est une aventure riche en expériences. Je pense particulièrement à mes chères
FMQMGM RX MLOOHXUV "
Merci à mes amis de France et du Canada pour vos encouragements, vos sms, vos appels, vos Aurélie, Alimatou, Lorène, Leslie, Aimée, Alda, Lyse, Sonia, Johana, Christian, Éric, Yannick, Clémence, Marcel, Marianne, Malaika et Jeremy. Merci à vous tous. Djou, un grand merci pour ton soutien inconditionnel (pour les goûters de minuit et demi etpour toutes les fois où tu as veillé avec moi !), ce serait trop long pour tout écrire, mais du
IRQG GX Ń°XU : Murakoze, Imana iguhezagire "Un très grand merci à mes parents. Que de temps passé depuis 2004 pour mon premier départ
pour Orsay, moi qui étais triste de cette séparation de quelques dizaines de km, me voilàmaintenant sur un autre continent ! Merci pour tout, pour le soutien infaillible dans les
moments les plus compliqués, pour les encouragements depuis toujours, depuis toujours.sacrifices sont pour moi des exemples. De la " Systématique de la langue Fon » à
Merci j PM V°XU HP PHV IUqUHV Auria, Arnaud et Teddy, à mes cousins de Munich et Montréal, Ghislaine et JD, mes plus grands supporters! Merci à Nadège, Adonis, Cyrille, Audrey, aux vois grandir si vite GH ORLQ" 0HUŃL OM IMPLOOH ŃHV TXHOTXHV OLJQHV QH VXIILURQP SMV j H[SULPHUIl n'y a pas de victoire sans combat
Charles Péguy
7 8Avant-Propos
rocédés (en anglais Process Analytical Technologies : PAT) en génie pharmaceutique.qualité en amont des chaînes de fabrication de différents produits pharmaceutiques. Ces
méthodes permettent de suivre la qualité des produits à chaque étape de leur fabrication et de
corriger rapidement tout écart aux spécifications établies.À travers cet objectif, la Chaire contribue à la formation de personnel hautement qualifié, tant
baccalauréat, de maîtrise et de doctorat, en ce qui concerne la recherche fondamentale, la Le rayonnement de la chaire de recherche est international. En effet, elle collabore, entreautres, avec le département de Pharmacie Galénique et Génie pharmaceutique de la faculté de
et leurs applications pharmaceutiques.Cette thèse se situe dans ce contexte et est réalisée au sein de la Chaire, en cotutelle entre
conformer aux régulations et aux normes actuelles et futures concernant le QbD, en proposantplusieurs éléments de réponses à une problématique liée au test de dissolution. Cette thèse, la
première en son genre, sera un point de départ pour de futures recherches touchant à
Ce projet interdisciplinaire fait appel aux domaines du génie pharmaceutique, de la pharmacie galénique, de la chimiométrie et du génie chimique appliqué aux processus de fabrication pharmaceutique. Il a été réalisé dans les laboratoires suivants : Laboratoires de Contrôle qualité de Pfizer Montréal, Canada Laboratoires de Caractérisation des matériaux de Pfizer Sandwich, Grande-BretagneLe financement de cette thèse a été assuré par le Conseil de Recherches en Sciences Naturelles
9 10Table des matières
RESUME ................................................................................................................................... 3
ABSTRACT .............................................................................................................................. 4
REMERCIEMENTS ................................................................................................................ 5
AVANT-PROPOS .................................................................................................................... 8
TABLE DES MATIERES ..................................................................................................... 10
LISTE DES FIGURES ........................................................................................................... 13
LISTE DES TABLEAUX ...................................................................................................... 15
LISTE DES EQUATIONS ..................................................................................................... 17
LISTE DES ANNEXES ......................................................................................................... 18
LISTE DES PRINCIPAUX ACRONYMES ........................................................................ 19
REALISATIONS SCIENTIFIQUES .................................................................................... 20
INTRODUCTION .................................................................................................................. 22
CHAPITRE I. ÉTAT DE .......................................................................................... 29
I. LA QUALITE DES COMPRIMES PHARMACEUTIQUES .................................... 30I.1. LES COMPRIMÉS PHARMACEUTIQUES ........................................................................................................... 30
I.2. APPROCHE TRADITIONNELLE DU CONTRÔLE QUALITÉ DES COMPRIMÉS PHARMACEUTIQUES ....................... 35
II. UNE NOUVELLE MANIERE DE CONCEVOIR LA QUALITE EN INDUSTRIE PHARMACEUTIQUE, LE QUALITY BY DESIGN ......................................................... 40PHARMACEUTIQUE ............................................................................................................................................. 40
II.2. LES RECOMMANDATIONS DU COMITÉ DE PILOTAGE DE LA CONFÉRENCE INTERNATIONALE SURII.3. LES BÉNÉFICES DE LA MÉTHODE QUALITY BY DESIGN ............................................................................... 45
III. LA DEMARCHE QUALITY BY DESIGN .................................................................. 48
III.1. LA MISE EN PLACE DU QUALITY TARGET PRODUCT PROFILE ...................................................................... 49
III.2. LES ATTRIBUTS CRITIQUES DE QUALITÉ ................................................................................................... 49
III.3. LES ATTRIBUTS DE MATÉRIAUX ET LES PARAMÈTRES DE PROCÉDÉS ....................................................... 49
III.4. ÉVALUATION DES RISQUES ........................................................................................................................ 50
IV. LES PAT, OUTILS ANALYTIQUES IMPORTANTS DU CONCEPT QUALITYBY DESIGN ............................................................................................................................ 52
IV.1. ORIGINE ET INTÉRÊT ................................................................................................................................. 52
IV.2. RÉGLEMENTATION QBD-PAT .................................................................................................................. 53
INFRAROUGE ...................................................................... 61V.1. UN APERÇU DE LA SPECTROSCOPIE PROCHE INFRAROUGE .......................................................................... 61
11 VI. LE TEST DE DISSOLUTION, TEST DE CONTROLE QUALITE DESCOMPRIMES ......................................................................................................................... 74
VI.1. LE RÔLE DU TEST DE DISSOLUTION ........................................................................................................... 74
VI.2. LA FORMULATION PHARMACEUTIQUE ....................................................................................................... 81
VI.3. LES MODÈLES CINÉTIQUES ........................................................................................................................ 82
CHAPITRE II. DEVELOPIE DE CONTROLE POUR
SUPPRIMER LE TEST DE DISSOLUTION ..................................................................... 92
I. INTRODUCTION ........................................................................................................... 93
II. ......................................................................................................... 94
III. METHODOLOGIE ........................................................................................................ 95
IV. DEVELOPPEMENT DE LA STRATEGIE DE CONTROLE................................... 96IV.2. ÉVALUATION DES RISQUES ....................................................................................................................... 96
V. RESULTATS ................................................................................................................. 115
V.1. ÉTUDE DU PROFIL DE DISSOLUTION .......................................................................................................... 115
V.2. MODÉLISATION DES PROFILS DE DISSOLUTION ......................................................................................... 118
V.3.ÉTUDE STATISTIQUE .................................................................................................................................. 121
VI. DISCUSSION ................................................................................................................ 129
VII. CONCLUSION .............................................................................................................. 131
CHAPITRE III. UTILISCHIMIQUE POUR LA
CARACTERISATION DE COMPRIMES ........................................................................ 133
I. INTRODUCTION ......................................................................................................... 134
II. ....................................................................................................... 135
III. METHODOLOGIE ...................................................................................................... 135
IV. MATERIEL ET METHODES ..................................................................................... 138
IV.1. MATIÈRES : PRINCIPE ACTIF ET EXCIPIENTS ............................................................................................ 138
IV.2. PRÉPARATION DES COMPRIMÉS ............................................................................................................... 138
IV.3. TEST DE DISSOLUTION ............................................................................................................................. 140
IV.4. IMAGERIE PROCHE INFRAROUGE (ACQUISITION ET TRAITEMENT DES DONNÉES) ..................................... 140
IV.5. ANALYSE MULTIVARIÉE .......................................................................................................................... 141
V. RESULTATS ET DISCUSSION .................................................................................... 144
V.1. CARACTÉRISATION DES MATIÈRES PREMIÈRES ......................................................................................... 144
V.2. VARIATION DU POURCENTAGE DE KOLLIDON CL (ÉTUDE DES LOTS 1A, 1B, 1C ET 1D) .......................... 148
12V.3. VARIATION DE LA TAILLE DE PARTICULES DE KOLLIDON CL (ÉTUDE DES LOTS 2A ET 2B) ..................... 157
V.4. VARIATION DU POURCENTAGE DE GRANULÉS DE KOLLIDON CL (ÉTUDE DES LOTS 3A ET 3B) ................ 166
V.5. PRÉDICTION DU POURCENTAGE MASSIQUE DE KOLLIDON CL .................................................................. 173
VI. CONCLUSION ............................................................................................................... 176
CONCLUSION GENERALE ET PERSPECTIVES ........................................................ 179ANNEXES ............................................................................................................................. 186
BIBLIOGRAPHIE ............................................................................................................... 194
13Liste des figures
Figure 1 : Processus de fabrication industrielle des comprimés pharmaceutiques .............. 32 Figure 2 : Les différentes possibilités de la fabrication des comprimés (Le Hir, et al.,2009), (Wehrlé, 2012) ......................................................................................... 33
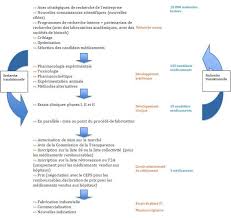
Figure 3 : Développement pharmaceutique primitif (Roché, 2011) .................................... 40
Figure 4 : Productivité des plus grandes industries pharmaceutiques (AstraZeneca, Bristol-Myers Squibb, Eli Lilly, GlaxoSmithKline, Merck, Novartis, Pfizer, Roche and Sanofi-Aventis) de 2005 à 2010 combinée aux approbations de nouveaux médicaments en fonction des dépenses Recherche et Développement (Bernstein, 2011) ................................................. 42 Figure 5 : Application du guide CIH Q8 au développement pharmaceutique ..................... 44 Figure 6 : Interaction entre la gestion de risque qualité et le Quality by Design, figuremodifiée de (Caire, 2011) .................................................................................... 48
contrôle ................................................................................................................ 51
Figure 8 : Spectre électromagnétique .................................................................................. 62
Figure 9 : Illustration des chemins optiques suivis par la lumière au contact d'unéchantillon (adaptée de Gendrin, 2008) .............................................................. 63
Figure 10 : Nombre de publications concernant l'imagerie proche infrarouge par lamaison d'édition Elsevier au 1er octobre 2013 ..................................................... 66
Figure 11 : Cube de données générées pour l'obtention d'une image chimique ................... 67
Figure 12 : Les trois différentes approches pour l'obtention d'image chimique : (a) le point mapping, (b) le line mapping et (c) le global imaging ............................... 67Figure 13 : Principe de l'analyse en composantes principales (Gendrin, 2008) .................... 69
Figure 14 : Les phases du cheminement d'un médicament (Canal-Raffin, 2007) ................. 75Figure 15 : Rôle du test de dissolution in vivo ...................................................................... 76
Figure 16 : Représentations des appareils de dissolution 1 et 2 ............................................ 78
Figure 17: Principaux phénomènes après administration de formulations variées (excepté suspensions, comprimés orodispersibles, effervescents et capsulesliquides) ............................................................................................................... 80
Figure 18 : Test de dissolution comme reflet de la complexité pharmaceutique deproduits finis (Scheubel, 2010) ........................................................................... 82
Figure 20 : Différents styles de sondes pour le système de dissolution avec fibre optique, (a) rode probe, (b) arch probe, (c) shaft probe (Lu, et al., 2003) ......... 88ISPE de Davis Bruce (Bruce , 2009) ................................................................... 94
Figure 22 : Diagramme d'Ishikawa ........................................................................................ 97
Figure 23 : Dissolution du principe actif/ désintégration du comprimé .............................. 104
Figure 24 : Schéma récapitulatif des essais ......................................................................... 113
Figure 25 : Pourcentage de dissolution en fonction du temps à 3 pH différents ................. 116
Figure 26 : Valeurs des coefficients de détermination pour les modèles cinétiques auxpH 6,4, 6,8 et 7,2 ............................................................................................... 119
14 Figure 27: Valeurs des constantes de dissolution k1 pour les 13 lots aux pH 6,4, 6,8 et7,2 ...................................................................................................................... 120
Figure 28 : Valeurs des temps de demi-vie T50 pour les 13 lots aux pH 6,4, 6,8 et 7,2 ...... 120 Figure 29 : Les diagrammes de Pareto au temps de test de 10 minutes aux pH 6,4, 6,8et 7,2 .................................................................................................................. 124
actif .................................................................................................................... 134
Figure 31 : Étapes permettant la réalisation des comprimés ............................................... 137
Figure 32 : Schéma des expériences conduisant à l'obtention d'images chimiques,adapté de (Clarke, 2004) ................................................................................... 140
Figure 35 : Distribution de taille de particules du Kollidon CL .......................................... 146
Figure 36 : Analyse au Microscope électronique à balayage de la poudre commercialedu Kollidon CL .................................................................................................. 147
Figure 37 : Analyse au Microscope électronique à balayage de la poudre commercialedu Kollidon CL (zoom) ..................................................................................... 147
Figure 38 : Analyse au Microscope électronique à Balayage du KolCL (125-2D0 ȝP ..... 148 Figure 39 : Analyse au Microscope électronique à Balayage du KolCL (355-42D ȝP ..... 148 Figure 40 : Profils de dissolution (points) et modélisation (lignes pointillées) des lots1A, 1B, 1C et 1D ............................................................................................... 149
surface de comprimé échantillonnée ................................................................. 154
Figure 42 : Histogramme de distribution des tailles de particules pour 3 comprimés dulot 1B ................................................................................................................. 155
Figure 43 : Histogramme de distribution des tailles de particules pour 3 comprimés dulot 1C ................................................................................................................. 155
Figure 44 : Histogramme de distribution des tailles de particules pour 3 comprimés dulot 1D ................................................................................................................. 156
Figure 45 : Profils de dissolution (points) et modélisation (lignes pointillées) des lots2A et 2B ............................................................................................................ 158
Figure 46: Exemples de mauvais critères de détermination pour la comparaisonstatistique des images chimiques ....................................................................... 162
Figure 47 : Méthode pour obtenir des images chimiques contenant uniquement lesgranulés ............................................................................................................. 163
Figure 48 : Démarche utilisée pour la comparaison statistique ........................................... 165
Figure 49 : Profils de dissolution (points) et modélisation (lignes pointillées) des lots3A, 3B, 3C et 1C ............................................................................................... 167
15Liste des tableaux
Tableau 1 : Avantages et inconvénients liés à la fabrication et l'utilisation decomprimés ............................................................................................................. 35
Tableau 2 : Les tests de contrôle qualité des comprimés pharmaceutiques ............................. 37
Tableau 3 : Liste des principaux médicaments dont le brevet expire en 2011 (et chiffres de vente aux États-Unis) (Pharmactua.com, 2011) .................................. 43 Tableau 4 : Comparaison entre la méthode traditionnelle et le Quality by design (CIHQ8 (R2), 2009) ...................................................................................................... 46
Tableau 5 : Avantages et inconvénients de l'application du concept Quality by Design (Rathore, et al., 2009), (Kourti, et al., 2012), (DPT Laboratories, 2013) ............. 47Tableau 6 : Avantages des PAT ............................................................................................... 53
Tableau 7 : Outils PAT appliqués aux étapes unitaires pharmaceutiques ................................ 59
pharmaceutiques. ................................................................................................... 61
quotesdbs_dbs41.pdfusesText_41[PDF] préformulation et formulation d'un médicament
[PDF] quelle vision de la guerre ces trois textes présentent ils
[PDF] conditions sink galénique
[PDF] test de dissolution pharmacopée européenne
[PDF] formule de l'accélération
[PDF] résolution de problèmes 4ème
[PDF] équation allométrique définition
[PDF] allométrie définition
[PDF] oeuvre in situ de daniel buren
[PDF] formule brute du sorbitol
[PDF] formule semi développé de l'acide lactique
[PDF] pyruvate formule
[PDF] butanol formule
[PDF] formule semi développée isomère c4h10o
