 Exercice : La bouteille magique Corrigé
Exercice : La bouteille magique Corrigé
1- Équation de la réaction modélisant la transformation chimique entre le glucose et la solution de bleu de méthylène. 1-1) Définitions :.
 Activité expérimentale n°2 : LE LIQUIDE MAGIQUE
Activité expérimentale n°2 : LE LIQUIDE MAGIQUE
Le schtroumpf curieux vient de dérober la recette d'un liquide magique chez Gargamel chimie arrive à le réaliser. Faire valider ce protocole par le professeur ...
 Exercice : La bouteille magique
Exercice : La bouteille magique
Exercice : La bouteille magique. D'après épreuve de BAC Terminale S Afrique 2008. 2008-2009. Au cours d'une séance de travaux pratiques un élève de terminale
 CHAPITRE 9 : QUANTITÉ DE MATIERE TP1 : LA BOUTEILLE
CHAPITRE 9 : QUANTITÉ DE MATIERE TP1 : LA BOUTEILLE
Le schtroumpf curieux vient de dérober la recette d'un liquide magique chez Gargamel. Page 2. Doc 2 : quelques définitions de cours. ➢ Une mole est un « ...
 CORRIGE
CORRIGE
1 août 2020 La pression dans la bouteille est égale à 370 bars si tout le CO2 qu ... Exercice 5 : Un exemple de valorisation de CO2. CO2(g) + 4 H2(g) ...
 TP15 La chimie du liquide magique
TP15 La chimie du liquide magique
de glucose. LE PROTOCOLE À SUIVRE pour réaliser le liquide magique est donc le suivant : Lorsque la bouteille est agitée le dioxygène qui se trouve dans l' ...
 BACCALAURÉAT GÉNÉRAL PHYSIQUE-CHIMIE
BACCALAURÉAT GÉNÉRAL PHYSIQUE-CHIMIE
Chez le nourrisson les ions nitrate (NO3. -) sont incriminés dans la survenue de la méthémoglobinémie (ou maladie bleue). La formation des ions nitrite
 Exercice 10. La bouteille de butane
Exercice 10. La bouteille de butane
Tous les gaz seront assimilés à des gaz parfaits. Une bouteille de gaz pour usage domestique contient 130 kg de butane C4H10 partiellement liquéfié. La
 La chimie verte adaptée aux exercices et aux expériences
La chimie verte adaptée aux exercices et aux expériences
La chimie verte appliquée aux expériences. La soi-disant “expérience de la bouteille bleue” (dont sont décrites un grand nombre de variantes. 4. ) peut être
 Mes premières expériences de chimie
Mes premières expériences de chimie
Fixe la bouteille n°1 sur la bouteille n°2 avec du scotch. Au fond de la - Découvrir la craie magique. 9. Pour aller. Page 10. 10. 15. Extrait de : « Le Labo ...
 Exercice : La bouteille magique Corrigé
Exercice : La bouteille magique Corrigé
1- Équation de la réaction modélisant la transformation chimique entre le glucose et la solution de bleu de méthylène. 1-1) Définitions :.
 Exercice : La bouteille magique
Exercice : La bouteille magique
Exercice : La bouteille magique. D'après épreuve de BAC Terminale S Afrique 2008. 2008-2009. Au cours d'une séance de travaux pratiques
 CHIMIE Partie I : Chimie et Magie – La bouteille magique
CHIMIE Partie I : Chimie et Magie – La bouteille magique
Dans la suite on s'intéresse plus particulièrement au tour de la « bouteille magique ». A grands renforts de mise en scène
 Activité expérimentale n°2 : LE LIQUIDE MAGIQUE
Activité expérimentale n°2 : LE LIQUIDE MAGIQUE
Le schtroumpf curieux vient de dérober la recette d'un liquide magique chez Gargamel. 1. AIDONS LE SCHTROUMPF CURIEUX… chimie arrive à le réaliser.
 TP : La bouteille magique : correction
TP : La bouteille magique : correction
Calcul de la masse de n= 6.10-2 mol d'HYDROXYDE DE SODIUM. Formule du composé ionique à l'état solide NaOH. Masse molaire M= 23+16+1=40 g/mol.
 La chimie verte adaptée aux exercices et aux expériences
La chimie verte adaptée aux exercices et aux expériences
Le terme de chimie verte (ou durable) renvoie vers une façon de pratiquer la La soi-disant “expérience de la bouteille bleue” (dont sont décrites un ...
 Exercice 10. La bouteille de butane
Exercice 10. La bouteille de butane
La constante des gaz parfaits vaut : R = 831 J?mol-1?K-1. Tous les gaz seront assimilés à des gaz parfaits. Une bouteille de gaz pour usage domestique
 Appendice: réponses aux exercices
Appendice: réponses aux exercices
littérature 6. le droit 7. l'informatique 8. la chimie. B. A2. Appendice: réponses aux exercices. Chapitre 2. UNIVERSITÉ DE CAEN.
 Français interactif
Français interactif
Students also categorize vocabulary in the “Chassez l'intrus” exercises. Phonetics la chimie chemistry l'informatique (f) ... 1 bouteille de vin rouge.
 TP15 La chimie du liquide magique
TP15 La chimie du liquide magique
LE PROTOCOLE À SUIVRE pour réaliser le liquide magique est donc le suivant : Lorsque la bouteille est agitée le dioxygène qui se trouve dans l'air de ...
 [PDF] Exercice : La bouteille magique Corrigé
[PDF] Exercice : La bouteille magique Corrigé
Exercice : La bouteille magique D'après épreuve de BAC Terminale S Afrique 2008 Corrigé 2008-2009 1- Équation de la réaction modélisant la
 [PDF] Exercice : La bouteille magique
[PDF] Exercice : La bouteille magique
Exercice : La bouteille magique D'après épreuve de BAC Terminale S Afrique 2008 2008-2009 Au cours d'une séance de travaux pratiques
 Exercice : La bouteille magique - Yumpu
Exercice : La bouteille magique - Yumpu
12 juil 2015 · Le glucose est noté RCHO (aq) Sa masse molaire vaut M = 180g mol -1 Couples oxydant/réducteur mis en jeu :• BM + (aq)/BMH (aq)• O 2(g) /H 2 O
 Exercice III La bouteille magique (4 pts)
Exercice III La bouteille magique (4 pts)
1 1 Un oxydant est une espèce chimique capable de capter un ou plusieurs électrons Un réducteur est exercices corriges pdf
 Travaux pratiques sur la bouteille magique - correction - Docsity
Travaux pratiques sur la bouteille magique - correction - Docsity
Télécharge Travaux pratiques sur la bouteille magique - correction et plus Exercices au format PDF de Chimie sur Docsity uniquement!
 Travaux pratiques sur la bouteille magique Exercices Chimie
Travaux pratiques sur la bouteille magique Exercices Chimie
Télécharge Travaux pratiques sur la bouteille magique et plus Exercices au format PDF de Chimie sur Docsity uniquement! Afrique 2008 EXERCICE III
 [PDF] Activité expérimentale n°2 : LE LIQUIDE MAGIQUE
[PDF] Activité expérimentale n°2 : LE LIQUIDE MAGIQUE
Le schtroumpf curieux vient de dérober la recette d'un liquide magique chez Gargamel 1 AIDONS LE SCHTROUMPF CURIEUX chimie arrive à le réaliser
 La bouteille magique - Labolycée
La bouteille magique - Labolycée
Bac S 2003-2012Tronc communChimieLa transformation d'un système chimique est-elle toujours rapide ? Durée 52 minutes 2008 Centres étrangers
 Examen corrige TS Chimie La bouteille magique Exercice résolu
Examen corrige TS Chimie La bouteille magique Exercice résolu
s p a c e 1re s physique manuel de l eleve pdf 250 exercices corriges de svt exercices de chimie 1ère eurin gié 1ère s et e page 155 corriges du livre
 [PDF] CHIMIE Partie I - La bouteille magique - Concours Agro Veto
[PDF] CHIMIE Partie I - La bouteille magique - Concours Agro Veto
Dans la suite on s'intéresse plus particulièrement au tour de la « bouteille magique » A grands renforts de mise en scène le magicien prépare une solution
1ere SExercice : La bouteille magique
D'après épreuve de BAC Terminale S Afrique 2008Corrigé2008-2009
1- Équation de la réaction modélisant la transformation chimique entre le glucose et la
solution de bleu de méthylène.1-1) Définitions :
Un oxydant est une espèce chimique capable de capter un ou plusieurs électrons. Un réducteur
est une espèce chimique capable de céder un ou plusieurs électrons.1-2) Demi-équation de réduction de la forme oxydée du bleu de méthylène :
BM+(aq) + H+(aq) + 2e- = BMH(aq)
1-3) Demi-équation d'oxydation du glucose :
RCHO(aq) + H2O = RCOOH(aq) + 2H+ + 2e-
1-4) En déduire l'équation de la réaction d'oxydoréduction :
BM+(aq) + H+(aq) + 2e- = BMH(aq)
RCHO(aq) + H2O = RCOOH(aq) + 2H+ + 2e-
BM+(aq) + H+(aq) +RCHO(aq) + H2OBMH(aq) + RCOOH(aq) + 2H+BM+(aq) + RCHO(aq) + H2OBMH(aq) + RCOOH(aq) + H+
2- Interprétation des observations :
2-1) Équation de la réaction d'oxydoréduction entre le dioxygène et la forme réduite du bleu de
méthylène : oxydation de BMH : BMH(aq) = BM+(aq) + H+(aq) + 2e- ×2 réduction de O2 : O2(aq) + 4H+(aq) + 4e- = 2H2O(l)2BMH(aq) + O2(aq) + 4H+(aq) 2BM+(aq) + 2H+(aq) + 2H2O(l)
2BMH(aq) + O2(aq) + 2H+(aq) 2BM+(aq) + 2H2O(l)
2-2) Interprétation des observations :
Le glucose dissout dans la solution, réduit le bleu de méthylène au cours d'une réaction qui est
lente, c'est pour cela qu'on observe une lente décoloration de la solution.Lorsque l'on agite le flacon, ou dissout le dioxygène présent dans la bouteille dans le solution et
il va oxyder la forme réduite du bleu de méthylène, ce qui explique l'apparition de la coloration
bleue (BMH réapparaît).3- Étude quantitative :
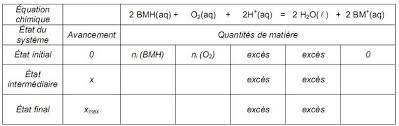
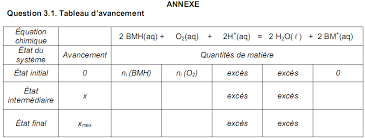
3-1) Tableau d'avancement :
ni(BMH) - 2xni(O2) - x2x ni(BMH) - 2xmaxni(O2) - xmax2xmax3-2) Quantité de matière initiale ni(O2) :
On a niO2=VO2
Vm =48×10-324,0Soit ni(O2) = 2,0×10-3 mol
3-3) Calcul de la quantité de matière ni(BMH) susceptible de réagir :
La quantité de matière ni(BMH) susceptible de réagir est telle que d'après le tableau
d'avancement on a : ni(BMH) - 2xmax = ni(O2) - xmax = 0 Soit xmax=niBMH2=niO2Soit
niBMH=2×niO2D'oùni(BMH) = 4,0×10-3 mol3-4) En déduire la quantité de glucose n(RCHO) ayant réagit avec le bleu de méthylène :
Tableau d'avancement de la réaction 1 :
BM+(aq) + RCHO(aq) + H2OBMH(aq) + RCOOH(aq) + H+État initialni(BM+)ni(RCHO)excès00
État intermédiaireni(BM+) - xni(RCHO) - xexcèsXx État finalni(BM+) - xmaxni(RCHO) - xmaxexcèsxmaxxmaxOn en déduit donc qu'à l'état final :
ni(RCHO) - xmax = 0où ni(RCHO) est la quantité de glucose ayant réagit. On en déduit donc que ni(RCHO) = xmax = ni(BMH)Soitni(RCHO) = 4,0×10-3 mol
3-5) Calcul de la masse de glucose n'ayant pas réagit :
Calculons la masse de glucose ayant réagit :
m(RCHO) = n(RCHO) × M(RCHO) = 4,0×10-3 × 180 = 7,2×10-1 g Sachant que l'on a introduit 5,0g de glucose dans l'erlenmeyer on en déduit que la masse de glucose n'ayant pas réagit vaut : m'(RCHO) = 5,0 - 7,2×10-1 m'(RCHO) = 4,3 gLe glucose a donc été introduit en large excès puisque 86% en masse du glucose introduit n'a
pas réagit.quotesdbs_dbs22.pdfusesText_28[PDF] conservation de l'eau potable
[PDF] durée conservation eau distillée
[PDF] combien de temps peut on conserver de l eau distillée
[PDF] conservation eau demineralisee
[PDF] expérience évaporation de l'eau
[PDF] combien de temps peut on conserver de l'eau en bouteille
[PDF] eau stérile conservation
[PDF] 20 expériences avec l'eau et la glace
[PDF] images séquentielles glaçon qui fond
[PDF] a quelle temperature fond un glacon
[PDF] ballon de stockage eau glacée
[PDF] a quelle température la glace fond elle
[PDF] dimensionnement ballon tampon eau glacée
[PDF] exercice fonte d un glaçon
