 Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
Exercice 3 : On prépare une solution tampon de pH = 45 à partir d'acide acétique CH3COOH (pKa = 4
 Fiche dexercices sur les acides bases et pH (fiche n°11)
Fiche dexercices sur les acides bases et pH (fiche n°11)
Pour cela on peut ajouter à l'eau des solutions qui font augmenter ou diminuer le pH. On fait une dilution. Corrigé 5. 1) On parle de pluies acides car le pH ...
 ACIDES et BASES solutions aqueuses acides et solutions aqueuses
ACIDES et BASES solutions aqueuses acides et solutions aqueuses
Calculer la concentration molaire des trois espèces ioniques. Exercice 2 : Une solution a un pH = 126. Elle contient les ions hydronium
 CORRECTION EXERCICES sur SOLUTIONS AQUEUSES - pH
CORRECTION EXERCICES sur SOLUTIONS AQUEUSES - pH
CORRECTION EXERCICES sur SOLUTIONS AQUEUSES - pH. EXERCICE 1 : 1.) Pour un mélange on écrit chaque dissolution séparément : CuSO4. →. Cu. 2+. +. SO4. 2–.
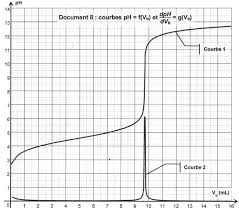 Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
solution S d'ibuprofène a le même comportement qu'une solution aqueuse. ... Le document 2 montre l'évolution du pH de la solution S lorsqu'on ajoute une solution ...
 F2School
F2School
Corrigés des exercices. Table des matières. Table des matières a) Quel serait le pH d'une solution aqueuse d'hydroxyde de potassium de même concentration ?
 Exercice 2 : « Concentration en soluté et pH ».
Exercice 2 : « Concentration en soluté et pH ».
Exercice 2 : « Concentration en soluté et pH ». On prépare une solution aqueuse acide avec 063 g d'acide nitrique (HNO3) dissous dans 1000 mL d'eau.
 Corrigé exercice 22 - LE ZIRCONIUM EN SOLUTION AQUEUSE
Corrigé exercice 22 - LE ZIRCONIUM EN SOLUTION AQUEUSE
Pour discuter de la stabilité du zirconium vis-à-vis du solvant eau on trace le diagramme potentiel-pH de l'eau et on le superpose à celui du zirconium. Couple
 pH dune solution aqueuse
pH dune solution aqueuse
Masse molaire de soluté en g/mol. Page 2. nombre de moles en mol. concentration en mol/L c = V n. Volume en L. Exercice :
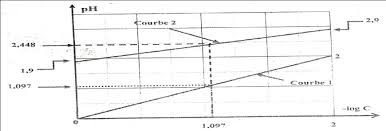 Série chimie : PH des solutions aqueuses
Série chimie : PH des solutions aqueuses
Série chimie : PH des solutions aqueuses. 4 éme M-SC exp. Exercice N° 1. On dispose de deux solutions aqueuses (S1) et (S2) de même concentration molaire C>10.
 Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
Corrigé- Série 2- Travaux dirigés de Chimie des Solutions
quantité de CH3COOH en mg à ajouter est donnée par : Exercice 3 : On prépare une solution tampon de pH = 45 à partir d'acide acétique CH3COOH (
 Cours et exercices de chimie des solutions
Cours et exercices de chimie des solutions
Dans le cas des solutions aqueuses suffisamment diluées la molarité et la Le pH mesure l'acidité ou la basicité d'une solution et non la force de ...
 F2School
F2School
Acides-bases 14 : Calcul du pH des solutions d'un acide ou d'une base dans Quelles sont les particules en présence dans une solution aqueuse d'acide ...
 Fiche dexercices sur les acides bases et pH (fiche n°11)
Fiche dexercices sur les acides bases et pH (fiche n°11)
Exercice 1. Deux élèves mesurent le pH d'un soda ils trouvent un pH de 1. 1) Le sucre permet-il de rendre une solution moins acide ?
 td corriges biochmv 2014-2015.pdf
td corriges biochmv 2014-2015.pdf
EXERCICE 1 : Calculer le pH des solutions suivantes: EXERCICE 3 : a) Déterminer le pHi approximatif de solutions aqueuses d'acide.
 COURS DE CHIMIE GENERALE Semestre 1 SVI
COURS DE CHIMIE GENERALE Semestre 1 SVI
Constantes d'acidité et de basicité. 1.6. Coefficient de dissociation d'un acide faible : 2. CALCUL DE PH DES SOLUTIONS AQUEUSES. 2.1. Cas d'
 Exercices et problèmes de chimie générale
Exercices et problèmes de chimie générale
Corrigés des exercices . CHAPITRE 5 ? SOLUTIONS AQUEUSES DE COMPOSÉS IONIQUES ... 7.1 pH de solutions d'un monoacide fort ou d'une monobase forte.
 Série chimie : PH des solutions aqueuses
Série chimie : PH des solutions aqueuses
Série chimie : PH des solutions aqueuses. 4 éme M-SC exp. Exercice N° 1. On dispose de deux solutions aqueuses (S1) et (S2) de même concentration molaire C>
 ANNALES SCIENCES PHYSIQUES Terminale D
ANNALES SCIENCES PHYSIQUES Terminale D
Chapitre 2: Les solutions aqueuses de chlorure d'hydrogène et pH des solutions diluées pour lesquelles 10 -14 mol.L-1< ... Exemples d'épreuves corrigées.
 20 - Lecture diagramme E-pH chlore
20 - Lecture diagramme E-pH chlore
Transformations en solution aqueuse. Exercice 20. Page 1 sur 4. Corrigé exercice 20. LECTURE DU DIAGRAMME = (PH) DE LsÉLÉMENT CHLORE.
Corrigé exercice 20
LECTUREDUDIAGRAMME���=���
PHDEL'ÉLÉMENTCHLORE
Entoutpoint,onpeutappliquer:2
Cl HClO ClO Cl g avecledichloredissousCl aq ;danscet1) Ondéterminelenombred'oxydationduchloredanslesquatreespècesapparaissantdansle
estuncoupleacido-basiquedeBrønsted: n.o. pH +IHClO/ClO 0Cl -ICl ClA:HClO
B:Cl C:Cl D:ClO2) Onutilisel'ordonnéeàl'originedesfrontières1et2,lesvaleursétantclairementindiquéessur
lediagrammefourni.FrontièreA/BàpH=0:
CoupleHClO/Cl
:2HClO+2H +2��� =Cl +2H O log HClO H ClÀpH=0,onprend
H =1(ils'agitenfaitdel'activité).Àlafrontière
HClO 5$ =2 Cl 5$ (convention"égalitéenatomes»)et HClO 5$ +2 Cl 5$ (autresespècesnégligeables),donc HClO 5$ 6 et Cl 5$ 6 7Donc���
5$ pH=0 =1,56V=���° log��� 1,56V 2 log��� =1,59VFrontièreB/CàpH=0:
CoupleCl
/Cl :Cl +2��� =2Cl log Cl ClÀlafrontière2
Cl 5$ Cl 5$ Cl 5$ Cl (autres espècesnégligeables),donc Cl 5$ 6 et Cl 5$ 6 7Donc���
5$ =1,42V=���° log 6 log��� 1,42V 2 log��� =1,39VPourdéterminer���°
8 et���°CoupleHClO/Cl
:HClO+H +2��� =Cl +H O 8 log HClO H Cl 2 log HClO H Cl 2 log Cl Cl 8 2 log HClO H Cl donne:2���=���°
2 log HClO H Cl +���°log HClO H Cl =2���° 8 +���°log HClO H ClOnadoncétabli:���°
=2���° 8 ,d'où: 8 2 =1,49V3) Ils'agitd'uncoupleacido-basiquedeBrønsted,caractériséparsaconstanted'acidité���
H ClO HClO HClO 5$ Cl 5$ donc��� H 5$ .Onlitdonc: p��� =pH 5$9 =7,54) Pourlafrontière1,onreprendl'équationcorrespondantàHClO/Cl
établieàlaquestion2,la
concentrationdeH n'étantmaintenantplusfixée: 5$, 2 log��� 2 log H 2 log��� -���°pHétablieàlaquestion2,la
concentrationdeH n'étantmaintenantplusfixée: 5$8 8 2 log H 8 2 pHPourlafrontière4,lecoupleestClO
/Cl ,dedemi-équationClO +2��� +2H =Cl +H O,la formuledeNernstdonne���=���° 7 log ClO H Cl .Àlafrontière, ClO 5$ Cl 5$ ,donc: 5$7 7 2 log H 7 -���°pH5) B=A+Cestlaréactiondedismutationdudichloreenmilieuacide.Onl'obtienten
soustrayantlesdemi-équationsdeCl /Cl etdeHClO/Cl etendivisantpar2poursimplification: Cl +HO=HClO+Cl
+H aundomainedestabilité.Enrevanche,auxpHplusélevés,Cl
HClO Cl H Cl 2 log HClO H Cl 2 log Cl Cl 2 log ���°=10 =10 "8,8 =4,6⋅10 "7 aupHstandard(pH=0).6) L'eaudejavelcontientdesconcentrationsapportéeségalesdeClO
etCl ,tellesqueleur sommeestégaleà��� =0,10mol⋅L .Donc��� ClO Cl =0,05mol⋅L OrClO ClO +HO=HClO+HO
Apporté0,050
Équilibre≈0,05������
(concentrationsenmol⋅LOntrouveàl'équilibre:
0,05Donclaconcentrationd'équilibredeHO
vaut: HO0,05���
=1,3⋅10 "7 mol⋅L peuavancée.Onendéduit
H HO =8,0⋅10 mol⋅L ⇒pH=-log H =10,1.L'eaudejavelaunpHde10,1.
d'équilibre���=1,11V. 7 ,onpeutparexemple utiliser���=���° 8 log HClO H Cl 8 log H 6 Cl =1,11V.L'eaudejavelaunpotentielde1,11V.
hypochloriteClO enconcentrationélevée.7) Lorsd'unexcèsd'acidefort,ilseproduiraitlaréactionquasi-totaleClO
+H =HClO,puisleDanscesconditions,HClOetCl
HClO+Cl
+H =Cl +H O libéréedansl'atmosphèreselon: Cl aq =Cl g jamaisacidifierdel'eaudejavel!8) Onreportelepoint(pH=10,1;���=1,11V)surlediagrammepotentiel-pHdufer(voir
OH 8Ons'attenddoncàl'oxydationdesionsFe
selon: Fe +3HO =Fe OH 8 s×(2)
ClO +2��� +H O=Clquotesdbs_dbs18.pdfusesText_24[PDF] exercices corrigés physique pcsi pdf
[PDF] exercices corrigés physique seconde forces et principe d'inertie
[PDF] exercices corrigés physique terminale s ondes
[PDF] exercices corrigés physique terminale s pdf
[PDF] exercices corrigés physique terminale sti2d
[PDF] exercices corrigés poo c# pdf
[PDF] exercices corrigés primitives terminale s pdf
[PDF] exercices corrigés probabilité 1es
[PDF] exercices corrigés probabilité universitaire
[PDF] exercices corrigés probabilités conditionnelles terminale s
[PDF] exercices corrigés probabilités terminale bac pro
[PDF] exercices corrigés probabilités terminale s
[PDF] exercices corrigés probabilités variables aléatoires discrètes
[PDF] exercices corrigés produit vectoriel pdf
