 CORRIGE-MOTEUR-A-COMBUSTION-INTERNE-ZERGANE.pdf
CORRIGE-MOTEUR-A-COMBUSTION-INTERNE-ZERGANE.pdf
Exercice N°1 (7.5 Pts). Donner la définition et le rôle des composants du moteur à combustion interne suivants: - Système bielle-manivelle …
 Untitled
Untitled
SOLUTION D'EXERCICE 01 (chaque réponse par 01 pts pour 12 pts) Corrigé-type d'Examen de moteur à combustion interne approfondie_2ème année Master Energétique.
 Sujet final
Sujet final
Exercice 1: Un tuyau de cuivre de rayon intérieur R1 de rayon Le moteur à explosion est un moteur à combustion interne dont l'allumage est commandé.
 Cours et exercices résolus De la Thermodynamique Appliquée
Cours et exercices résolus De la Thermodynamique Appliquée
Exercice corrigé du chapitre III. 36. Exercice 01 : Un gaz subit un cycle de On appelle moteur à combustion interne les moteurs où la combustion se produit à.
 Eléments de correction
Eléments de correction
RENDEMENT D'UN MOTEUR ESSENCE A COMBUSTION INTERNE. (Du moteur idéal au moteur réel). Eléments de correction. Le sous-système. Un moteur 4 cylindres fonctionne
 Exercice 4 physique
Exercice 4 physique
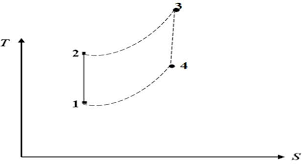
On considère un moteur à combustion interne à allumage par bougies. On se limite à l'étude de l'un des cylindres du moteur. Le cycle thermodynamique décrit par
 Untitled
Untitled
MOTEURS À. COMBUSTION INTERNE. ÉPREUVE : ÉTUDE DES MOTEURS. US1 - EXPLOITATION D'ESSAIS MOTEUR. Corrigé N°03ED13. 6 pages. Page 2. Partie : A. Etude
 Corrigé Examen ME911 Master 2 Energétique
Corrigé Examen ME911 Master 2 Energétique
https://ft.univ-tlemcen.dz/assets/uploads/2019-2020/S1/EXAM/NOTES/GM/Corrige/1/M2_ENERG_ME911_Corrige%CC%81.pdf.pdf
 Thermodynamique Appliquée
Thermodynamique Appliquée
Exercices corrigés………………………………………………. 136. Références bibliographiques Le moteur à explosion est un moteur à combustion interne dont l'allumage est commandé.
 SERIE DEXERCICES 25 : THERMODYNAMIQUE : PREMIER
SERIE DEXERCICES 25 : THERMODYNAMIQUE : PREMIER
Série d'exercices 25. 1. SERIE D Exercice 13 : étude du cycle de Lenoir. Un des premiers moteurs à combustion interne fonctionne de la manière suivante :.
 ????????? ????????? ??????????? ??????? Peoples Democratic R
????????? ????????? ??????????? ??????? Peoples Democratic R
Corrigé type - Moteur à combustion interne - L3- Construction Mécanique-S6-2019/2020. Exercice N°1. - Une liaison entre le piston et l'arbre du moteur
 CYCLES THERMODYNAMIQUES DES MACHINES THERMIQUES
CYCLES THERMODYNAMIQUES DES MACHINES THERMIQUES
V.4.6 Application au cas de la combustion dans un moteur . Les machines thermiques `a combustion interne peuvent revêtir des formes tr`es différentes ...
 Sujet final
Sujet final
Le moteur Diesel est un moteur à combustion interne dont l'allumage n'est pas commandé par des éclateurs mais une compression élevée. L'air et le carburant sont
 SERIE DEXERCICES 25 : THERMODYNAMIQUE : PREMIER
SERIE DEXERCICES 25 : THERMODYNAMIQUE : PREMIER
Exercice 4 : travail reçu par un gaz pour différents chemins suivis. Un des premiers moteurs à combustion interne fonctionne de la manière suivante :.
 ÉTUDE DES MOTEURS U52 – ÉTUDE ET ANALYSE DES MOTEURS
ÉTUDE DES MOTEURS U52 – ÉTUDE ET ANALYSE DES MOTEURS
U52 – ÉTUDE ET ANALYSE DES MOTEURS. Durée : 3h Coefficient : 3. Corrigé N° 05ED14. 15 pages. BREVET DE TECHNICIEN SUPÉRIEUR. MOTEURS À COMBUSTION INTERNE.
 Energie: ressources consommation
Energie: ressources consommation
https://cel.archives-ouvertes.fr/cel-01844243/document
 Exercices de Thermodynamique
Exercices de Thermodynamique
m3.mol?1) et l'énergie interne molaire U (en kJ.mol?1) de la vapeur d'eau à la puis l'air traverse une chambre de combustion (Cb) où il subit un ...
 Le moteur thermique Transformer lénergie chimique en énergie
Le moteur thermique Transformer lénergie chimique en énergie
chimique grâce à une combustion interne. Fig1 .fonction du moteur. Le moteur thermique reçoit de l'essence combustible du système d'alimentation.
 TD N°4 Exercice N°1 Aide simple Solution détaillée
TD N°4 Exercice N°1 Aide simple Solution détaillée
TD N°4. Exercice N°1. Le moteur à explosion est un moteur à combustion interne dont l'allumage est commandé par des éclateurs (bougies).
 polycopie page de garde-finale-3
polycopie page de garde-finale-3
I-11-5 Exercice 5. 29. CHAPITRE II. LES MOTEURS A COMBUSTION INTERNE. (MCI). II – 1 Introduction. 30. II – 2 Différents types de cycles et de moteur.
Exercices de Thermodynamique
" Ce fut la grande tâche et la grande gloire de la physique du XIX esiècle d"avoir ainsi considérablement précisé et étendu en tous sens notre connais- sance des phénomènes qui se jouent à notre échelle. Non seulement elle a continué à développer la Mécanique, l"Acoustique, l"Optique, toutes ces grandes disciplines de la science classique, mais elle a aussi créé de toutes pièces des sciences nouvelles aux aspects innombrables : la Thermodynamique et la science de l"Électricité. » LouisDe Broglie(1892-1987) -Matière et Lumière, exposés généraux sur la physique contemporaine, 1(1937) ?Syst`emes thermodynamiques T1? Soit une mole d"un gaz occupant une volumeVmsous la pressionPet `a la temp´eratureT.1)On suppose que ces grandeurs sont li´ees par l"´equation :?
P+a V2m? (Vm-b) =RT, o`ua,betRsont des constantes. Utiliser les propri´et´es d"intensivit´e ou d"extensivit´e des grandeurs pour
´etablir l"´equation correspondante relative `anmoles.2)Mˆeme question pour l"´equation :P(Vm-b) exp?a
RTVm? =RT. On consid`ere du sable fin dont chaque grain occupe un volumeV0= 0,1mm3. Quel est le volume Voccup´e parN= 6.1023grains? Si on ´etendait uniform´ement ce sable sur la France(d"aire S= 550000km2) quelle serait la hauteur de la couche de sable? ?Consid´erations `a l"´echelle microscopique T1? ???Ex-T1.3Vitesse de lib´eration et vitesse quadratique moyenne1)Calculer num´eriquement `a la surface de la Terre et de la Lune, pour une temp´erature
T= 300K, la vitesse de lib´erationvlet la vitesse quadratique moyenne pour du dihydrog`ene et du diazote. Commenter. Donn´ees :Constante de gravitationG= 6,67.10-11uSI. Rayon terrestreRT= 6,4.106m; masse de la TerreMT= 6.1024kg. Rayon lunaireRL= 1,8.106m; masse de la LuneML= 7,4.1022kg. Masses molaires :M(H2) = 2g.mol-1etM(N2) = 28g.mol-1.Constante desGP:R= 8,314J.K-1.mol-1.
2)Quel devrait ˆetre l"ordre de grandeur de la temp´eratureTpour que le diazote, constituant
majoritaire de l"atmosph`ere terrestre, ´echappe quantitativement `a l"attraction terrestre? R´ep : 1)Pour l"expression de la vitesse de lib´erationÜCf Cours de M´ecaniqueetDSn05: v l,T?11,2km.s-1etvl,L?2,3km.s-1. de plus :vq(H2)?1,9km.s-1etvq(N2)?0,5km.s-1.2)Il faudraitTT≂100000K(!)
1)calculer le nombre de mol´ecules parcm3dans un gaz parfait `a 27◦Csous une pression de
10 -6atmosph`ere.2)Calculer le volume occup´e par une mole d"un gaz parfait `a latemp´erature de 0◦Csous la
pression atmosph´erique normale. En d´eduire l"ordre de grandeur de la distance moyenne entre mol´ecules.Exercices de Thermodynamique2008-2009
Solution Ex-T1.1
1)CommeVm=Vn, on a :
P+a V2m? (Vm-b) =RT??P+n2aV2??
Vn-b? =RT? P+n2a V2? (V-nb) =nRT Rq :on peut ´ecrire l"´equation d"´etat sous la forme? P+A V2? (V-B) =nRTen posantB=nb etA=n2a. Best une grandeur extensive puisqu"elle est additive, sin=n1+n2,B=nb=n1n+n2b= B1+B2.Aest aussi une grandeur extensive, mais elle n"est pas additive car sin2a?=n21a+n22a.
2)P(V-nb)exp?na
RTV? =nRT.Solution Ex-T1.2
Le volume occup´e estV=N.v= 6.1013m3= 6.1016L(60 millions de milliards de litres!) . Ce sable ´etal´e surS= 5,5.105km2= 5,5.1011m2formerait une couche de hauteurh=VS?110m
Solution Ex-T1.3
1)D"apr`es l"´equation d"´etat du gaz parfait, le nombre de mol´ecules par unit´e de volume est
n ?=N V=PkBT?10-6.1,01325.1051,38.10-23×300?2,5.1019mol´ecules par m`etre cube soitn??2,5.1013 mol´ecules parcm3ou encoren??4.10-11mol.cm-3.2)Le volume molaire cherch´e est :Vm=RT
V=8,314×273,151,013.105= 22,4.10-3m3= 22,4L.
?Mod´elisations de gaz r´eelsT1? ???Ex-T1.4Dioxyde de carbonePour le dioxyde de carbone (" gaz carbonique »), les coefficientsaetbde l"équation d"état deVan
der Waalsont pour valeurs respectives0,366kg.m5.s-2.mol-2et4,29.10-5m3.mol-1. On place deux moles de ce gaz dans une enceinte de volumeV= 1Là la température deT= 300K.Q :Comparer les pressions données par les équations d"état du gaz parfait et du gaz deVan der
Waals, la valeur exacte étantP= 38,5bars.
Rép :PGP=nRT
V?4,99.106Pa, soit une erreur relative de?
?P-PGP P? ?≈30%;PVdW= nRTV-nb-n2aV2?3,99.106Pa, soit une erreur relative de? ?P-PVdW P? ?≈4%. Le modèle du gaz parfait est donc inacceptable, tandis que le modèle du gaz deVan der Waalsmontre une bien meilleure précision. ???Ex-T1.5Deux r´ecipients Un récipient(A)de volumeVA= 1L, contient de l"air àtA= 15◦Csous une pressionPA=72cmHg.
Un autre récipient(B)de volumeVB= 1L, contient également de l"air àtB= 20◦Csous une pressionPB= 45atm.On réunit(A)et(B)par un tuyau de volume négligeable et on laisse l"équilibre se réaliser à
t= 15◦C. On modélise l"air par un gaz parfait de masse molaireM= 29g.mol-1.Données :le "centimètre de mercure» est défini par la relation1atm= 76cmHg= 1,013.105Pa.Q :Quelle est la pression finale de l"air dans les récipients? Quelle est la masse d"air qui a été
transférée d"un récipient dans l"autre? Indications :Exprimer, initialement, les quantités de matièrenAetnBdans les récipients. Endéduire la quantité de matière totale. L"état final étant un état d"équilibre thermodynamique,
2http ://pcsi-unautreregard.over-blog.com/qadripcsi@aol.com
2008-2009Exercices de Thermodynamique
les variables intensives sont uniformes, dont la densité moléculaire etla pression. En déduire les
quantités de matière finalesnAFetnBF.Rép :mB→A= 26,1getP?22,5bars?22,2atm.
???Ex-T1.6Point critique et ´equation r´eduite d"un gaz de Van der Waals (*)1)Une mole de gaz deVan der Waalsa pour équation d"état :?
P+a V2? (V-b) =RT ExprimerPen fonction deTetVet calculer les dérivées partielles :?∂P ∂V? T et?∂2P∂V2? T2)Montrer qu"il existe un unique état C tel que :?∂P
∂V? T = 0et?∂2P∂V2? T = 0. Déterminer son volume molaireVC, sa températureTCet sa pressionPC.3)On poseθ=T
TC,ν=VVCet?=PPC.
Montrer que l"équation d"état liantθ,νet?est universelle, c"est à dire qu"elle ne fait plus
intervenir aucune constante dépendant du gaz.Rép : 1)?∂P
∂V? T =-RT(V-b)2+2aV3et?∂2P∂V2? T =2RT(V-b)3-6aV4 2)C? VC= 3b;TC=8a
27Rb;PC=a27b2?
-3)? ?+3ν2? (ν-1) = 8θ ???Ex-T1.7Mod´elisations d"un gaz r´eel (*)1)Le tableau ci-dessous donne avec trois chiffres significatifs exacts le volume molaireV(en
m3.mol-1) et l"énergie interne molaireU(enkJ.mol-1) de la vapeur d"eau à la température
t= 500◦Cpour différentes valeurs de la pressionP(enbars). On donne en outre la constante des GP :R= 8,314J.K-1.mol-1.P110204070100
U56,3356,2356,0855,7755,4754,78
Justifier sans calcul que la vapeur d"eau ne se comporte pas comme unGP. On se propose d"adopter le modèle deVan der Waalspour lequel on a, pour une mole de gaz : P+a V2? (V-b) =RTetU=UGP(T)-aV.Calculer le coefficientaen utilisant les énergies internes des états àP= 1baret àP= 100bars.
Calculerben utilisant l"équation d"état de l"état àP= 100bars. Quelle valeur obtient-on alors pourUàP= 40bars? Quelle température obtient-on alors en utilisant l"équation d"état avecP= 40barsetV= 1,56.10-3m3.mol-1?
Conclure sur la validité de ce modèle.
2)On réalise une détente isochore (ie à volume constant) d"une mole de vapeur d"eau de l"état
initialI{tI= 500◦C;PI= 100bars}jusqu"à l"état finalF{TF=?;PF= 70bars}. Le tableau ci-dessous donne le volume molaireV(enm3.mol-1) et l"énergie interne molaireU (enkJ.mol-1) de la vapeur d"eau sousP= 70barspour différentes valeurs de la températuret (en ◦C). t300320340360380400U47,3048,3849,3250,1750,9651,73
Déterminer la température finaleTFet la variation d"énergie interneΔU=UF-UI. qadripcsi@aol.comhttp ://pcsi-unautreregard.over-blog.com/3Exercices de Thermodynamique2008-2009
Rép : 1)UH2O(g)ne vérifie pas la première loi deJoule:H2O(g)ne se comporte pas comme un gaz parfait. Modélisation deVdW:a= 9,23.10-1J.m-3.mol-1etb= 8,2.10-5m3.mol-1.2)TF= 599KetΔU=UF-UI=-6,1kJ.mol-1.
?Coefficients thermo´elastiques et phases condens´ees T1? ???Ex-T1.8Gaz de Van der Waals Une mole de dioxyde de carboneCO2obéit à l"équation deVan der Waals:? P+a V2? (V-b) =RT, oùVest le volume molaire du gaz.
Déterminer le coefficient de dilatation à pression constanteαen fonction des variables indépen-
dantesTetV, des constantesa,bet deR. Retrouver son expressionαGPdans le cas d"un gaz parfait.Rép :a=R
-2aV2(V-b) +RTVV-bet on vérifie quelim a→0 b→0α=1T=αGP.
???Ex-T1.9Gaz de JouleUne mole de gaz deJouleobéit à l"équation d"état :P(V-b) =RT, oùVest le volume molaire
du gaz.Déterminer le coefficient de compressibilité isothermeχTen focntion des variables indépendantes
V,P, etb.
Retrouver son expressionχT,GPdans le cas d"un gaz parfait. Exprimer l"écart relatif :χT-χT,GP
χT,GP.
Comparer les compressibilité d"un gaz deJouleet d"un gaz parfait.Rép :χT=?
1-b V?1Pet on vérifie quelim
b→0χT=1P=αGP.T-χT,GP
χT,GP=-bV<0→; donc le gaz de Joule est moins compressible que le gaz parfait. ???Ex-T1.10Eau liquideUne mole d"eau liquide est caractérisée dans un certain domaine de températures et de pressions
autour de l"état 0 où{P0= 1bar;T0= 293K;V0= 10-3m3}, par un coefficient de dilatation isobareα= 3.10-4K-1et par un coefficient de compressibilité isothermeχT= 5.10-10Pa-1 constants.1)Établir que l"équation d"état liantV,PetTde ce liquide est :
ln VV0=α(T-T0)-χT(P-P0)
2)Calculer son volume molaire sousP= 1000barset àT= 293K. Commenter.
3)Une mole d"eau liquide est enfermée dans une bouteille métallique de volumeV0constant.
Par suite d"un incendie, la température passe deT0= 293KàT= 586K. Calculer la pressionPdans le récipient et commenter. Reprendre le calcul pour un gaz parfait et commenter.Rép : 2)V= 9,51.10-4m3soit?
?ΔV V0? ?= 5%.3)P=P0+α(T-T0)χT= 1,8.103bar: cette
pression est très élevée : la bouteille risque d"exploser.4http ://pcsi-unautreregard.over-blog.com/qadripcsi@aol.com
2008-2009Exercices de Thermodynamique
?" Atmosphère! atmosphère!... »T2? ???Ex-T2.1Masse de l"atmosph`ere On travaille avec le modèle d el"atmosphère isotherme avecT= 290K. Le champ de pesanteur est supposé uniforme (g= 9,8m.s-2) et l"air est assimilé à un gaz parfait de masse molaire M= 29g.mol-1. On noteP0= 105Pala pression de l"air au niveau du sol (z= 0) et on choisit un axe verticalOzascendant.1)retrouver la loi du nivellement barométriqueP(z)pour l"atmosphère isotherme. À quelle
altitudez1la pression vaut-elleP02?A.N.
2)En supposant cette loi valable dez= 0à " l"infini » calculer la masseMatmde l"atmosphère
et faire l"application numérique avecRT= 6400km.quotesdbs_dbs4.pdfusesText_7[PDF] exercices corrigés moteur a courant continu
[PDF] exercices corrigés moyenne 4ème
[PDF] exercices corrigés ms dos
[PDF] exercices corrigés multiplexeur demultiplexeur pdf
[PDF] exercices corrigés nombre dérivé
[PDF] exercices corrigés nombres complexes math sup
[PDF] exercices corrigés nombres complexes mpsi pdf
[PDF] exercices corrigés nombres complexes terminale sti2d
[PDF] exercices corrigés nombres complexes type bac pdf
[PDF] exercices corrigés nombres réels mpsi
[PDF] exercices corrigés nombres réels pdf
[PDF] exercices corrigés nombres réels seconde
[PDF] exercices corrigés nomenclature 1ere s
[PDF] exercices corrigés nomenclature alcanes
