 FICHE TECHNIQUE
FICHE TECHNIQUE
bactériologie alimentaire pour le dénombrement des bactéries aérobies dans les produits alimentaires les produits Ensemencement en surface (NF EN ISO 4833-2) ...
 Lamothe-Abiet
Lamothe-Abiet
bactéries. Pour de plus amples informations consulter notre fiche en ligne des « bonnes pratiques de l'ensemencement des bactéries lactiques ». Dose d ...
 Lamothe-Abiet
Lamothe-Abiet
bactéries. Pour de plus amples informations consulter notre fiche en ligne des « bonnes pratiques de l'ensemencement des bactéries lactiques ». Dose d ...
 Ensemencement en surface pour antibiogramme Étape préliminaire
Ensemencement en surface pour antibiogramme Étape préliminaire
Cette bactérie est responsable d'infections transmises par voie oro-digestive. Étape préliminaire. Préparation o du poste de travail o des matériels
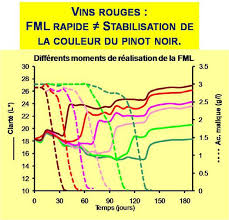 MATINEE TECHNIQUE - Gestion de la fermentation malolactique
MATINEE TECHNIQUE - Gestion de la fermentation malolactique
Des mesures de clarté sur des vins ensemencés en bactéries lactiques sélectionnées à différents moments montrent que l'ensemencement bactérien précoce n'est
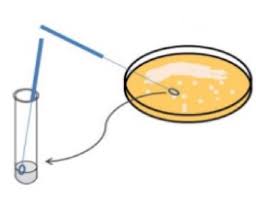 TP3 de microbiologie (L 2): Méthodes densemencement préparé
TP3 de microbiologie (L 2): Méthodes densemencement préparé
alimentaire ou biologique ou culture bactérienne) et votre nouveau milieu de culture. à l'aide d'une « pipette Pasteur »ou anse de platine ou écouvillonnage. •.
 Souche de bactéries lactiques pour lensemencement des vins à
Souche de bactéries lactiques pour lensemencement des vins à
REFLEXMALO®HD est une culture starter lyophilisée d'Oenococcus oeni pour la fermentation malolactique. Cette souche de bactérie lactique a été sélectionnée
 LA CO -INOCULATION LEVURES -BACTÉRIES :
LA CO -INOCULATION LEVURES -BACTÉRIES :
Si moment du levurage est bien positionné celui de l'ensemencement bactérien peut donc être discuté. Classiquement
 III. — Milieux de culture et ensemencements
III. — Milieux de culture et ensemencements
Restait ensuite à choisir une méthode d'ensemencement et un milieu de culture en vue de l'analyse quantitative de ces bactéries. Dans la littérature les
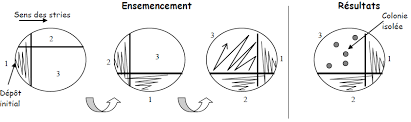 TP n°2 : Techniques densemencement et disolement des
TP n°2 : Techniques densemencement et disolement des
-Plonger l'anse dans la suspension bactérienne réalisée à partir d'une colonie que l'on veut identifier ou confirmer. -Prendre une goutte de la suspension. -On
 TP n°2 : Techniques densemencement et disolement des
TP n°2 : Techniques densemencement et disolement des
TP n°2 : Techniques d'ensemencement et d'isolement des microorganismes -Plonger l'anse dans la suspension bactérienne réalisée à partir d'une colonie ...
 LA CO -INOCULATION LEVURES -BACTÉRIES :
LA CO -INOCULATION LEVURES -BACTÉRIES :
Si moment du levurage est bien positionné celui de l'ensemencement bactérien peut donc être discuté. Classiquement
 III. — Milieux de culture et ensemencements
III. — Milieux de culture et ensemencements
Restait ensuite à choisir une méthode d'ensemencement et un milieu de culture en vue de l'analyse quantitative de ces bactéries. Dans la littérature les
 Souche de bactéries lactiques pour lensemencement des vins à
Souche de bactéries lactiques pour lensemencement des vins à
REFLEXMALO®HD est une culture starter lyophilisée d'Oenococcus oeni pour la fermentation malolactique. Cette souche de bactérie lactique a été sélectionnée
 Travaux pratiques de microbiologie générale
Travaux pratiques de microbiologie générale
L'ensemencement c'est-à-dire le transport des bactéries dans un milieu de culture neuf
 Aide mémoire (microbiologie) Ensemencement dune gélose-cor-JT
Aide mémoire (microbiologie) Ensemencement dune gélose-cor-JT
Ensemencement stérile à partir d'une plaque de Petri 5) Déposer l'anse sur une région de la gélose qui n'a pas de bactéries. Ceci permettra.
 SIMMONS CITRATE 61834 64834 IVD
SIMMONS CITRATE 61834 64834 IVD
Les bactéries capables d'utiliser le citrate de sodium comme seule source de n'apporter aucun élément nutritif dans le milieu lors de l'ensemencement.
 Manuel des Travaux Pratiques de Bactériologie
Manuel des Travaux Pratiques de Bactériologie
Ensemencement et mise en culture des bactéries……………………… 11. 9. Préparation et utilisation des milieux de culture………………………… 12.
 TD 1 : Les différents types de milieux de culture.
TD 1 : Les différents types de milieux de culture.
Ensemencement ou inoculation en microbiologie : introduire un inoculum bactérien dans un milieu de culture stérile (bouillon ou gélose ect.)
 Bactérie œnologique Oenococcus oeni à ensemencement direct
Bactérie œnologique Oenococcus oeni à ensemencement direct
Bactérie œnologique Oenococcus oeni à ensemencement direct sélectionnée par l'Institut Français de la Vigne et du Vin (IFV)
 TP n°2 : Techniques d’ensemencement et d’isolement des
TP n°2 : Techniques d’ensemencement et d’isolement des
>TP n°2 : Techniques d’ensemencement et d’isolement des WebTechniques d’ensemencement Avant toute manipulation il faut rassembler tout le matériel dont on a besoin On l’organise de façon à les avoir dans la zone stérile (à proximité du
 TD 03 : Techniques d’ensemencement et d’isolement des bactéries
TD 03 : Techniques d’ensemencement et d’isolement des bactéries
>TD 03 : Techniques d’ensemencement et d’isolement des bactéries WebTD 03 : Techniques d’ensemencement et d’isolement des bactéries -Introduction Les microorganismes coexistent en populations mélangées dans les différents
 Travaux pratiques de microbiologie générale
Travaux pratiques de microbiologie générale
>Travaux pratiques de microbiologie généraleWeb- Ensemencement par incorporation A partir de la dilution 10-5transvaser stérilement 1 ml dans une boite de Pétri vide et stérile ; verser dessus le contenu d’un tube de gélose en
 Traitement des prélèvements en Bactériologie - Infectiologie
Traitement des prélèvements en Bactériologie - Infectiologie
>Traitement des prélèvements en Bactériologie - InfectiologieWebBactériémietransitoire(saufencasd’endocarditebactériémie continue) Corrélationsensibilité etvolumedesangrecueilli Généralement2à 3sériesd’hémocultures24h(espacede30à
 Les techniques d’ensemencements et les examens
Les techniques d’ensemencements et les examens
>Les techniques d’ensemencements et les examens WebLes techniques d’ensemencements et les examensmacroscopiques des cultures bactériennes Objectifs : * Connaître les techniques d’ensemencement (GN GNi BN)
Comment mettre en évidence les bactéries dans leur intégralité ?
Les méthodes mettant en évidence les bactéries dans leur intégralité sont basées principalement sur les techniques de microscopie en l’absence de coloration (l’état frais), ou après coloration, et sur les techniques de culture sur milieu artificiel.
Quels sont les différents types d’ensemencement sur boites?
Il existe plusieurs techniques d’ensemencement sur boites : 1er Isolement ou épuisement : -C’est la technique des 4 quadrants qui consiste à disperser le microorganisme à la surface d’un milieu solide afin d’obtenir des colonies séparées, ainsi permet de retrouver
Quel est le risque de contamination en cas d’ensemencement de plusieurs échantillons dans le même milieu de culture ?
Analyse et interprétation des résultats : D’après les résultats obtenus, et les réponses à la question (N°08), 75% des techniciens pensent qu’il n’y a pas de risque de contamination en cas d’ensemencement de plusieurs échantillons dans le même milieu de culture, 25% ne donnent aucune réponse.

Rédigé par : BELMESSIKH A. et MERGOUD L.
Manuel des travaux pratiques de Microbiologie générale 2 èmeannée LMD 1TP n°2 des microorganismes
1. Principe
tout seul pas suffisant pour caractériser et identifier un germe. Pour ulture.-Ensemencer : consiste à déposer un microorganisme dans un milieu de culture neuve et stérile.
-Milieu de culture : est une préparation permettant aux microorganismes de se multiplierrapidement en grand nombre. Il doit donc satisfaire les exigences nutritives du germe étudié.
(apporte la source : de de facteurs de croissance, pH voisin du pH ). -Selon leurs consistances les milieux de culture se divisent en deux types :Â Le milieu de culture liquide = le bouillon
 Le milieu de culture solide = le bouillon + agar-agar (gélose) --agar ou la gélose :possédant des propriétés permettant son utilisation pour solidifier (gélifier) les milieux de culture
des germes : températures basses forme un gel transparent plus ou moins solide selon la est pas dégradée par les microorganismes. Les germes se développent parfaitement dans les milieux de culture liquide mélange. Ce qui implique les microorganismes. Par contre, les milieux de culture solides permettent une croissance des germes avec fixation sousforme des colonies microbiennes séparées, ce qui facilite leur isolement et par conséquent leur
purification et identification. Les milieux de culture solides sont utilisés alors pour microbien. -Colonie microbienne : ensemble de cellules identiques issues de la même cellule microbienne mère. - Isoler : consiste à séparer les divers microorganismes poly microbien. - Souche pure s par boite de Pétri . 2.Rédigé par : BELMESSIKH A. et MERGOUD L.
Manuel des travaux pratiques de Microbiologie générale 2 èmeannée LMD 2 3. de façon à les avoir dans la zone stérile (à proximité du bec). Selon visé, on utilisera différentes techniques :3.1. Ensemencement dans le tube
a) Ensemencement dans le tube de bouillon -Devant le bec, prendre le tube contenant les microorganismes dans la main gauche, déboucher le et garder le bouchon -Plonger identifier ou confirmer. -Prendre une goutte de la suspension. -On la retire sans toucher les parois du tube, contient une bulle de suspension avec des germesinoculum. -E - tube de bouillon neuf et stérile (après flambage de son col). -O toute la hauteur afin de répartir la suspension dans tout le milieu. -Ref -Repasser le fil de platine à la flamme en le portant au rouge. -Incuber le tube ensemencé .Remarque :
 On prendra en garde à conserver tout les objets dans la zone stérile du bec bunsen et de ne
jamais les faire entrer en contact avec la paillasse. Les bouchons des tubes seront passés à la flamme du bec avant et après toute manipulation,
tout comme les instruments. Pipette Pasteur :
La pipette est passée rapidement dans la flamme. Aspirer le bouillon de culture.
Ensemencer dans les tubes sans souffler.
Rédigé par : BELMESSIKH A. et MERGOUD L.
Manuel des travaux pratiques de Microbiologie générale 2 èmeannée LMD 3 b) Ensemencement dans le tube étroit de gélose en culotIl est ensemencé grâce à une pipette Pasteur en réalisant un mouvement hélicoïdal du fond
vers la surface, la suspension bactérienne est libérée progressivement. (test type respiratoire)
c) Ensemencement dans le tube de gélose en culot piqure centrale une pipette Pasteur boutonnée, après avoir préalablement chargé celle-ci de suspension bactérienne. (test metaboloique) d) Ensemencement dans le tube de gélose inclinée (pente) On utilise de suspension selon le procédé décrit pour le milieu liquide. On réalise des stries espacées sur toute la longueur de la pente en commençant par le fond du tube et en remontant. (conservation du microorganisme) e) Ensemencement dans le tube de gélose semi-inclinée (culot + pente) Le culot est classiquement ensemencé par piqure centrale par pipette Pasteur boutonnée et la pente par stries selon le principe de la gélose inclinée. (test type respiratoire)3.2. Ensemencement dans la boite de Pétri (contient le milieu de culture solide)
a) Ensemencement en masse (en profondeur) -Incorporer 1 ml de suspension microbienne dans la boite de Pétri vide. -Faire couler le milieu de culture en surfusion (45°C). - Faire homogénéiser les germes avec toute la masse du milieu. - Laisser solidifier puis incuber. b) Ensemencement en double couche -Faire couler une première couche 15ml du milieu de culture et laisser solidifier. -Déposer 1 ml de la suspension des germes et ensemencer par étalement. -deuxième couche 5ml du milieu de culture en surfusion (45°C).quotesdbs_dbs2.pdfusesText_3[PDF] encg casa inscription
[PDF] encg casa inscription 2017
[PDF] encg casa logo
[PDF] encg casa master
[PDF] encg casa partenariat
[PDF] encg casa passerelle s5
[PDF] encg casablanca
[PDF] encg dakhla inscription
[PDF] encg dakhla passerelle s5
[PDF] encg dakhla seuil
[PDF] encg date d'inscription
[PDF] encg formation avis
[PDF] encg jadida
[PDF] encg kenitra 2017
