 Contrôle n° 3 de Sciences Physiques
Contrôle n° 3 de Sciences Physiques
Un atome de soufre possède 16 charges positives. Il peut facilement former un ion sulfure en gagnant 2 électrons. a) Quel est le numéro atomique de l'atome de
 Reproduire et compléter le tableau suivant : Symbole Nombre de
Reproduire et compléter le tableau suivant : Symbole Nombre de
Donner la composition de l'atome de soufre sachant que Z = 16 et A = 32 Donner la structure électronique de l'ion de cet élément sachant qu'il possède.
 Le SOUFRE et les MINÉRAUX SULFURÉS
Le SOUFRE et les MINÉRAUX SULFURÉS
Oxydation indirecte des sulfures par les ions ferriques (Fe3+) cubique et possède la composition chimique suivante: Mn2+S. Il se.
 Synthèse et caractérisation de sulfures de métaux de transition
Synthèse et caractérisation de sulfures de métaux de transition
1 janv. 2018 La pyrite de composition Fe2+(S2)2- peut insérer jusqu'à 4 ions lithium par unité formulaire avec une capacité massique très importante de ...
 CHAPITRE 1 LA MATIÈRE
CHAPITRE 1 LA MATIÈRE
d) Montrer que la masse est concentrée dans le noyau. Composition atomique a) D'après la classification périodique. Le numéro atomique de l'atome de soufre est
 Détermination de la composition isotopique du soufre pour létude
Détermination de la composition isotopique du soufre pour létude
29 mai 2017 la formation d'ions sulfures se produit simultanément au ... bio-corrosion et l'utilisation de la composition isotopiques du soufre pour la ...
 DS SCIENCES PHYSIQUES MATHSPÉ
DS SCIENCES PHYSIQUES MATHSPÉ
20 févr. 2009 Combien la maille dessinée contient-elle d'ions sulfure . ... Un mélange gazeux sortant d'un four a la composition molaire suivante: 8% de ...
 Détermination de la composition isotopique du soufre pour létude
Détermination de la composition isotopique du soufre pour létude
1 févr. 2017 la formation d'ions sulfures se produit simultanément au processus de dissolution anodique du fer la précipitation de phases de sulfures de ...
 Activité sulfatique dans les bétons consécutive à loxydation des
Activité sulfatique dans les bétons consécutive à loxydation des
Suivant la composition de la phase liquide en de sulfures de fer dans les granulats sur la durabi- ... Enfin
 Formule dun cristal ionique dune solution et équation de dissolution
Formule dun cristal ionique dune solution et équation de dissolution
I - Les principaux ions. Les ions monoatomiques sont issus d'un seul atome qui a gagné ou perdu un ou plusieurs électrons. ion sulfure. S2- ion fer II.
 Sulfure - Wikipédia
Sulfure - Wikipédia
L'ion sulfure est S2? un anion qui a une charge de ?2 En solution aqueuse ce n'est qu'à un pH alcalin (pH élevé) que les ions sulfure sont présents en
 [PDF] Le sulfure (sous forme de H2S) - Santé
[PDF] Le sulfure (sous forme de H2S) - Santé
Généralités Le soufre est un corps non métallique Ses valences les plus courantes sont –2 +4 et +6; le degré d'oxydation –2 est connu sous le nom de
 [PDF] Reproduire et compléter le tableau suivant : Symbole Nombre de
[PDF] Reproduire et compléter le tableau suivant : Symbole Nombre de
Donner la composition de l'atome de soufre sachant que Z = 16 et A = 32 Donner la structure électronique de l'ion de cet élément sachant qu'il possède
 [PDF] Soufre-et-sulfurespdf - Club de Minéralogie de Montréal
[PDF] Soufre-et-sulfurespdf - Club de Minéralogie de Montréal
L'ALABANDITE ou alabandine est un rare sulfure de manganèse Il cristallise dans le système cubique et possède la composition chimique suivante: Mn2+S Il se
 [PDF] CHAPITRE 1 LA MATIÈRE
[PDF] CHAPITRE 1 LA MATIÈRE
a) À l'aide de la classification périodique précédente donner la composition exacte de l'atome de soufre 32 b) Calculer la masse du noyau de soufre 32 c)
 [PDF] Tableau de certains ions polyatomiques Formules Constantes et
[PDF] Tableau de certains ions polyatomiques Formules Constantes et
Constantes et conversions Solubilité des composés ioniques dans l'eau à 25 °C Ions - 1 Ions - 2 Ions - 3 Formule Nom Formule Nom Formule Nom
 [PDF] Synthèse et caractérisation de sulfures de métaux de transition
[PDF] Synthèse et caractérisation de sulfures de métaux de transition
La pyrite de composition Fe2+(S2)2- peut insérer jusqu'à 4 ions lithium par unité formulaire avec une capacité massique très importante de 894 mAh g-1
 [PDF] Rôle des espèces sulfures sur le comportement dun acier non allié
[PDF] Rôle des espèces sulfures sur le comportement dun acier non allié
16 avr 2012 · fois des ions SO4 2- et HCO3 - à la concentration de 003 mol L -1 Enfin les interactions entre sulfures et produits de corrosion ont
 [PDF] Nouveaux Sulfures Complexes pour Application Batteries au Lithium
[PDF] Nouveaux Sulfures Complexes pour Application Batteries au Lithium
22 oct 2019 · Impact de la concentration en LiOH sur la composition Les batteries au lithium et en particulier les batteries Li-ion connaissent
Comment S'est formé l'ion sulfure ?
Les ions du soufre en solution aqueuse
Les ions sulfure, de formule S2-, sont des ions monoatomiques qui peuvent se former par dissolution du sulfure d'hydrogène (H2S) dans l'eau.Quelle est la composition du soufre ?
Le symbole chimique du soufre est S, l'atome de soufre porte le numéro atomique 16. Sa masse atomique est de 32,065 u et sa masse volumique de 2,07g/cm-3. Il s'agit d'un métal jaune faisant partie du groupe des chalogènes, il est insoluble dans l'eau.Quelle est la structure électronique de l'ion sulfure ?
Exercice2 : soufre
Sa structure électronique est donc : (K)2(L)8(M)6.- L'ion sulfure est S2?, un anion qui a une charge de ?2.
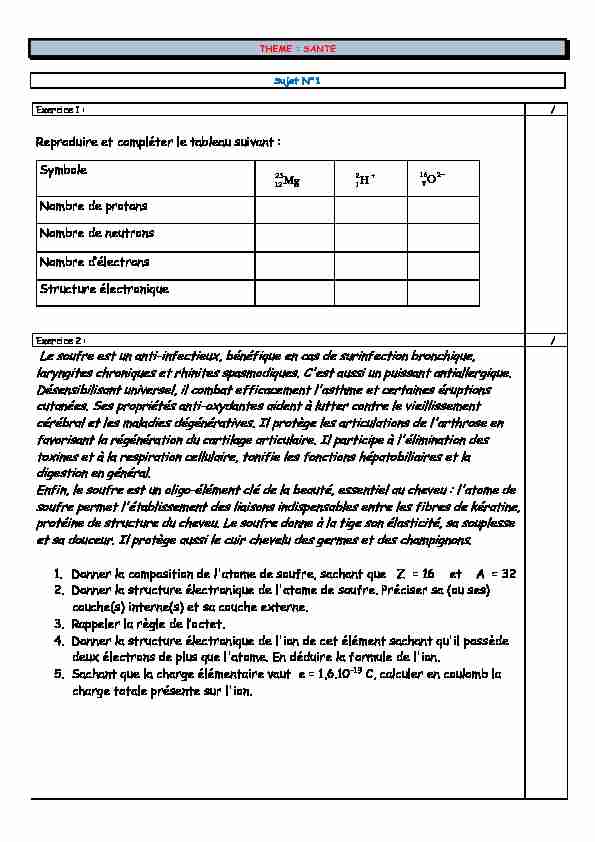
THEME : SANTE
Sujet N°1
Exercice 1 : /
Reproduire et compléter le tableau suivant :
Symbole
Nombre de protons
Nombre de neutrons
1RPNUH G·pOHŃPURQV
Structure électronique
Exercice 2 : /
Le soufre est un anti-infectieux, bénéfique en cas de surinfection bronchique, laryngites chroniques et rhinites spasmodiques. C'est aussi un puissant antiallergique. Désensibilisant universel, il combat efficacement l'asthme et certaines éruptions cutanées. Ses propriétés anti-oxydantes aident à lutter contre le vieillissementcérébral et les maladies dégénératives. Il protège les articulations de l'arthrose en
favorisant la régénération du cartilage articulaire. Il participe à l'élimination des toxines et à la respiration cellulaire, tonifie les fonctions hépatobiliaires et la digestion en général. Enfin, le soufre est un oligo-élément clé de la beauté, essentiel au cheveu : l'atome de soufre permet l'établissement des liaisons indispensables entre les fibres de kératine, protéine de structure du cheveu. Le soufre donne à la tige son élasticité, sa souplesse et sa douceur. Il protège aussi le cuir chevelu des germes et des champignons.1. Donner la composition de l'atome de soufre, sachant que Z = 16 et A = 32
2. Donner la structure électronique de l'atome de soufre. Préciser sa (ou ses)
couche(s) interne(s) et sa couche externe.3. Rappeler la règle GH O·RŃPHPB
4. Donner la structure électronique de l'ion de cet élément sachant qu'il possède
deux électrons de plus que l'atome. En déduire la formule de l'ion.5. Sachant que la charge élémentaire vaut e = 1,6.10-19 C, calculer en coulomb la
charge totale présente sur l'ion. H2 1Mg25 12 2168O Exercice3 : IH UMGRQ XQ JM] UMGLRMŃPLI G·RULJLQH naturelle Le radon est un élément chimique du tableau périodique de symbole Rn et de numéro atomique 86. F·HVP XQ JM] UMGLRMŃPLI G·RULJLQH QMPXUHOOH provenant de la désintégration du radium, lui-PrPH LVVX GH OM GpVLQPpJUMPLRQ GH O·XUMQLXP ŃRQPHQX GMQV Oa croûte terrestre. Il est inodore et incolore. Il est présent partout à la surface de la Terre mais plus particulièrement dans les sous-sols granitiques et volcaniques. En France, les régions riches en radon sont la Bretagne, le Massif central, les Vosges et la Corse. Il existe 34 isotopes de radon connus jusqu'à ce jour. Seuls 3 de ces isotopes se rencontrent dans la nature :
Le radon 222 qui est l'isotope le plus stable.
Le radon 220
Le radon 219
1. GRQQHU OM ŃRPSRVLPLRQ G·XQ QR\MX GH UMGRQ 222 HP G·Xn noyau de radon 220.
2. Quand dit-on que deux noyaux sont isotopes ?
3. (ŃULUH OM UHSUpVHQPMPLRQ V\PNROLTXH GH O·LVRPRSH OH SOXV VPMNOHB
Correction
Exercice 1 :
Exercice2 : soufre
1) Cet atome contient 16 protons (car Z =16), 16 neutrons (car A Z = 32 16 = 16) et autant d'électrons que de protons
(c'est-à-dire 16) pour assurer l'électroneutralité de l'atome.2) Cet atome possède 16 électrons. Sa structure électronique est donc : (K)2(L)8(M)6.
3 5qJOH GH O·RŃPHP : Pour accéder à la stabilité des gaz inertes, certains atomes ont tendance à gagner ou perdre des
électrons pour avoir une structure électronique en octet ( 8 électrons sur la couche externe ).
4) L'ion possède 16 + 2 = 18 électrons. Sa structure électronique est donc : (K)2(L)8(M)8
L'ion possède deux charges élémentaires négatives et se note 3216 S2².5) La charge de l'ion vaut : q(ion S2²) = q(protons) + q(électrons) = 16 e + 18 ( e) = 2 e = 2 1,6.10-19 = 3,2.10-19 C.
Exercice 3 : Radon
1) Représentation symbolique du noyau : 86 protons et 222 86 = 136 neutrons
2) neutrons sont
différents.3) Isotope le plus stable : 22286Rn
Symbole
Nombre de protons 12 1 8
Nombre de neutrons 13 1 8
1RPNUH G·pOHŃProns 12 0 10
Structure électronique K2L8M2 K0 K2L8
H2 1Mg25 12 2168Oquotesdbs_dbs28.pdfusesText_34
[PDF] nombre de charges positives dans le fer
[PDF] ion soufre formule
[PDF] ion lithium formule
[PDF] formule de l'ion iodure
[PDF] diametre primitif pignon chaine
[PDF] datedif ne fonctionne pas
[PDF] datedif excel 2010
[PDF] masse d'une mole de glucose
[PDF] lors d'un effort physique une partie du glucose stocké
[PDF] comment compter les mots en anglais
[PDF] compter les mots dans une phrase cp
[PDF] compter les lettres
[PDF] mots avec apostrophe
[PDF] compte-t-il
