 SV Concours
SV Concours
26 февр. 2020 г. spectroscopie : ... UV / Visible Infra-Rouge
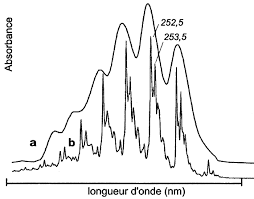 Spectroscopie UV-Visible
Spectroscopie UV-Visible
Spectroscopie : Etude des interactions entre la matière et un rayonnement ε ➚ : effet hyperchrome ε ➘ : effet hypochrome. Conjugaison; mais aussi ...
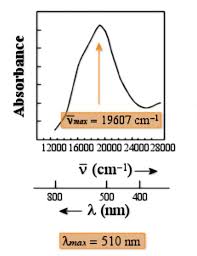 chap.I master Spectr. UV
chap.I master Spectr. UV
SPECTROSCOPIE D'ABSORPTION. DANS L'UV-VISIBLE. CHAPITRE I : PLAN. CHAPITRE II + effet hyperchrome sur la bande π → π*. Même effet observé sur la ...
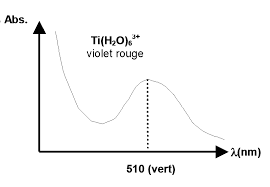 Chapitre III-Spectroscopie dabsorption dans lUV-visible
Chapitre III-Spectroscopie dabsorption dans lUV-visible
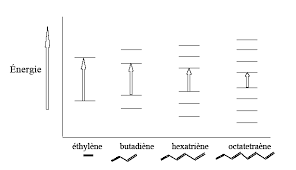
Il en découle un effet bathochrome et un effet hyperchrome sur la bande d'absorption correspondant à la transition π → π*. Composé λmax εmax. Ethylène. 165.
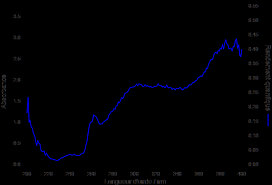 Intérêt de la méthode des ajouts dosés en spectroscopie UV-Visible
Intérêt de la méthode des ajouts dosés en spectroscopie UV-Visible
26 апр. 2023 г. une influence sur les propriétés d'absorption et un effet hyperchrome dans le cas de HCl et l'eau par rapport à H2SO4. 9 Dans le cas des ...
 CHAPITRE I-spectroscopie dabsorption UV-visible
CHAPITRE I-spectroscopie dabsorption UV-visible
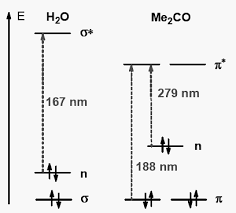
portés par un chromophore C=C ou C=O donnent des effets bathochrome et hyperchrome. V.3 - Effet de la conjugaison. L'enchaînement d'insaturations entraîne la
 8 Chapitre II - SPECTROSCOPIE DABSORPTION DANS LUV
8 Chapitre II - SPECTROSCOPIE DABSORPTION DANS LUV
portés par un chromophore C=C ou C=O donnent des effets bathochrome et hyperchrome. V.3 - Effet de la conjugaison. V.3.1 - Composés éthyléniques. L'enchaînement
 Chapitre 2 : Spectroscopie ultraviolet/visible
Chapitre 2 : Spectroscopie ultraviolet/visible
Remarque : On utilise également l'effet hyperchrome et l'effet hypochrome si on résonne par rapport à Є (coefficient d'absorption molaire). Effet
 3. Spectroscopie UV-Visible
3. Spectroscopie UV-Visible
Effet hyperchrome : le chromophore augmente l'intensité d'absorption : (augmente I). 3.4. Transitions π – π*. Mettre d'un e. Page
 [PDF] 3 Spectroscopie UV-Visible - LCMCP
[PDF] 3 Spectroscopie UV-Visible - LCMCP
Effet hyperchrome : le chromophore augmente l'intensité d'absorption : (augmente I) 3 4 Transitions ? – ?* Mettre d'un e Page
 [PDF] CHAPITRE I-spectroscopie dabsorption UV-visible
[PDF] CHAPITRE I-spectroscopie dabsorption UV-visible
Effet hypsochrome : déplacement des bandes d'absorption vers les courtes longueurs d'onde ? Effet hyperchrome : augmentation de l'intensité d'absorption
 [PDF] Chapitre 2 : Spectroscopie ultraviolet/visible
[PDF] Chapitre 2 : Spectroscopie ultraviolet/visible
La spectroscopie UV-Visible est la plus ancienne et la plus utilisée des méthodes d'analyse Effet hyperchrome: augmentation de l'intensité d'absorption
 [PDF] Spectroscopie UV-Visible - L3 Chimie Dijon
[PDF] Spectroscopie UV-Visible - L3 Chimie Dijon
Spectroscopie d'absorption UV-Visible Spectroscopie : Etude des interactions entre la matière et un rayonnement ? ? : effet hyperchrome
 [PDF] INTRODUCTION A LA SPECTROSCOPIE - EST Fkih Ben Salah
[PDF] INTRODUCTION A LA SPECTROSCOPIE - EST Fkih Ben Salah
Substituants à effet mésomère (auxochromes) OH -OR -X -NH2 portés par un chromophore C=C ou C=O : Effets bathochrome et hyperchrome
 [PDF] Spectroscopie UV-Visible
[PDF] Spectroscopie UV-Visible
La spectroscopie d'absorption dans l'UV et le visible est basée sur la propriété des molécules Effet hyperchrome : Augmentation de l'absorbance
 [PDF] Cours_Spectrophotométrie UV-VISIBLE
[PDF] Cours_Spectrophotométrie UV-VISIBLE
Effet hyperchrome: augmentation de l'intensité d'absorption L'analyse quantitative par la spectrométrie UV-visible est très employée (beaucoup
 [PDF] Chapitre XI Transitions électroniques Spectroscopie UV-visible 1
[PDF] Chapitre XI Transitions électroniques Spectroscopie UV-visible 1
Enfin un effet hyperchrome augmente ? un effet hypochrome le diminue 4 5 Aspect des spectres : raies bandes et structure fine
 [PDF] SPECTROSCOPIE MOLECULAIRE Introduction
[PDF] SPECTROSCOPIE MOLECULAIRE Introduction
La spectroscopie d'absorption dans l'UV et le visible est une méthode très commune Effet hyperchrome : Augmentation de l'absorbance
 Spectroscopie infrarouge - Webjournal Julie Daubié Rombas
Spectroscopie infrarouge - Webjournal Julie Daubié Rombas
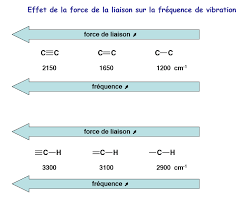
Les trois bandes précédentes subissent un effet hyperchrome ; le subit en outre un effet hypsochrome et les autres un effet bathochrome : 3 Triple liaison carbone–carbone Spectroscopie Infrarouge Page 3 sur 14
Quels sont les effets du chromophore ?
Effet hypsochrome :le chromophore augmente la fréquence d’absorption (diminue le lambdamax). Effet hypochrome :le chromophore diminue l’intensité d’absorption : (diminue varepsilon). Effet hyperchrome :le chromophore augmente l’intensité d’absorption : (augmente varepsilon).
Qu'est-ce que la spectroscopie infrarouge?
Spectroscopie infrarouge Spectroscopie infrarouge Les transitions énergétiques se font ici entre les niveaux d’énergie de rotation des molécules ou entre leurs niveaux d’énergie de vibration. Les transitions entre niveaux de rotation apparaissent dans l’I.R. lointain (de 20 à 250 µm ou de 500 à 40 ).
Comment calculer la spectrophotométrie d’absorption moléculaire ?
Spectrophotométrie d’absorption moléculaire Uv – Visible Les spectres Caractéristiques générales Spectres de bandes : A = f(lambda) niveaux d’énergie électronique Zone spectrale : UV: 100 à 400 nm en pratique, on travaille à partir de 200 nm, car les UV sont absorbés par l’O2 de l’air et par le matériel ( cuve de mesure) Visible: 400 à 800 nm
Qu'est-ce que la spectrophotométrie UV-visible ?
spectrophotométrie Uv-Visible est la technique spectroscopique implique l'interaction des substances avec les rayonnements ultra-violet et visible Skip to content Chimie Analytique Analyse chimique en main Menu Accueil Chimie en solution Les concentrations en chimie Eléctrochimie Chromatographie Eléctrophorèse Spéctroscopie Quiz Contact Search for:
P. Chaquin LCT-UPMC
Chapitre XI
Transitions électroniques
Spectroscopie UV-visible
1. Domaine UV-visible, lumière, couleurs
1.1. Domaine spectral
routine dans des laboratoires visible.Proche IR 1000 nm (10 000 cm-1)
Rouge 700 nm
Orangé 620 nm
Vert 530 nm
Bleu 470 nm
Violet 420 nm
Proche UV 400-200 nm
247P. Chaquin LCT-UPMC
de se placer en atmosphère de diazote pur. Au-delà, il faut opérer sous pression réduite et on
parle de la région " UV du vide ».1.2. Perception des couleurs
1.2.1 Couleurs résultant s sélectives
Figure 1. Couleurs fondamentales et complémentaires en absorptionRappelons que, les trois couleurs fondamentales étant le bleu, le jaune et le rouge1, le mélange
où les absorptions des pigments et colorants se cumulent par mélange. En mélangeant une fondamentale et son complémentaire on absorbe pratiquement tout le spectre visible et on obtient un gris plus ou moins foncé.1 Ou plus exactement, le cyan, le jaune et le magenta.
248P. Chaquin LCT-UPMC
La Fig. 2 montre le spectre de quelques filtres de couleur pour photographie, ce qui permet de couleur complémentaire.Fig. 2. Spectres
1.2.2 addition de lumières
Figure 3. Couleurs fondamentales et complémentaires en additionLe problème est alors de savoir quelle couleur est perçue lors de la superposition de faisceaux
lumineux de diverses couleurs. Les couleurs fondamentales sont, cette fois, le rouge, le vert et 249P. Chaquin LCT-UPMC
considérant le mécanisme physiologique de la perception des couleurs àFigure 4. Absorption des pigments rétiniens.
On peut constater, par exemple que la pe
simultanée des pigments rouge et vert.1.2.3. Intermède poétique : ciel bleu et soleil couchant
2 et N2
pas dans le visible), avec des gouttelettes et des petites particules, qui diffusent une partie de -à-dire absorbent et réémettent immédiatement des photons sans être portéesdans un état excité stationnaire. La probabilité de ce phénomène varie comme la puissance
lumière rouge. " rougie qui nous concerne, plus rarement observé) du soleil. 250P. Chaquin LCT-UPMC
Coucher de soleil à Paros
1.4. Energie photonique et transitions moléculaires
domaine mettent en jeu des énergies -1 mol-1 pour 200 nm à 150 kJ mol-1 pour 800 nm. Ces énergies sont susceptibles de provoquer des transitions électroniques entre OM de la couche de valence. Elles sont insuffisantes pour électrons de " -à-dire des couches atomiques internes (ex. 1s du2. Spectres atomiques
leurs spectres évidemment tendance à se recombiner très rapidement en molécules diatomiques. Seuls des 251P. Chaquin LCT-UPMC
exemp" chauffer au rouge », " au blanc ». Une " étincelle » ou " décharge électrique » dans un gaz,
lécules sont ionisées puis dissociées en atomes, ions atomiques et électrons (plasma). Ces derniers tendent à se niveau en niveau en émettant des photons, ce qui p atomiques, dans la mesure où elles sont permises.2.1.1. Règles de sélection
Les transitions obéissent aux règles de sélection suivantes valables pour les atomes " légers »
présentant le couplage LS (cf. chapitre III.3.2) : Règles de sélection pour les transitions atomiques S = 0 L = 0, ± 1 (L = ± 1 pour un atome à un électron)J = 0, ± 1 sauf J ĺJ = 0
de transition. fiifM) PF& aspects importants. (i) Règles relatives au spin Les fonctions du moment de transition sont les fonctions électroniques totales dépendant -orbite est négligeable en première approximation des ne contient que 252P. Chaquin LCT-UPMC
fififfiiifM6<< 6<6< PPquotesdbs_dbs44.pdfusesText_44[PDF] groupe caractéristique terminal s
[PDF] groupe caractéristique acide carboxylique
[PDF] societe coloniale def
[PDF] reproduction humaine cm2 évaluation
[PDF] analyse focus group
[PDF] focus groupe pdf
[PDF] grille pour focus group
[PDF] exemple question focus groupe
[PDF] qu'est ce qu'un entretien collectif
[PDF] focus groupe exemple
[PDF] l'entretien collectif: l'enquête et ses méthodes
[PDF] comment animer focus groupe
[PDF] spectroscopie uv visible
[PDF] influence du groupe sur l'individu
