 Activité Numérique : Histoire de latome
Activité Numérique : Histoire de latome
27 juil. 2016 Cycle 4 - 3ème. Organisation et transformations de la matière. Activité Numérique : Histoire de l'atome. DESCRIPTIF DE SUJET DESTINE AU ...
 Scénario Modèle de latome. Cycle 4 (niveau 3ème)
Scénario Modèle de latome. Cycle 4 (niveau 3ème)
l'histoire du modèle de l'atome La longue · histoire de l'atome. - Bilan des activités. Leçon (le modèle planétaire de Rutherford ). - Exercices d'entraînement
 Il était une fois latome ….- Correction
Il était une fois latome ….- Correction
3 La théorie atomique n'a cessé d'évoluer au fil des siècles au fur et à mesure des découvertes scientifiques et de l'évolution des mentalités. 4 On considèrera
 PHYSIQUE-CHIMIE
PHYSIQUE-CHIMIE
Chaque groupe travaille sur une des 7 étapes de l'histoire de l'atome. Les 3ème étape : Chaque élève complète ensuite sa frise chronologique grâce aux ...
 Fiche de révision de 3eme en physique chimie - DNB
Fiche de révision de 3eme en physique chimie - DNB
Ions positifs appélés CATIONS : Atome ou groupe d'atomes qui a PERDU des électrons. L'univers a une histoire qui débute il y a 138 milliards d'années avec ...
 Fiche de révision de 3eme en physique chimie - DNB
Fiche de révision de 3eme en physique chimie - DNB
Ex : Fe2+ Fe3+
 Chapitre 5 : Atomes et ions I –Latome 1. Histoire de latome Activité
Chapitre 5 : Atomes et ions I –Latome 1. Histoire de latome Activité
- L'atome est électriquement neutre c'est à dire qu'il a autant de charges positives. Page 3. (protons) dans le noyau que de charges négatives dans le nuage d'
 Création (Pourquoi pas Synthèse
Création (Pourquoi pas Synthèse
Troisième. Durée. 1h30. Type d'activité : Activité documentaire « puzzle » qui peut être évaluée. Titre de l'activité: L'Histoire de l'atome. Partie du
 séquence n°1: latome tout puissant !
séquence n°1: latome tout puissant !
3 sept. 2017 séquence n°1: l'atome tout puissant ! cycle 4: niveau 3ème. AUBIN JULIEN 03 ... la longue histoire de l'atome. Activit__documentaire__ ...
 TP ACTIVITE N°1
TP ACTIVITE N°1
L'histoire de l'atome. 5. I. La découverte des atomes. Page 2. 2. Coller les étiquettes sur la frise chronologique de l'histoire de la découverte de l'atome.
 Activité Numérique : Histoire de latome
Activité Numérique : Histoire de latome
Cycle 4 - 3ème. Organisation et transformations de la matière. Activité Numérique : Histoire de l'atome. DESCRIPTIF DE SUJET DESTINE AU PROFESSEUR.
 3-Activite-La longue histoire de latome
3-Activite-La longue histoire de latome
Activité : La longue histoire de l'atome. Les informations ci dessous sont complètement en désordre. En les lisant bien tu vas pouvoir reconstituer une
 Activité différenciée histoire de latome
Activité différenciée histoire de latome
Question bonus : comparer la taille du noyau atomique et celle de l'atome. E.Rutherford. Page 3. Niveau : 3ème-2nde. COMPETENCES : S'APPROPRIER
 Fiche de révision de 3eme en physique chimie - DNB
Fiche de révision de 3eme en physique chimie - DNB
Les 118 atomes différents sont classés dans le tableau périodique des éléments par numéro atomique Z croissant : 18 colonnes 7 lignes. Atome. Nombre de protons
 Scénario Modèle de latome. Cycle 4 (niveau 3ème)
Scénario Modèle de latome. Cycle 4 (niveau 3ème)
Expliquer par l'histoire des sciences et des techniques
 Il était une fois latome ….- Correction
Il était une fois latome ….- Correction
3 La théorie atomique n'a cessé d'évoluer au fil des siècles au fur et à mesure des découvertes scientifiques et de l'évolution des mentalités. 4 On considèrera
 TP ACTIVITE N°1
TP ACTIVITE N°1
Coller les étiquettes sur la frise chronologique de l'histoire de la découverte de l'atome. Les différentes images obtenues au microscope.
 Niveau 3ème pour lannée scolaire 2010/2011 Question
Niveau 3ème pour lannée scolaire 2010/2011 Question
Objectifs : au travers les deux documents et des questions qui suivent découvrir. La structure d'un atome. Une approche de l'historique de la découverte de
 CORRECTION ACTIVITE 4 Histoire de latome
CORRECTION ACTIVITE 4 Histoire de latome
CHIMIE CHAPITRE 2 : Conduction des métaux ACTIVITE 4 : Histoire de l'atome. CORRECTION. L'antiquité. Le premier modèle atomique. Dans le modèle les atomes
 PHYSIQUE-CHIMIE
PHYSIQUE-CHIMIE
Il s'agit d'un travail collaboratif sur l'histoire de l'atome. Mots clefs : Histoire des sciences Atome
La théorie atomique : une longue histoire
Dès l'antiquité, le mot atome a été utilisé. Il vient du grec atomos, " qu'on ne peut couper ».
Mais quelle évolution depuis la conception des Anciens jusqu'à la structure des atomes admise aujourd'hui ! L'intuition des philosophes de l'AntiquitéL'intuition des philosophes de l'AntiquitéLa notion d'atome a été introduite dès l'Antiquité. Cinq siècles avant J.C., les philosophes
grecs Leucippe et Démocrite affirmaient, sans preuve, que la matière ne pouvait être divisée
indéfiniment et que l'atome était le plus petit morceau de matière qui puisse exister. Un siècle
plus tard, le philosophe Aristote rejette cette théorie et ne prend en considération que quatre
éléments fondamentaux : l'air, l'eau, la terre et le feu. C'est sur ces idées fausses que vont reposer
les travaux des alchimistes pendant plus de vingt siècles. Ceux-ci, mi-sorciers, mi-alchimistes, recherchaient la pierre philosophale qui devait avoir des propriétés merveilleuses, notammentcelle de guérir les maladies et celle de transformer le plomb en or. La naissance de la chimieLa naissance de la chimie
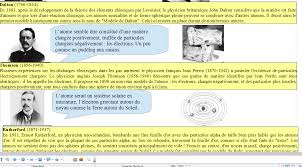
John Dalton (1766-1844) peut être considéré comme le fondateur de la théorie atomique. En 1803, il affirme que la matière est constituée d'atomes et que les atomes constituent un corps simple sont identiques entre eux mais qu'ils sont différents d'un corps simple à un autre. D'autre part, il interprète la réaction chimique comme un nouvel arrangement des atomes. Cependant, il ne fait pas encore la différence entre atomes et molécules. C'est Stanislao Cannizzaro (1826-1910), chimiste italien, qui faitadopter définitivement, en 1856, la théorie atomique grâce à ses travaux qui corrigent les
insuffisances de la théorie de Dalton. Il affirme qu'une molécule d'un corps composé contient un
nombre entier d'atomes de chacun de ses composants. Ce n'est qu'à partir de cette date qu'on fait la distinction entre atomes et molécules. A cette époque, on connaît 63 types d'atomes. Leschimistes ont remarqué que certains atomes ont des propriétés analogues et ils ont cherché à les
regrouper en familles. Ainsi, en 1869, Mendeleïev, chimiste russe, a réussi à classer les atomes
dans un tableau à huit colonnes dont certaines cases restaient vides. Pour remplir ces cases vides,
il a prévu la découverte de nouveaux atomes et même décrit leurs propriétés. Ces prédictions se
sont révélées exactes. De nos jours, les chimistes, s'inspirant du tableau de Mendeleïev, utilisent
un tableau appelé " tableau périodique des éléments » qui regroupe plus d'une centaine d'atomes.
Bien d'autres chimistes du XIXème siècle ont participé à la construction de la chimie. Leur
tâche était difficile car ils ne disposaient pas d'appareillages comparables à ceux qui sont utilisés
aujourd'hui.Le modèle planétaire de l'atomeLe modèle planétaire de l'atome En 1897, Joseph Thomson a découvert l'existence de l'électron. En 1907, des ions positifs ayant des masses beaucoup plus grandes que celle de l'électron sont mis en évidence. Thomsonpropose alors un modèle de l'atome : des électrons chargés négativement sont collés sur une
grosse particule chargée positivement. On a comparé ce modèle à un gâteau sur lequel sont posés
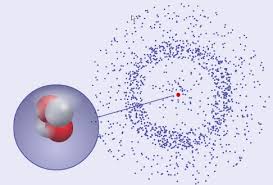
des raisins ! L'expérience de Rutherford, en 1912, a montré que l'atome a une structure lacunaire. Il estconstitué d'un noyau, chargé positivement, où est concentré l'essentiel de la masse. Autour de ce
noyau, qui occupe un volume très faible, gravitent à grande distance des électrons minuscules.
J. Dalton
Ce modèle planétaire de l'atome se rapproche beaucoup de celui qui est adopté aujourd'hui, mais il a connu bien des améliorations. Les recherches continuentLes recherches continuent Actuellement, les chercheurs travaillent beaucoup sur la structure des noyaux des atomes.Pour étudier les particules qui constituent les noyaux, ils disposent d'accélérateurs de particules
de plus en plus gigantesques. Le dernier accélérateur du Centre européen de recherche nucléaire
(Cern) est un anneau de 27 km de circonférence ! En 1992, Georges Charpak, physicien français né
en Pologne en 1924, a reçu le prix Nobel de physique pour " l'invention et le développement dedétecteurs de particules ». Ces détecteurs ont permis de découvrir de nouvelles particules.
Extrait " physique chimie collège », Michel Chevalet, Éditions de la CitéLexique
: " lacunaire » : constitué de vide.1) Compétence S'APPROPRIER.
A partir des documents, réaliser une frise chronologique qui retrace l'évolution de l'atome depuis
les grecs (V ème siècle avant J.C.) jusqu'à Georges Charpak (1992). Vous attribuerez à chaque personnage historique le travail effectué sur l'atome.2) Compétence REALISER.
A partir des documents, proposer un schéma représentant l'atome selon Rutherford.3) Compétence ANALYSER.
A l'aide de l'extrait vidéo appelé " l'expérience de Rutherford » sur le site http://www.palais- decouverte.fr/index.php?id=1837 et du schéma proposés, répondre aux questions suivantes.Schéma de l'expérience
1. Qu'interpose-t-on entre la source de particules alpha et les deux détecteurs D1 et D2?
2. On bombarde la feuille interposée de particules alpha, qu'observe-t-on au niveau de D
1 ? Que
peut-on en conclure quant à la composition de cette feuille ? Que peut-on en conclure quant à la
composition de l'atome de façon générale ?3. Certaines particules sont déviées vers D
2. Cela permet de montrer qu'une petite région dans
l'atome est capable de dévier les particules alpha. Comment s'appelle-t-elle ?4. Question bonus : comparer la taille du noyau atomique et celle de l'atome.
E.Rutherford
Niveau : 3ème-2nde COMPETENCES : S'APPROPRIER - REALISER - ANALYSERLa théorie atomique : une longue histoire
Dès l'antiquité, le mot atome a été utilisé. Il vient du grec atomos, " qu'on ne peut couper ».
Mais quelle évolution depuis la conception des Anciens jusqu'à la structure des atomes admise aujourd'hui ! L'intuition des philosophes de l'AntiquitéL'intuition des philosophes de l'AntiquitéLa notion d'atome a été introduite dès l'Antiquité. Cinq siècles avant J.C., les philosophes
grecs Leucippe et Démocrite affirmaient, sans preuve, que la matière ne pouvait être divisée
indéfiniment et que l'atome était le plus petit morceau de matière qui puisse exister. Un siècle
plus tard, le philosophe Aristote rejette cette théorie et ne prend en considération que quatre
éléments fondamentaux : l'air, l'eau, la terre et le feu. C'est sur ces idées fausses que vont reposer
les travaux des alchimistes pendant plus de vingt siècles. Ceux-ci, mi-sorciers, mi-alchimistes, recherchaient la pierre philosophale qui devait avoir des propriétés merveilleuses, notamment celle de guérir les maladies et celle de transformer le plomb en or. La naissance de la chimieLa naissance de la chimie John Dalton (1766-1844) peut être considéré comme le fondateur de la théorie atomique. En 1803, il affirme que la matière est constituée d'atomes et que les atomes constituent un corps simple sont identiques entre eux mais qu'ils sont différents d'un corps simple à un autre. D'autre part, il interprète la réaction chimique comme un nouvel arrangement des atomes. Cependant, il ne fait pas encore la différence entre atomes et molécules. C'est Stanislao Cannizzaro (1826-1910), chimiste italien, qui fait adopterdéfinitivement, en 1856, la théorie atomique grâce à ses travaux qui corrigent les insuffisances de
la théorie de Dalton. Il affirme qu'une molécule d'un corps composé contient un nombre entier
d'atomes de chacun de ses composants. Ce n'est qu'à partir de cette date qu'on fait la distinction
entre atomes et molécules. A cette époque, on connaît 63 types d'atomes. Les chimistes ontremarqué que certains atomes ont des propriétés analogues et ils ont cherché à les regrouper en
familles. Ainsi, en 1869, Mendeleïev, chimiste russe, a réussi à classer les atomes dans un tableau à
huit colonnes dont certaines cases restaient vides. Pour remplir ces cases vides, il a prévu ladécouverte de nouveaux atomes et même décrit leurs propriétés. Ces prédictions se sont révélées
exactes. De nos jours, les chimistes, s'inspirant du tableau de Mendeleïev, utilisent un tableau appelé " tableau périodique des éléments » qui regroupe plus d'une centaine d'atomes.Bien d'autres chimistes du XIX
ème siècle ont participé à la construction de la chimie. Leurtâche était difficile car ils ne disposaient pas d'appareillages comparables à ceux qui sont utilisés
aujourd'hui. Le modèle planétaire de l'atomeLe modèle planétaire de l'atome En 1897, Joseph John Thomson a découvert l'existence de l'électron. En 1907, des ions positifs ayant des masses beaucoup plus grandes que celle de l'électron sont mis en évidence.Thomson propose alors un modèle de l'atome : des électrons chargés négativement sont collés sur
une grosse particule chargée positivement. On a comparé ce modèle à un gâteau sur lequel sont
posés des raisins ! L'expérience de Rutherford, en 1912, a montré que l'atome a une structure lacunaire. Il estconstitué d'un noyau, chargé positivement, où est concentré l'essentiel de la masse. Autour de ce
noyau, qui occupe un volume très faible, gravitent à grande distance des électrons minuscules.
J. Dalton
Ce modèle planétaire de l'atome se rapproche beaucoup de celui qui est adopté aujourd'hui, mais il a connu bien des améliorations. Les recherches continuentLes recherches continuent Actuellement, les chercheurs travaillent beaucoup sur la structure des noyaux des atomes.Pour étudier les particules qui constituent les noyaux, ils disposent d'accélérateurs de particules
de plus en plus gigantesques. Le dernier accélérateur du Centre européen de recherche nucléaire
(Cern) est un anneau de 27 km de circonférence ! En 1992, Georges Charpak, physicien français né
en Pologne en 1924, a reçu le prix Nobel de physique pour " l'invention et le développement dedétecteurs de particules ». Ces détecteurs ont permis de découvrir de nouvelles particules.
Extrait " physique chimie collège », Michel Chevalet, Éditions de la CitéLexique
" lacunaire » : constitué de vide.1) Compétence S'APPROPRIER.
A partir des documents, recopier et compléter la frise chronologique qui retrace l'évolution de
l'atome depuis les grecs (V ème siècle avant J.C.) jusqu'à Georges Charpak (1992). Vous attribuerez à chaque personnage historique une phrase qu'il aurait pu dire.2) Compétence REALISER.
A partir des documents, ajouter une légende pour compléter le schéma représentant l'atome
selon Rutherford. L 'atome selon Rutherford.Vème siècle avant J.C.
IVème siècle avant J.C.1803
186918971912
1992Georges Charpak
Ernest RutherfordJoseph John Thomson
Mendeleïev
John Dalton
Aristote
Leucippe et Démocrite
Je pense que l'on ne peut pas
diviser indéfiniment la matière. Je suis affirmatif! La matière est constituée de quatre éléments fondamentaux : l'air, l'eau, la terre et le feu.J'affirme que la matière est
constituée d'atomes.J'ai classé les atomes dans un tableau
à huit colonnes dont certaines cases
restaient vides.J'ai découvert l'existence de l'électron.Je peux affirmer que l'atome est
essentiellement constitué de vide.Je suis fier d'avoir contribué à
l'invention de détecteurs de particules.E.Rutherford
3) Compétence ANALYSER.A l'aide de l'extrait vidéo appelé " l'expérience de Rutherford » sur le site
http://www.palais-decouverte.fr/index.php?id=1837 et du schéma proposés, cocher la (ou les) bonne(s) réponse(s).
Schéma de l'expérience
1. Entre la source de particules alpha et les deux détecteurs D1 et D2 , on interpose :
□un atome ; □une feuille d'or ; □un électron.2. On bombarde la feuille interposée de particules alpha. La plupart des particules atteignent D
1 comme si : □elles rencontraient un obstacle ; □elles ne rencontraient aucun obstacle ; □elles étaient inexistantes.3. Cette expérience permet de montrer que la feuille interposée est :
□constituée essentiellement de vide ; □constituée de matière ; □constituée de particules alpha.4. Les particules alpha déviées vers D
2 mettent en évidence une petite région de l'atome appelée...
□électron ; □noyau atomique ; □atome.5. Question bonus : le noyau atomique et l'atome ont-ils la même taille ? Si non, quel est celui qui
est le plus grand ?quotesdbs_dbs1.pdfusesText_1[PDF] histoire de l'école maternelle
[PDF] histoire de l'école pdf
[PDF] histoire de l'éducation dans l'antiquité
[PDF] histoire de l'éducation en france chronologie
[PDF] histoire de l'éducation en france pdf
[PDF] histoire de l'émancipation des femmes
[PDF] histoire de l'empire ottoman pdf
[PDF] histoire de l'empire ottoman robert mantran pdf
[PDF] histoire de l'enfance en occident
[PDF] histoire de l'enseignement des sciences ? l'école primaire
[PDF] histoire de l'enseignement en france
[PDF] histoire de l'enseignement et de l'éducation
[PDF] histoire de l'enseignement pdf
[PDF] histoire de l'eps capeps
