 Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Fiche Corrigés. 4) Les ions oxonium proviennent des ions ammonium acide du couple NH4. +/NH3. ▻ Exercice n°4. 1) Dans le cas de la solution de bromure de
 Conversion dénergie : piles et électrolyses
Conversion dénergie : piles et électrolyses
27 mars 2022 piles et électrolyses. Piles. Exercice 1 : Pile à combustible à oxyde solide écrit PT 2015
 DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
%20accu%20%26%20e%CC%81lectrolyse-Complet.pdf
 Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
3) Confirmer tout ceci en calculant le quotient de réaction initial. ▻ Exercice n°3. On considère une pile saline de f-é-m 15 V
 Exercices sur les piles et lélectrolyse
Exercices sur les piles et lélectrolyse
1F = 96500 C/mol. corrigé à la cathode négative se produit une réduction des ion Cd2+. Cd2+ + 2e- = Cd (s) à l'anode positive se produit une oxydation de l
 Oxydoréduction – corrigé des exercices Table des matières
Oxydoréduction – corrigé des exercices Table des matières
En effet pour que la pile fonctionne
 Conversion dénergie : piles et électrolyses
Conversion dénergie : piles et électrolyses
27 mars 2022 Piles. Exercice 1 : Pile à combustible à oxyde solide écrit PT 2015
 Conversion électrochimique dénergie : piles et électrolyses
Conversion électrochimique dénergie : piles et électrolyses
3 avr. 2023 d'énergie : piles et électrolyses. Piles. Exercice 1 : Pile à combustible à oxyde solide écrit PT 2015
 DM no10 – TS1 2011 Oscillations + Piles et électrolyses (pour le 27
DM no10 – TS1 2011 Oscillations + Piles et électrolyses (pour le 27
Corrigé du DM no10 – TS1 2011. Oscillations + Piles et électrolyses. Exercice 1 Exercice 1 – Pile .../11. Légende figure 1. Cu + réduction Zn - oxydation.
 CORRIGE
CORRIGE
trois modules « piles à combustibles » Hydrox (doc. 2). Chacun de ces électrolyses. (Fig. 4). l) Pourquoi devrait-on essayer de se passer de l'énergie ...
 DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
DS no8 Piles accumulateurs & électrolyse Exercice 1 – La pile sous
%20accu%20%26%20e%CC%81lectrolyse-Complet.pdf
 Exercices sur les piles et lélectrolyse
Exercices sur les piles et lélectrolyse
1F = 96500 C/mol. corrigé à la cathode négative se produit une réduction des ion Cd2+. Cd2+ + 2e- = Cd (
 Corrigés des exercices
Corrigés des exercices
l'exercice 9. On aurait pu aussi réaliser l'électrolyse d'une solution Le courant sort de la pile par l'électrode de cuivre. ... Corrigés des exercices.
 Oxydoréduction – corrigé des exercices Table des matières
Oxydoréduction – corrigé des exercices Table des matières
En effet pour que la pile fonctionne
 Conversion dénergie : piles et électrolyses
Conversion dénergie : piles et électrolyses
27 mars 2022 TD 24 – Électrochimie. Correction. Conversion d'énergie : piles et électrolyses. Piles. Exercice 1 : Pile à combustible à oxyde solide.
 Électrochimie
Électrochimie
15 Piles et électrolyses Constitution d'une pile éq de fonctionnement
 DM no10 – TS1 2011 Oscillations + Piles et électrolyses (pour le 27
DM no10 – TS1 2011 Oscillations + Piles et électrolyses (pour le 27
Les trois parties de cet exercice sont indépendantes. 1. La pile Daniell. Conçue en 1836 par le physicien britannique. John Daniell elle met en jeu les deux
 Liaisons chimiques (6 points) Deuxième exercice : Réalisation de la
Liaisons chimiques (6 points) Deuxième exercice : Réalisation de la
Deuxième exercice : Réalisation de la pile Magnésium - Chrome (8 points). Pour construire la pile Troisième exercice : Électrolyse de l'eau (6 points).
 Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
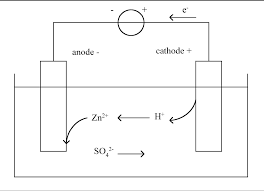
circulent de la demi pile à l’aluminium vers la demi pile au nickel et les anions en sens inverse Exercice n°2 1) Les électrons circulent dans le sens contraire du courant électrique
 Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
Déterminer le sens du courant électrique et le sens de déplacement des porteurs de charge dans la pile et hors de la pile Exercice n°2 On réalise une pile avec les couples Au 3+
 Correction Conversiond’énergie: pilesetélectrolyses
Correction Conversiond’énergie: pilesetélectrolyses
Correction TD 24 : Conversion d’énergie : piles et électrolyses Blaise Pascal PT 2021-2022 Exercice2:Pileargent-zinc 1 2 Structureetfonctionnementd’unepile; Capacité 1 Laf é m delapileestladifférenceentrelespotentielsredoxdesdeuxélectrodesquisontdonnésparlaloide Nernst Pourl’électroded’argent E Ag = E Ag+/Ag + 006logc= 076V
En partenariat avec :
Fiche téléchargée sur www.studyrama.com
LE TALENT C'EST D'AVOIR ENVIE
CHIMIESérie SNº : 37004
Fiche Corrigés
1) 2) Ni (s) = Ni2+(aq)
+ 2 e (× 3) Al3+(aq)
+ 3 e = Al (s) (× 2) __________________________ 3 Ni (s) + 2 Al3+(aq)
= 3 Ni2+(aq)
+ 2 Al (s) 3)Il faut calculer [Ni2+]i et [Al3+]i
A.N. :
12 3 - i2Lmol 0 18,610 115016,0) 432,1(58,70 0,2 ][Ni
VMm 2 Vn 2Vn ][Al
3423423423
)(SOlA )(SOlA )(SOlA lA i3A.N. :
12 3 - i3 Lmol 0 17,790 115016,0)) 432,1(327,02 (0 0,22 ][Al 2 i33 i2 ir, ][Al][Ni QA.N. : 1,11)0 19 7,7()0 11 6,8( Q
2232ir, Q donc la réaction avance spontanément dans le sens indirect de l'équation. 4)
On en déduit qu'il y a oxydation de l'aluminium et réduction des ions nickel. Ainsi la lame d'aluminium est l'anode et la lame de
nickel est la cathode. 2En partenariat avec :
Fiche téléchargée sur www.studyrama.com
LE TALENT C'EST D'AVOIR ENVIE
CHIMIESérie SNº : 37004
Fiche Corrigés
5) Dans une pile, l'anode s'enrichit en électrons, ici par la réaction Al (s) = Al3+(aq)
+ 3 e , donc il s'agit de la borne -. La cathode s'appauvrit en électrons, ici par la réaction Ni2+(aq)
+ 2 e = Ni (s) , donc il s'agit de la borne +. 6)Hors de la pile, le courant électrique circule de la borne + vers la borne -, donc de la demi pile au nickel vers la demi pile à
l'aluminium. Les électrons circulent en sens inverse : de la demi pile à l'aluminium vers la demi pile au nickel. Dans la pile, les cations
circulent de la demi pile à l'aluminium vers la demi pile au nickel et les anions en sens inverse.
1)Les électrons circulent dans le sens contraire du courant électrique, donc de la demi pile au cuivre vers la demi pile à l'or. Dans
la pile les anions vont de la demi pile à l'or vers la demi pile au cuivre et les cations dans l'autre sens.
2)Les électrons arrivent sur l'électrode d'or, ils y sont donc transformés, il y a réduction :
Au3+(aq)
+ 3 e = Au (s) Les électrons sont libérés sur l'électrode de cuivre, donc il y a oxydation : Cu (s) = Cu2+(aq)
+ 2 e L'équation de fonctionnement de la pile dans le sens direct est : 3 Cu (s) + 2 Au3+(aq)
= 3 Cu2+(aq)
+ 2 Au (s) L'anode est l'électrode de cuivre et la cathode est l'électrode d'or. 3) 2 i33 i2 ir, ][Au][Cu QA.N. :
2- 2131ir,
0 18,9)0 10,3()0 10,2( Q
Q par conséquent la réaction de fonctionnement avance bien dans le sens direct. 1)Les couples sont Zn
2+ /Zn et MnO 2 /MnO(OH). A l'anode Zn = Zn 2+ + 2e et à la cathode MnO 2 + H 3 O + e = MnO(OH) + H 2 O.Pour le fonctionnement de la pile :
Zn + 2 MnO
2 + 2 H 3 O = Zn 2+ + 2 MnO(OH) avec le nombre stoechiométrique d'échange d'électrons z = 2. 2) Q max = z · xquotesdbs_dbs2.pdfusesText_3[PDF] exercices corrigés pourcentages 5ème
[PDF] exercices corrigés pourcentages 6ème
[PDF] exercices corrigés probabilités lois usuelles
[PDF] exercices corrigés produit de convolution
[PDF] exercices corrigés programmation assembleur 8086
[PDF] exercices corrigés programmation en c pdf
[PDF] exercices corrigés reaction chimique pdf
[PDF] exercices corrigés recherche opérationnelle
[PDF] exercices corrigés relation binaire pdf
[PDF] exercices corrigés relation fondamentale de la dynamique
[PDF] exercices corrigés repère dans le plan 3ème pdf
[PDF] exercices corrigés rmn terminale s
[PDF] exercices corrigés second degré 1ère s
[PDF] exercices corrigés seconde fonctions
