 LES ALCANES
LES ALCANES
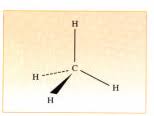
Les alcanes sont des hydrocarbures de formule brute CnH2n+2. Tous leurs atomes de carbone sont tétragonaux. Le méthane CH4 est le plus simple des alcanes.
 NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
b) Trouver la structure d'une molécule connaissant le nom. 1. Hydrocarbures (HC) saturés acycliques : les alcanes. Les hydrocarbures saturés ne sont formés
 Les alcanes et les alcools
Les alcanes et les alcools
On appelle hydrocarbures les molécules contenant uniquement des atomes de carbone et d'hydrogène : les alcanes sont des hydrocarbures à chaîne linéaire et
 T.P. cours Alcanes Alcools
T.P. cours Alcanes Alcools
Doc n°2 : Les alcanes. Les alcanes sont des hydrocarbures (constitués uniquement d'atomes de carbone et d'hydrogènes) acycliques de formule brute : CnH2n+2.
 Ce document est le fruit dun long travail approuvé par le jury de
Ce document est le fruit dun long travail approuvé par le jury de
pdf. Baldwin et al. (1982). BALDWIN R.R.
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
Les alcanes sont des hydrocarbures saturés de formule brute CnH2n+2. Le nom Pour nommer un radical il suffit de remplacer la terminaison. "ane" de l'alcane ...
 Les alcanes exercices corrigés
Les alcanes exercices corrigés
Les alcanes exercices corrigés pdf 3eme. Hydrocarbure saturé les alcanes exercices corrigés pdf. Exercices corrigés sur les alcanes 3ème pdf. Les alcanes
 Untitled
Untitled
Les ligroïnes (Eb = 60-120°C) sont constituées principalement d'hexane d'heptane et d'octane. Les essences (Eb = 50 à 200°C) se composent d'alcanes moyens
 ALCANES ET ALCOOLS
ALCANES ET ALCOOLS
Combien de doublets liants forme-t-il avec les atomes voisins ? (Rappel : numéro atomique du carbone Z =6.) ➢ Un alcane non-cyclique est un hydrocarbure de
 LES ALCANES
LES ALCANES
Les alcanes sont des hydrocarbures de formule brute CnH2n+2. Tous leurs atomes de carbone sont tétragonaux. Le méthane CH4 est le plus simple des alcanes.
 NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
Hydrocarbures (HC) saturés acycliques : les alcanes. Les hydrocarbures saturés ne sont formés que de carbone et d'hydrogène.
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
I/ NOMENCLATURE DES ALCANES ACYCLIQUES. Les alcanes sont des hydrocarbures saturés de formule brute CnH2n+2. Le nom des alcanes se termine par le suffixe
 Nomenclature des alcanes et des alcènes
Nomenclature des alcanes et des alcènes
Par conséquent dans une molécule d'alcane
 63 Chapitre 6 : Alcanes
63 Chapitre 6 : Alcanes
Ils sont saturés de formule brute générale CnH2n+2. Les alcanes de C1 à C4 (du méthane au butane) sont gazeux à température ambiante. Jusqu'à C16
 Les alcanes et les alcools
Les alcanes et les alcools
On appelle hydrocarbures les molécules contenant uniquement des atomes de carbone et d'hydrogène : les alcanes sont des hydrocarbures à chaîne linéaire et
 Lycée Maurice Ravel
Lycée Maurice Ravel
Exercices sur les alcanes et les alcools. Exercice 3 : 4. Ecrire la formule brute du 2-methylpropane. 5. Ecrire la formule semi-développée de cette molécule.
 ALCANES ET CYCLOALCANES 1- Définitions Les hydrocarbures
ALCANES ET CYCLOALCANES 1- Définitions Les hydrocarbures
Les noms des alcanes linéaires comportant un nombre d'atomes de carbone supérieur à quatre sont obtenus en faisant suivre du suffixe "ane" un préfixe numérique
 Cours de chimie organique
Cours de chimie organique
Les 4 orbitaux « s » sphériques de 4 atomes d'hydrogène formant un système tétraédrique. Cette hybridation du carbone se retrouve dans tous les alcanes de
 Devoirs : Les alcanes
Devoirs : Les alcanes
On recherchait les composés du gazole …. Exercice 1 : I can all ! / 12 pts. Nommer les alcanes suivants : 1
 [PDF] LES ALCANES
[PDF] LES ALCANES
Alcanes à chaîne carbonée non ramifiée Les quatre premiers alcanes (1 < n < 4) portent des noms consacrés par l'usage : méthane éthane propane butane Les
 [PDF] Nomenclature en chimie organique - UniNE
[PDF] Nomenclature en chimie organique - UniNE
1 NOMENCLATURE EN CHIMIE ORGANIQUE La nomenclature permet de : a) Trouver le nom d'une molécule 1 Hydrocarbures (HC) saturés acycliques : les alcanes
 [PDF] COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
[PDF] COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
Les alcanes sont des hydrocarbures saturés de formule brute CnH2n+2 Le nom des alcanes se termine par le suffixe "ane" I-1- Alcanes à chaîne linéaire Les
 [PDF] Les alcanes et les alcools - Physique - Chimie
[PDF] Les alcanes et les alcools - Physique - Chimie
I/ L'identification des alcanes et des alcools 1/ Les différents types de squelettes carbonés Les alcanes et les alcools sont des molécules organiques
 [PDF] Nomenclature des alcanes et des alcènes - Nicole Cortial
[PDF] Nomenclature des alcanes et des alcènes - Nicole Cortial
1°) Généralités : Un n-alcane est un alcane où chaque atome de carbone est lié au maximum à deux atomes de carbone
 [PDF] alcanes Courspdf - CELENE
[PDF] alcanes Courspdf - CELENE
ALCANES ????? 41 Ce sont les constituants principaux des pétroles et du gaz Si on donne la vitesse 1 à la chloration d'un carbone primaire on a :
 [PDF] Chapitre 3: Nomenclature en chimie organique
[PDF] Chapitre 3: Nomenclature en chimie organique
Un hydrocarbure est une molécule comportant uniquement des atomes de carbone et d'hydrogène 2 1 1 Hydrocarbures acycliques saturés linéaires : Les alcanes sont
 [PDF] Chimie organique 1 (cours) Nomenclature des alcanes alcènes et
[PDF] Chimie organique 1 (cours) Nomenclature des alcanes alcènes et
Nomenclature des alcanes alcènes et alcools 1 Les alcanes a Définition : ce sont des hydrocarbures saturés (donc formés à partir d'atomes de carbone et
 [PDF] cour-chimie-organique-S2-2017-2018pdf
[PDF] cour-chimie-organique-S2-2017-2018pdf
1 Département de Chimie Support de cours de chimie organique Chapitre VI : Hydrocarbures aliphatiques (Alcanes ; Alcènes ; Alcynes) I Les alcanes :
Quels sont les différents alcanes ?
4C4H10 n-butane 5 C5H12 n-pentane 6 C6H14 n-hexane 7 C7H16 n-heptane Quels sont les 4 premiers alcanes ?
Alcanes à chaîne carbonée non ramifiée Les quatre premiers alcanes (1 < n < 4) portent des noms consacrés par l'usage : méthane, éthane, propane, butane.Quelles sont les formules des alcanes ?
Dénommés également paraffines, les alcanes sont des hydrocarbures acycliques saturés de formule générale CnH2n+2. On peut les représenter symboliquement par la notation RH, où R correspond à un groupe alkyle (CnH2n+1). Ils ne comportent que des liaisons carbone-carbone simples.- Hydrocarbure saturé à chaîne ouverte, de formule générale CnH2n+2.
NOMENCLATURE EN CHIMIE ORGANIQUE
La nomenclature permet de :
a) Trouver le nom d'une molécule connaissant la structure. b) Trouver la structure d'une molécule connaissant le nom.1. Hydrocarbures (HC) saturés acycliques : les alcanes
Les hydrocarbures saturés ne sont formés que de carbone et d'hydrogène. Nom : préfixe correspondant au nombre de carbones de la chaîne + terminaison aneNombre de C Préfixe Nombre de C Préfixe
1 méth 8 oct
2 éth 9 non
3 prop 10 déc
4 but 11 undéc
5 pent 12 dodéc
6 hex 13 tridéc
7 hept
Ex. CH 3 -CH 2 -CH 2 -CH 31) 4C but
4 carbones : préfixe but, HC saturé : terminaison ane butane
2. Hydrocarbures saturés ramifiés acycliques
chaîne principale ramification La ramification est un substituant (ou un radical) qui est accroché à la chaîne principale.Un radical prend une terminaison en yle.
Ex. CH 3 -CH 2 - éthyle 22.1. Numérotation de la chaîne
La chaîne principale est celle qui possède le plus grand nombre de carbone. Les indices indiquant l'emplacement des radicaux doivent être les plus petits possibles.1 2 3 4 5 6
6 5 4 3 2 1
Numérotation correcte
CH 3 CH 2 CH 2 CH CH 3 CH 2 CH 33-méthylhexane
Dans le nom, les substituants ne prennent pas de e ; terminaison yl Les substituants sont placés avant le groupe principal.S'il y a plusieurs groupes substituants, ils sont placés par ordre alphabétique (sans les préfixes
multiplicateurs). S'il y a plusieurs fois le même groupe dans la molécule, on utilise un préfixe : nb de substituants identiques Préfixe 2 di 3 tri4 tétra
2.2. Indices et signes
Règles générales (valables pour tous les composés) :- Les indices de position sont placés immédiatement avant la partie du nom à laquelle ils se
réfèrent. - Les indices sont reliés à la fonction par un tiret.- S'il y a plusieurs indices qui se rapportent à la même partie, ils sont séparés par une
virgule. CH 3 CH 2 CH 2 CH 2 CH CH 2 CH 3 CH 31234567
3-méthylheptane
CH 3 CH 2 CH 2 CH CH 3 CCH 2 CH 2 CH 3 CH 2 CH 3 CH 2 CH 3123456789
5-éthyl-4,5-diméthylnonane
32.3. Ramifications multiples
CH 3 CH 2 CH 2 CH 2 CH CH CH 2 CH 3 CH 3 CH 2 CH 2 CH 2 CH 2 CH 312345678910
2 1 3 toujours n°1- Les chaînes latérales sont numérotées à partir du carbone lié à la chaîne principale.
- Si nécessaire, le nom de la chaîne secondaire est mise entre parenthèses.1) Chaîne principale : décane
2) Indice de substitution principal : 5
3) Nom du radical ramifié : 5-propyl
4) Nom de la ramification secondaire : 1-méthyl
5-(1-Méthylpropyl)décane
3. Hydrocarbures insaturés acycliques
3.1. Hydrocarbures à doubles liaisons : les alcènes
Le nom d'un HC insaturé avec double liaison est formé par le préfixe de l'HC saturé correspondant. La terminaison ane devient ène Ex.1 2 3 4 5 6
CH 3 -CH=CH-CH 2 -CH 2 -CH 31) 6C hex
2) 1 double liaison en position 2
hex-2-èneS'il y a plusieurs doubles liaisons :
Nb de doubles liaisons Terminaison
2 diène
3 triène
6 5 4 3 2 1
CH 3 -CH=CH-CH 2 -CH=CH 21) 6C hex
2) 2 doubles liaisons en position 1et 4
hex-1,4-dièneDénomination non systématique :
CH 2 =CH 2éthylène (et non éthène)
43.1.1. Substituant à doubles liaisons
ATTENTION :
dans le cas des composés insaturés, la chaîne principale n'est pas forcément la plus longue mais celle qui contient le plus d'insaturations. - Terminaison : ényle (ényl dans le nom)Dénomination non-systématique :
CH 2 =CH- vinyle (et non éthényle) CH 2 =CH-CH 2 - allyle (et non prop-2-ényle) Ex. 1234 56
7
3-propylhept-1-ène
3.2. Hydrocarbures à triples liaisons : les alcynes
Le nom d'un HC insaturé avec triple liaison est formé par le préfixe de l'HC saturé correspondant. La terminaison ane devient yne.CHC CH
2 CH 2 CH 3 12345pent-1-yne
Avec plusieurs triples liaisons :
CHC CCCH
3 12345pent-1,3-diyne
CHC CCCCH
hexatriyneDénomination non-systématique :
HC CH acétylène (et non éthyne)3.2.1. Substituant à triples liaisons
-Terminaison : ynyle (ynyl dans le nom) 5 H 3 CCCCH 2 but-2-ynyle3.3. HC avec doubles et triples liaisons
On utilise le préfixe de l'HC saturé et une terminaisonényne.
Les liaisons multiples ont les indices les plus bas possibles. S'il subsiste un choix, la double liaison a l'indice le plus bas. CCH 2CHCHCH
2 12345pent-1-ène-4-yne
4. Hydrocarbures monocycliques saturés et insaturés
4.1. Hydrocarbures monocycliques saturés
Le nom d'un HC monocyclique saturé se forme en accolant le préfixe cyclo- au nom de l'HC acyclique saturé. H 2 CCH 2 CH 2 cyclopropane cyclohexane Les noms des radicaux sont obtenus en remplaçant la terminaison ane en yle (yl dans le nom). H 2 CCH 2 CH cyclopropyle cyclohexyle4.2. Hydrocarbures monocycliques insaturés
Comme un monocycle saturé avec une terminaison
ène, diène,..., yne, diyne, etc.
64.3. Hydrocarbures monocycliques aromatiques
Un composé mono- ou polycyclique est aromatique lorsque : 1)Il possède des doubles liaisons alternées.
2) Il comprend (4n + 2) électrons ; n étant un nombre entier. Ex.4n+2 électrons
alternanceouiouiouiouinonnon aromatique non aromatique non aromatique La plupart des HC monocycliques aromatiques ont un nom non-systématique :Benzène Toluène
CHH 3 CCH 3 CH=CH 2Cumène Styrène
CH 3 74.3.1. Substitution du cycle
La substitution est indiquée par des nombres.
Les substituants ont les indices les plus bas possibles. Si un choix subsiste, on prend l'ordre alphabétique.1-butyl-3-éthyl-2-propylbenzène
4.3.2. Radicaux aromatiques
CH 2 phénylebenzyle4.3.3. Polyaromatiques condensés
Il existe une grande variété de composés polycycliques dont les noms deviennent rapidement très compliqués. Nous ne nous intéresserons qu'à trois composés : naphtalène anthracène phénantrène 1 2 3 456781 2 3 4 567
89
10 1 2
3456789
10 La numérotation dans le sens des aiguilles d'une montre commence par le carbone le plushaut dans le cycle de droite, les carbones communs à plusieurs cycles ne sont pas numérotés.
Cette règle implique un positionnement correct de la molécule. L'anthracène fait exception à cette règle. 1238 CHquotesdbs_dbs6.pdfusesText_12
[PDF] les alcanes cours 1ere s
[PDF] formule alcane
[PDF] alcane groupe caractéristique
[PDF] alcane ramifié
[PDF] oxydation des alcools exercices corrigés
[PDF] taux de sulfate dans l'eau
[PDF] teneur en sulfate dans les sols
[PDF] écrouissage isotrope et cinématique
[PDF] écrouissage isotrope linéaire
[PDF] comportement non linéaire des matériaux
[PDF] la chine et l'afrique un nouveau partenariat pour le développement
[PDF] relation chine afrique
[PDF] la chine en afrique : enjeux et perspectives
[PDF] la chine populaire et l afrique
