 Physique chimie 4eme Chapitre 2 Combustion
Physique chimie 4eme Chapitre 2 Combustion
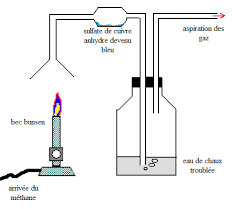
11 mai 2005 RÉALISATION DE LA COMBUSTION DU BUTANE AVEC UN BEC BUNSEN ... Exercice n°5 : Etude de la combustion du fer (5 Points). On fait brûler de la laine ...
 Devoir Surveillé n° 1 de Physique-Chimie
Devoir Surveillé n° 1 de Physique-Chimie
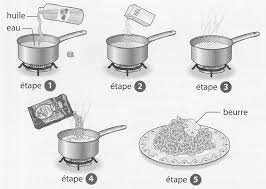
Quatrième. Page 2 sur 4. Exercice 1 – Et si on se faisait des pâtes ? (5 points) : Pour préparer des pâtes 5 étapes sont nécessaires : 1. Compléter le
 Tome 1 pollution (15 juillet)
Tome 1 pollution (15 juillet)
15 juil. 2023 différents combustibles visés par la loi organisent le contrôle des appareils de combustion et ... La quatrième réunion de Haut Niveau du ...
 La combustion du méthane
La combustion du méthane
Correction. Exercice 1 : Combustion du butane. 1. Le butane est composé de quatre atomes de carbone et de dix atomes d'hydrogène. 2. Formule: C4H10 . 3. Les
 correction exercices Précis de Physique-Chimie chapitre1 à 4
correction exercices Précis de Physique-Chimie chapitre1 à 4
6 fév. 2010 La suite de la résolution se fait comme la question 1 de l'exercice 9 de ce chapitre. Par comparaison avec la question précédente ces résultats ...
 Chapitre 5 : les combustions
Chapitre 5 : les combustions
Remarques : dans une combustion il y a un corps qui brûle le combustible (carbone) et un corps qui permet Correction. Exercice 8. Joséphine n'a pas raison ...
 Plus de bonnes notes
Plus de bonnes notes
20 nov. 2019 Exercice 1 : questions de cours (4 pts). 1- Lors d'une réaction chimique comme une combustion qu'est-ce qu'un réactif et qu'est-ce qu'un ...
 Untitled
Untitled
Lors de la combustion du butane il se forme du dioxyde de carbone et de l'eau. 3 Les combustions incomplètes. 4/ Combustion incomplète du butane. • On allume
 Chapitre 1 : Les trois états de la matière
Chapitre 1 : Les trois états de la matière
avec le dioxyde de carbone la poudre... et le combustible en réalisant une zone morte. Exercice 4. Pour brûler 10 g de carbone il faut 80 L d'air. Liste des ...
 Contrôle n°5
Contrôle n°5
Exercice 2 : Combustion du carbone. 5.5 pts. On réalise la combustion du carbone dans le dioxygène : 1) Quel(s) est(sont) le(s) réactif(s) ? 1 pt. Le carbone
 Contrôle n°5
Contrôle n°5
Une combustion est une réaction chimique qui dégage de la chaleur et dont l'un 3) Lors de l'expérience schématisez (avec une légende) le test qui t'a ...
 Correction du devoir de chimie n°1 (4e) Exercice 1 : Atomes et
Correction du devoir de chimie n°1 (4e) Exercice 1 : Atomes et
3- Les réactifs de la combustion du carbone sont le carbone et le dioxygène car ils disparaissent au cours de la combustion. 4- Le produit de la combustion du
 Untitled
Untitled
Lors de la combustion du butane il se forme du dioxyde de carbone et de l'eau. 3 Les combustions incomplètes. 4/ Combustion incomplète du butane. • On allume
 0D/1D combustion modeling for the combustion systems
0D/1D combustion modeling for the combustion systems
18-Jul-2020 Cette thèse a été effectuée avec la collaboration du laboratoire PRISME de l'Université ... The correct evaluation of maximum cylinder.
 EVALUATION EXPERIMENTALE INDIVIDUELLE 4ème TP n°7 : La
EVALUATION EXPERIMENTALE INDIVIDUELLE 4ème TP n°7 : La
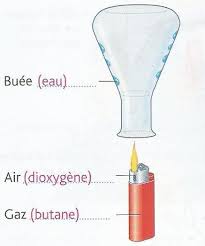
Lorsque le magicien approche l'allumette la paraffine brûle et réagit avec le dioxygène de l'air pour former de l'eau et un gaz ». Elle ne se souvient plus du
 Devoir de sciences physiques n°4 (Chimie) Note : /30
Devoir de sciences physiques n°4 (Chimie) Note : /30
3- Le bilan de la combustion du méthane (CH4) est le suivant : Le danger est donc bien réel pour toutes les personnes en contact avec la fumée de ...
 Design taking into account the partial discharges phenomena
Design taking into account the partial discharges phenomena
https://tel.archives-ouvertes.fr/tel-03124398/document
 4eme - Chimie - Corrigé Exercices chap 1 2 3
4eme - Chimie - Corrigé Exercices chap 1 2 3
Le nombre de molécule de dioxygène qui vont réagir avec le fer lors de la combustion des neuf atomes de fer est six.
 Communication Nationale du Maroc
Communication Nationale du Maroc
Technology Needs Assessment. TPE. Très Petite Entreprise. QCN. Quatrième Communication Nationale. UCA. Université Cadi Ayyad Marrakech.
 The development and combination of electromagnetic non
The development and combination of electromagnetic non
13-Dec-2013 evaluation techniques for the assesment of cover concrete condition ... electrode offset increases (ii) geometric correction by numerical ...
 Réglementation ICPE 2910 : focus sur les chaufferies entre
Réglementation ICPE 2910 : focus sur les chaufferies entre
Exercice n°3 : Ecrire le bilan de la combustion du butane : 4pts On étudie la combustion complète du butane Complétez le schéma suivant à l’aide des mots : dioxyde de carbone combustible comburant eau dioxygène produits butane réactifs Exercice n°4 : Prévenir un danger : 3pts
 Contrôle sur la combustion Quatrième - Plus de bonnes notes
Contrôle sur la combustion Quatrième - Plus de bonnes notes
Contrôle sur la combustion – Quatrième Exercice 1 : questions de cours (4 pts) 1- Lors d’une réaction chimique comme une combustion qu’est-ce qu’un réactif et qu’est-ce qu’un produit ? (2 pts) 2- Donner la définition d’une combustion (1 pts) 3- Quel est le test qui met en évidence le dioxyde de carbone ? (1 pts)
 CHP 4 les combustions - ac-versaillesfr
CHP 4 les combustions - ac-versaillesfr
4) Explication de la combustion du butane avec le modèle moléculaire : Vérifie que la citation de Lavoisier est bien respectée et que le nombre d’atome de carbone d’oxygène et d’hydrogène est bien conservé avant et après la réaction chimique en complétant le tableau ci-dessous :
 Searches related to evaluation combustion 4ème avec correction PDF
Searches related to evaluation combustion 4ème avec correction PDF
On réalise la combustion du carbone dans le dioxygène : 1) Quel(s) est(sont) le(s) réactif(s) ? 1 pt Le carbone et le dioxygène 2) Quel(s) est(sont) le(s) produit(s) ? 0 5 pt Le dioxyde de carbone 3) Lors de l’expérience schématisez (avec une légende) le test qui t’a permis de trouver le produit de la réaction 2 pt
Quelle est la fiche technique de combustion?
La fiche technique de combustion A - I précise que si la puissance d'un appareil est bridée, celle-ci est prise en compte à condition que la solution de bridage soit explicitement précisée dans le dossier de déclaration et que les mesures conservatoires permettant de la respecter soient mises en place. 41.
Quelle est la température de combustion d'un four?
La combustion commence sur charbon à une température de 1250 degrés. Par exemple, le four de fusion travaille sur charbon. La flamme qui est formée en étant alimenté avec de l'air four, fond facilement le métal. En raison du four à haute température tous les éléments internes sont en briques réfractaires spéciales.
Qu'est-ce que le phénomène de combustion ?
Lorsque votre voiture roule, un phénomène de combustion se déroule à l'intérieur de votre moteur, impliquant les pistons et les segments. En fonction de votre vitesse, ces deux éléments vont se déplacer des milliers de fois par minute. Pour limiter les dégâts de ce frottement, le moteur a besoin de lubrifiant pour fonctionner.
Comment calculer le cours de combustion ?
Cours de combustion : définitions et équations de combustion. Quantité d'oxygène nécessaire: 1 mole d'O 2 par mole de C, ou 32/12 = 2.67 kg d'O 2 par kg de carbone. Combustion de l'hydrogène: H 2 + 1/2 O 2 -> H 2 O, enthalpie D H R25°C = -241,6 kJ.mol -1, Quelques repères quand on parle de combustion: Pouvoir...
 >G A/, i2H@ykNykR3d ?iiTb,ffi?2b2bX?HXb+B2M+2fi2H@ykNykR3d am#KBii2/ QM R3 CmH kyky
>G A/, i2H@ykNykR3d ?iiTb,ffi?2b2bX?HXb+B2M+2fi2H@ykNykR3d am#KBii2/ QM R3 CmH kyky L8GBb KmHiB@/Bb+BTHBM`v QT2M ++2bb
`+?Bp2 7Q` i?2 /2TQbBi M/ /Bbb2KBMiBQM Q7 b+B@2MiB}+ `2b2`+? /Q+mK2Mib- r?2i?2` i?2v `2 Tm#@
HBb?2/ Q` MQiX h?2 /Q+mK2Mib Kv +QK2 7`QK
i2+?BM; M/ `2b2`+? BMbiBimiBQMb BM 6`M+2 Q` #`Q/- Q` 7`QK Tm#HB+ Q` T`Bpi2 `2b2`+? +2Mi2`bX /2biBMû2 m /ûT¬i 2i ¨ H /BzmbBQM /2 /Q+mK2Mib b+B2MiB}[m2b /2 MBp2m `2+?2`+?2- Tm#HBûb Qm MQM-Tm#HB+b Qm T`BpûbX
y.fR. +QK#mbiBQM KQ/2HBM; 7Q` i?2 +QK#mbiBQM bvbi2KbQTiBKBxiBQM Q7 bT`F B;MBiBQM 2M;BM2b
aQF`iBb .2K2bQmFb hQ +Bi2 i?Bb p2`bBQM, aQF`iBb .2K2bQmFbX y.fR. +QK#mbiBQM KQ/2HBM; 7Q` i?2 +QK#mbiBQM bvbi2Kb QTiBKBxiBQM Q7 bT`FÉCOLE DOCTORALE
LABORATOIRE PRISME
THÈSE présentée par
Sokratis DEMESOUKAS
17Discipline:
THÈSE dirigée par :
RAPPORTEURS :
Fabio BProfessore Ordinario, Università di Napoli "Federico II"Luis LE MOYNEProfesseur, Université de
JURY Xavier TAUZIAMaître de Conférences (HDR), École Centrale NantesDr. Ingénieur, IFP
Andrei BOIARCIUCDr. Ingénieur, Renault SAS
Modélisation 0D/1D de la combustion pour
teurs à allumage commandé0D/1D combustion modeling for the combustion
systems optimization of spark ignition engines5HPHUŃLHPHQPV
direction scientifique plusieurs fois. thèse CIFRE au sein de Renault. remercie M. Xavier Tauzia et M. Cédric Servant et M. Benoit Lorenzon pour avoir fourni les calculs 3D de mécanique des avec les dessins CAO. nous a donné uneFRQPHQPV
Chapter 1 Context of contemporary SI combustion engines design1.1 Introduction
1.2 Pollutant emissions and law
1.3 Carbon dioxide emissions and future goals
1.4 The Spark Ignition c
1.5 Solutions for the emissions and consumption reduction
1.5.1 Downsizing by turbocharging
1.5.2 Compression ratio adjustment
1.5.3 Variable Valve Actuation (VVA)
1.5.4 High Research Octane Number (RON) fuels
1.5.5 Mixture Dilution
1.6 Concise description of Spark Ignition combustion and emissions
1.6.1 Nitrogen Oxides (NOx)
1.6.21.6.3 Hydrocarbons (HC)
1.7 Research tools for development of Spark Ignition Combustion
1.7.1 Computational Fluid Dynamics tools
1.7.2 Tools for chemical processes description
1.7.3 0D System simulation
1.8 Objectives and structure of this work
Chapter 2 Turbulent premixed combustion: physics and models2.1 Laminar premixed flames
2.2 Flame stretch
2.3 Aerodynamic turbulence
2.2.4.1 Flame propagation inside the combustion chamber
2.5 Comparison of turbulent flame models
2.5.1 Laminar flame surface
2.5.2 Laminar flame speed
2.5.3 Aerodynamic turbulence
2.5.4 Eddy Burn Up model
2.5.5 Fractal model
2.5.6 Flame Surface Density model
2.5.7 Results and discussion of the comparison
2.5.8 Conclusion for the comparison of models
Chapter 3 Development and validation of a SI combustion model3.1 Piston kinematics
3.2 Nu
3.3 Two
3.3.1 Mass and energy conservation
3.3.2 Composition of each zone
3.4 Heat transfer
3.5 Reconstructed heat release rate
3.6 Flame Geometry
3.6.1 Concise description of the flame geometry model
3.6.2 Validation of geometric model
3.7 Overview of the combustion model
3.8 Turbulence
3.9 Flame
3.9.1 Quenching of laminar
3.9.2 Quenching of turbulent flames
3.9.3 Flame
3.10 Validation of f
3.10.1 Experimental setup
3.10.2 Validation results
3.3.12 Post flame reactions sub
3.12.1 Contribution of CO to the heat release rate
3.12.2 Contribution of HC to the heat release rate
3.13 Validation of post flame reactions sub
3.13.1 Experimental setup
3.13.2 Impact of CO on the heat release rate
3.13.3 Impact of HC on the heat release rate
3.14 Conclusion for the post
3.15 Impact of flame stretch
3.16 Validation of flame stretch sub
3.16.1 Experimental setup for flame stretch impact
3.16.2 Validation results for flame stretch impact
3.17 Conclusion for impact of flame stretch
Chapter 4 Model validation for different engine configurations4.1 Test bed engine description
4.2 Comparison with optimal advance angle engine test bed results
4.2.1 Typical evolutions of combustion variables in a cycle
4.2.3 Results for all operating points
4.3 Specific tests for sub
4.3.1 Fuel/air equivalence ratio variation
4.3.2 Gasoline/Ethanol fuel
4.3.3 Variable valve timing
Chapter 5 Conclusion and Perspective
5.1 Comparison of turbulent premixed combustion models
5.2 Flame
5.3 Post flame reactions
5.4 Impact of flame stretch on heat release
5.5 Model validation for different engine configurations
5.6 Perspective
Appendix A Thermodynamic model
A.1 System of differential equations
A.2 Composition of fresh gases zone
A.3 Composition of burnt gases zone
A.4Appendix B Geometric model
B.1 Burnt gas volume calculation
B.2 Mean flame surface calculation in function of the distance from the wallAppendix C Flame Surface density equation
Appendix D Supplementary results of optimal advance configuration Appendix E Résumé du manuscrit en français E.1 Contexte de la conception contemporaine des moteur à allumage commandéE.2 Combustion de pré
E.4 Validation du modèle pour des différentes configurations de moteurE.5 Conclusions et perspectives
References
Nomenclature
Abbreviations
0D Zero Dimensional (only function of time)
1D One Dimensional (only one spatial variable and time)
BDC Bottom Dead Center
CAD Computer Aided Design
CAXX Crank Angle when XX % of charge has been burntCFD Computational Fluid Dynamics
DEM Dilution Exponent Multiplier
DI Direct Injection
DNS Direct Numerical Simulation
EGR Exhaust Gases Recirculation
EVC Exhaust Valve Closing
EVO Exhaust Valve Opening
EXX Fuel with XX % volume fraction of ethanol and 1-XX % of gasolineFSD Flame Surface Density
HC HydroCarbons
IMEP Indicated Mean Effective Pressure
IVC Inlet Valve Closing
IVO Inlet Valve Opening
KPP Kolmogorov Petrovskii Piskunov
LES Large Eddy Simulation
LHS Left Hand Side
LHV Lower Heating Value
PFI Port Fuel Injection
RANS Reynolds Averaged Navier-Stokes
RBG Residual Burnt Gases
RHS Right Hand Side
RON Research Octane Number
SI Spark Ignition
TDC Top Dead Center
TKE Turbulent Kinetic Energy
VCR Variable Compression Ratio
VVA Variable Valve Actuation
VVL Variable Valve Lift
VVT Variable Valve Timing
Latin letters
A 2 cp, cv D D3 Da Dm 2 Dth 2 h HP hr J 2 K k Ka kf/b Ki L Le LT m M Ma NNtumble
p P Pe Q R Re Rf s sb Sc sL sR sT t T u U u V 3 v 3 X xb y Y yb ZeGreek letters
Ƚ Exponent for temperature (-)
Ⱦ Exponent for pressure (-)
ɀ Ratio of specific heats cp/cv (-)
Ȟ Efficiency function (-)
Ɂ Distance of the flame from the wall (m)
ɁL Laminar flame thickness (m)
Ɂp Thickness of preheat zone (m)
Ɂr Thickness of reaction zone (m)
ɂ Geometric compression ratio (-)
Ʉ Efficiency (-)
Ʌ Crank angle (deg)
Ɉ Flame stretch (sec-1)
ɉ Thermal conductivity (W/m/K))
Ɋ Wavenumber (m-1)
ɉT ȉM\ORU OHQJPO P
ɋ Kinematic viscosity (m2/sec)
ȩ Flame wrinkling (-)
ȭ Flame Surface Density (m2/m3)
ɔ Fuel/Air equivalence ratio (-)
ɘeng Engine speed (rad/sec)
Indices/Exponents
0 Typical definition
air Air b Burnt gases b Backwards (reaction) c Crevice d Displacement e Exhaust ent Entrainment eq Chemical equilibrium equ Wrinkling equilibrium f Forward (reaction) ff Flame front fl Full load free Free flame fuel Fuel i Inlet inf InfluenceL Laminar
P Piston
p Preheat pf Post flameQ Quenching
r ReactionST Stoichiometric
T Turbulent
t Turbulent u Fresh gases w WallChapter 1
1.1 One of the major challenges for spark ignition engines, as well as for any type of thermal Figure 1-1: Number of vehicles per 1000 inhabitants in various regions (Years 1999 and 2009) [2] 24,9157,7
101,2
620,9
169,7
363,9
583,3560,9
828,04
0 100200
300
400
500
600
700
800
900
Africa
East Asia,Middle
EastCanadaSouth
America
Europe,
EastEurope,
WestPacificUSA
Vehicles per 1000 inhabitants
20091999
Chapter 1: Context of contemporary SI combustion engines design 1.2According to specific studies
x, esp2, cause respiratory problems
Figure 1-2: Pollutant emissions limitations passenger vehicles with Spark Ignition engines in European Un-
ion. [5] x, CO and HC emi 1.3 As it1,E+00
1,E+01
1,E+02
1,E+03
1,E+04
Carbon
Monoxide CO
HydroCarbonsNon-Methanic
HCNOxHC+NOxParticulate
Matter
Emissions (mg/km)
Pollutants
Euro 1 (1994)Euro 2 (1998)Euro 3 (2000)Euro 4 (2005)Euro 5 (2009)Euro 6 (2014) Chapter 1: Context of contemporary SI combustion engines design2O) is 270 times more powerful as a global warming gas
2/km2/km in 2002. In the scope of a similar effort, various
Figure 1-3: Contribution of the various greenhouse gases to the problem of global warming [3] 64%19% 6% 5%5%
Carbon dioxide
Methane
Nitrous oxide
CFC 12
Other organic substances
Chapter 1: Context of contemporary SI combustion engines design Figure 1-4: Comparison of global CO2 regulations for passenger cars, in terms of NEDC gCO2/km. [7] 1.4 TheThis is why sometimes a SI engine is also
The value of fuel/air equivalence ratio ߮
݉) in the charge. When߮Ps, the mixture is rich (fuel in excess) and when ߮݉௨ௌ் (1-1)
Figure Figure During the intake stroke the
Chapter 1: Context of contemporary SI combustion engines designFigure 1-5: Strokes of a 4-stroke Spark Ignition engine. All four strokes make a cycle. The colored ar-
rows show the direction of the piston displacement. Figure 1-6: Duration of the four strokes of a SI engine. The overlap period when intake and exhaust valves are simultaneously opened is visible. 1Intake
SITop Dead Center (TDC)
Intake
Compression
E Chapter 1: Context of contemporary SI combustion engines designFigure 1-7: Ideal throttled constant volume cycle
(Otto cycle). Combustion is ideally considered to occur instantly so as that the volume does not change.Figure 1-8: Logarithmic (logP-logV) ideal throt-
tled constant volume cycle (Otto cycle). (See Figure1-7). Exhaust pressure is higher than intake pres-
sure due to the throttling.ൌL) is assumed, i
݉: fuel mass, ܳ
Pressure
Volume
IntakeCompression
CombustionExpansion
Exhaust
0 log(Pressure) log(Volume)IntakeCompression
CombustionExpansion
Exhaust
0 Chapter 1: Context of contemporary SI combustion engines design Figure 1-9: Typical LogP-LogV diagram of a SI engine functioning at part load. Applying logarithmpermits a more clear view of the different strokes, the valve openings and closings, the spark ignition as
well as the valve overlap period when intake and exhaust valves are open simultaneously. IVO/IVC stand
for Inlet Valve Opening and Closing and EVO/EVC stands for Exhaust Valve Opening and Closing. SI stands for Spark Ignition. IVC IVO EVO EVCIgnition
log(Pressure) log(Volume) 0 Chapter 1: Context of contemporary SI combustion engines design 1.5 Figure 1-10: Efficiencies of a three-way catalyst for the reduction of CO, NOx and HC emissions in function of fuel/air equivalence ratio ij [8]From the era of Euro 1 regulations,
x x x CO NOx HCStoichiometric
20 3040
50
60
70
80
90
100
0,980,9850,990,99511,0051,011,0151,02
Catalyst efficiency (%)
Fuel/Air equivalence ratio ij(-)
Chapter 1: Context of contemporary SI combustion engines design Figure 1-11: Comparative analysis in terms of cost of specific technologies for SI engines with re- duced CO2 emissions [9] 1.5.1Irrespective of displacement,
Conventional
PFIStratified DI
Turbo DI with
EGRTurbo, stratified
DITurbo, lean
charge DI 0 5 10 15 20 250102030405060
Reduction of CO
2emissions (%)
Cost increase of the control system (%)
Chapter 1: Context of contemporary SI combustion engines design 1.5.2 Figure 1-12: Comparison of main categories of friction losses: friction mean effective pressures atquotesdbs_dbs29.pdfusesText_35[PDF] combustion bougie 4eme
[PDF] qu'est ce qu'une combustion complète
[PDF] combustion complete d'un hydrocarbure
[PDF] combustion complète définition
[PDF] combustion incomplète du méthane
[PDF] exemple de combustion complète
[PDF] equation de combustion propane
[PDF] combustion complète de l'acétylène dans le dioxygène
[PDF] combustion ethane
[PDF] combustion de l'acétylène formule
[PDF] combustion incomplète des alcanes
[PDF] equation de combustion complete du glucose
[PDF] réaction exothermique
[PDF] réaction endothermique
