 Chapitre sur « les combustions » (classe 4e)
Chapitre sur « les combustions » (classe 4e)
La combustion est réaction vive au cours de laquelle on brûle un combustible à l'aide d'un comburant (dioxygène). Elle libère de la chaleur et de la lumière.
 PHYSIQUE - CHIMIE 4e
PHYSIQUE - CHIMIE 4e
Complète sans regarder le cours qui précède
 Physique chimie 4eme Chapitre 2 Combustion
Physique chimie 4eme Chapitre 2 Combustion
11 mai 2005 Pour découper une plaque de fer on la fait brûler avec un chalumeau dans un courant de dioxygène. Du dioxyde de carbone se forme-t-il au cours ...
 Chapitre 4 : Les combustions
Chapitre 4 : Les combustions
5- La combustion du carbone est une transformation chimique au cours de laquelle des réactifs disparaissent (le carbone et le dioxygène) et un produit apparaît
 Les transformations chimiques
Les transformations chimiques
Au cours de sa combustion le carbone réagit avec le dioxygène pour se transformer en dioxyde de carbone. -L'équation d'une réaction chimique traduit la
 Contrôle de chimie
Contrôle de chimie
Le barème est donné à titre indicatif. Exercice n°1 : Question de cours sur l'atome : Dans ce cas la combustion du méthane est-elle complète ou incomplète ?
 La combustion du méthane
La combustion du méthane
Dans cette combustion quel est le comburant ? 3. Que déduire si le sulfate de cuivre anhydre est devenu bleu pendant l'expérience ? 4. L'eau de chaux s
 Physique – 4ème - bilan période prévacances Thème : la matière
Physique – 4ème - bilan période prévacances Thème : la matière
Une combustion est une transformation chimique. ➔ Définir une transformation chimique (≠ transformation physique). ➔ Une transformation chimique peut
 Plus de bonnes notes
Plus de bonnes notes
20 nov. 2019 Exercice 1 : questions de cours (4 pts). 1- Lors d'une réaction chimique comme une combustion qu'est-ce qu'un.
 Le moteur thermique Transformer lénergie chimique en énergie
Le moteur thermique Transformer lénergie chimique en énergie
Dans le cycle à 4 temps au troisième temps moteur appelé combustion détente
 Chapitre sur « les combustions » (classe 4e)
Chapitre sur « les combustions » (classe 4e)
La combustion est réaction vive au cours de laquelle on brûle un combustible à l'aide d'un comburant (dioxygène). Elle libère de la chaleur et de la lumière.
 Chapitre 4 - Atomes et transformations chimiques
Chapitre 4 - Atomes et transformations chimiques
Au cours de la combustion du carbone un atome de carbone réagit avec une molécule de dioxygène pour former une molécule de dioxyde de carbone.
 CHP 4 : les combustions les combustions les combustions
CHP 4 : les combustions les combustions les combustions
Toutefois au cours de cette réaction chimique la masse n'a pas varié
 Physique chimie 4eme Chapitre 2 Combustion
Physique chimie 4eme Chapitre 2 Combustion
May 11 2005 Physique chimie 4eme. Chapitre 2 Combustion. Plan du cours: Introduction. Qu'est ce que brûler ? 1 – LA COMBUSTION DU CARBONE.
 PHYSIQUE - CHIMIE 4e
PHYSIQUE - CHIMIE 4e
4e. Livret de cours. Rédaction. Muriel Couret. Anne Sontag. Julien Gomba. Relecture Exprime l'équation chimique de la combustion complète du méthane :.
 Epreuves Communes 2014 corrigé
Epreuves Communes 2014 corrigé
1 Épreuve commune de Sciences Physiques 2014 – Classe de 4ème - Collège CHARLET Au cours de la combustion on a conservation de la masse totale.La.
 4eme - Chimie - Corrigé Exercices chap 1 2 3
4eme - Chimie - Corrigé Exercices chap 1 2 3
Physique Chimie - Corrigés d'exercices – niveau 4 ème. Exercice 6 page 49 (chapitre 1 du cours) combustion des neuf atomes de fer est six.
 Chapitre 4 : Les combustions
Chapitre 4 : Les combustions
5- La combustion du carbone est une transformation chimique au cours de laquelle des réactifs disparaissent (le carbone et le dioxygène) et un produit apparaît
 © Cours Pi Paris & Montpellier www.cours-pi.com
© Cours Pi Paris & Montpellier www.cours-pi.com
Bienvenue en 4ème ! de Quatrième avec le souci permanent de vous permettre de ... La combustion des hydrocarbures (essence
 4ème Interrogation COMBUSTION 4ème Interrogation COMBUSTION
4ème Interrogation COMBUSTION 4ème Interrogation COMBUSTION
4ème Interrogation COMBUSTION. Exercice 1 Choisir le bon mot. Au cours de la combustion du carbone le carbone et le dioxygène sont les produits / réactifs
 Leçon n°7 : La combustion du méthane et du butane
Leçon n°7 : La combustion du méthane et du butane
Leçon n°7 : La combustion du méthane et du butane Le méthane est le gaz naturel ; Le butane est le gaz contenu dans les briquets ou les camping-gaz L’unet l’autres’enflammentà la moindre étincelle : ce sont des gaz combustibles Leur combustion dégage beaucoup de chaleur
 Chapitre sur « les combustions » (classe 4e - ac-guyanefr
Chapitre sur « les combustions » (classe 4e - ac-guyanefr
La combustion du carbone est une transformation chimique au cours de laquelle : - des Réactifs sont consommés (le carbone et le dioxygène) - un produit se forme (du dioxyde de carbone) Bilan de la combustion du carbone: carbone + dioxygène dioxyde de carbone
 CHP 4 les combustions - ac-versaillesfr
CHP 4 les combustions - ac-versaillesfr
2) Explication de la combustion du carbone avec le modèle moléculaire : En utilisant le modèle moléculaire prépare les réactifs nécessaires pour la combustion du carbone À partir seulement de ces réactifs (sans te resservir dans la boite) construit le produit formé lors de la combustion du carbone
 Searches related to cours combustion 4ème PDF
Searches related to cours combustion 4ème PDF
La combustion du butane est un nouvel exemple de transformation chimique : Le utane (gaz) rûle dans l’air ave le dioxygène pour former deux nouveaux produits : l’eau et le dioxyde de arone Bilan de la combustion du butane : (En fait appelée combustion complète du butane donnant une flamme bleue )
Comment fonctionne la réaction de combustion?
•Conclusion : La réaction de combustion produit de la vapeur d’eau. Elle produit aussi du dioxyde de carbone. Résumons : Le méthane (ou le butane) réagit avec le dioxygène contenu dans l’air. Lorsqu’ily a assez de dioxygène, la combustion est complète (flamme bleue).
Qu'est-ce que la combustion du carbone ?
La combustion du carbone est la transformation par laquelle le carbone et le dioxygène réagissent entre eux. Le carbone et le dioxygène sont alors consommés et il se forme du dioxyde de carbone (mis en évidence par le test à l'eau de chaux). On active un briquet contenant du butane en dessous d'un tube à essai. On observe de la buée.
Quels sont les éléments nécessaires pour la combustion ?
Le réactif 1 réagit avec le réactif 2 pour former le produit 1. Pour qu'une combustion ait lieu, trois éléments sont nécessaires : Un combustible : le réactif susceptible de brûler (carbone, méthane, papier, bois, etc.). Un comburant : le réactif entretenant la combustion. Le plus souvent, le dioxygène (présent dans l'air) est le comburant.
Quels sont les effets de la combustion du méthane?
Elle produit aussi du dioxyde de carbone. Résumons : Le méthane (ou le butane) réagit avec le dioxygène contenu dans l’air. Lorsqu’ily a assez de dioxygène, la combustion est complète (flamme bleue). Cette combustion produit de l’eauet du dioxyde de carbone.

CHP 4 Page 1 sur 6 4ème
CHP CHP CHP CHP 4444 : : : : les combustionsles combustionsles combustionsles combustionsI) Une réaction chimique
1) Que se passe-t-il lors d"une réaction chimique :
Expérience :
On mesure à l"aide d"une balance la masse d"un flacon contenant de l"acide chlorhydrique, surmonté d"un ballon
de baudruche dans lequel on a disposé un morceau de craie. On note m initiale = .................. On fait tomber la craie dans le flacon et on observe la réaction chimique qui se produit.Lorsque la réaction chimique est terminée, on relève de nouveau la masse du récipient surmonté du ballon de
baudruche. On note m finale =.........................Observations :
On observe un dégagement gazeux : le ballon de baudruche gonfle. Au bout de 5 min la craie a disparue, la
solution a pris une couleur jaunâtre. Toutefois au cours de cette réaction chimique, la masse n"a pas varié, on a
m initiale = mfinaleInterprétation :
Lors d"une réaction chimique, des réactifs réagissent entre eux pour se transformer en de nouveaux
produits. Au cours de cette transformation, la masse ne change pas, donc " rien ne se perd, rien ne se
crée, tout se transforme » (citation de Lavoisier 1743-1794).2) Qu"est-ce qu"une combustion ?
Questions du document ci-dessous :
a. Quel est le verbe issu de la même famille que le nom " réactif » ? b. Comment sont appelés les 2 réactifs dans une combustion ? c. Cite un exemple pour chacun de ces deux réactifs. d. Quels sont les 3 facteurs qui doivent être réunis pour qu"une combustion ait lieu ? e. Quelles sont les formes d"énergie libérée par une combustion ?CHP 4 Page 2 sur 6 4ème
Extrait du livre Belin Parisi p 52
II) Combustion du carbone
1) Manipulations :
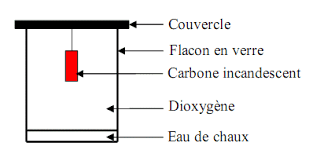
Expérience 1 : On fait brûler un morceau de fusain (carbone) à l"air à l"aide d"un briquet. Il est porté à incandescence. On l"introduit alors précipitamment dans un flacon rempli au préalable avec du dioxygène. On observe. Observation 1 : On remarque qu"une partie du fusain a disparu. Interprétation 1 : On a vu précédemment que rien ne se perd, rienne se crée, tout se transforme. C"est donc que le carbone disparu s"est transformé en gaz. Il se
pourrait que ce soit du dioxyde de carbone.Expérience 2 : On réalise alors le test à l"eau de chaux qui consiste à introduire un peu
d"eau de chaux (incolore) dans le flacon où a eu lieu la combustion du carbone. On agite le flacon et on observe. Observation 2 : L"eau de chaux se trouble elle devient blanchâtre. Interprétation 2 : On a vu en cinquième que l"eau de chaux mettait en évidence la présence de dioxyde de carbone. Cela confirme donc sa présence. Le carbone a donc réagit avec le dioxygène pour se transformer en dioxyde de carbone.Résumé : CARBONE +
DIOXYGÈNE DIOXYDE DE CARBONE
RÉACTIFS PRODUIT
CHP 4 Page 3 sur 6 4ème
2) Explication de la combustion du carbone avec le modèle moléculaire :
En utilisant le modèle moléculaire, prépare les réactifs nécessaires pour la combustion du carbone.
À partir seulement de ces réactifs (sans te resservir dans la boite), construit le produit formé lors de la
combustion du carbone. Complète alors le résumé ci-dessous en dessinant les modèles moléculaires.3) Equation chimique de la combustion du carbone :
L"équation ci-dessus s"écrit simplement à l"aide des symboles déjà appris au chapitre 2 :
C + O2 → CO2
III) Combustion du butane ou du méthane
1) Manipulation :
Expérience : La combustion du butane et du méthane génère les mêmes produits mais dans des proportions différentes. Nous n"allons expérimenter que celle du butane, mais interpréterons les deux. On place un récipient vide au-dessus d"une flamme bleue d"un bec bunsen. On verse ensuite de l"eau de chaux dans le récipient. Observation : On observe la formation de gouttelette d"eau le long des parois du tube. L"eau de chaux versée dans le tube à essai se troubleInterprétation : Comparé à la combustion du carbone, il apparait un nouveau produit : l"eau. Le butane se
transforme donc en réagissant avec le dioxygène pour former du dioxyde de carbone et de l"eau. Le butane et le dioxygène sont les réactifs. Le dioxyde de carbone et l"eau sont les produits.Remarque : On peut faire la combustion d"autres gaz tels que le méthane, le propane ... etc. Les produits de
tels combustions sont toujours les mêmes.CARBONE + DIOXYGENE → DIOXYDE DE CARBONE
BUTANE + DIOXYGENE → DIOXYDE DE CARBONE + EAU METHANE + DIOXYGENE → DIOXYDE DE CARBONE + EAU CARBONE + DIOXYGÈNE DIOXYDE DE CARBONE + EAUCHP 4 Page 4 sur 6 4ème
2) Explication de la combustion du méthane avec le modèle moléculaire:
Comme pour la combustion du carbone, construit les modèles moléculaires des réactifs de la combustion du
méthane.À partir de ces deux modèles moléculaires, reconstruit les produits obtenus lors de la combustion du méthane.
Attention il y a une difficulté : Pour respecter la citation de Lavoisier (rien ne se perd, rien ne se crée, tout se
transforme) tu ne dois pas laisser d"atomes seuls : tout doit se transformer. Tu peux utiliser plusieurs fois le
même réactif mais pas autre chose. Tu peux aussi obtenir plusieurs fois le même produit. Complète alors le résumé ci-dessous en dessinant les modèles moléculaires.3) Equation chimique de la combustion du méthane :
L"équation ci-dessus s"écrit simplement à l"aide des symboles déjà appris au chapitre 2 :
CH4 + 2 O2 → CO2 + 2 H2O
4) Explication de la combustion du butane avec le modèle moléculaire :
Vérifie que la citation de Lavoisier est bien respectée et que le nombre d"atome de carbone, d"oxygène et
d"hydrogène est bien conservé avant et après la réaction chimique en complétant le tableau ci-dessous :
Réactifs Produits
nombre d"atome de carbone nombre d"atome d"hydrogène nombre d"atome d"oxygène nombre d"atome de carbone nombre d"atome d"hydrogène nombre d"atome d"oxygène8 20 26 8 20 26
5) Équation chimique de la combustion de butane :
2 C4H10 + 13 O2 → 8 CO2 + 10 H2O
CHP 4 Page 5 sur 6 4ème
6) Méthode :
C + O2 → CO2
CH4 + 2 O2 → CO2 + 2 H2O
2 C4H10 + 13 O2 → 8 CO2 + 10 H2O
Les nombres placés devant les molécules s"appellent des coefficients stoechiométriques. Il y a une méthode pour ajuster ces coefficients stoechiométriques pour les réactions de combustions. La méthode consiste à ajuster les coefficients stoechiométriques dans l"ordre suivant :→ D"abord avoir le même nombre de C aussi bien du côté des produits que du côté des réactifs
→ Puis ajuster le nombre de H → Puis le nombre de OAppelons cela la méthode CHO !
L"équation de départ est la suivante :
...CH4 + .... O2 → .... CO2 + .... H2O
On compte d"abord le nombre d"atomes de carbone dans les réactifs. Ici il y en a 1. Il en faut donc autant dans
les produits.L"équation devient donc :
1 CH4 + .... O2 → 1 CO2 + .... H2O ou CH4 + .... O2 → CO2 + .... H2O
On compte ensuite le nombre d"atome d"hydrogène dans les réactifs. Ici il y en a 4 (dans CH4). Il en faut donc
autant dans les produits. La seule molécule contenant de l"hydrogène dans les produits est la molécule d"eau.
Pour obtenir 4 atomes d"hydrogène il faut multiplier cette molécule par 2.L"équation devient donc :
CH4 + .... O2 → CO2 + 2 H2O
Pour finir on compte le nombre d"atome d"oxygène dans les réactifs. Ici il n"y en a 2 (dans O2). Or dans les
produits il y en a 2 dans la molécule de CO2 et 2 dans 2 H2O. Donc au total 4. Pour en avoir autant dans les
réactifs, il faut multiplier par 2 la molécule de dioxygène.L"équation devient donc :
CH4 + 2 O2 → CO2 + 2 H2O
Appliquez cette même méthode pour établir l"équation de la réaction du butane.7) Énergie et combustions
Étude de document : combustion et énergie, comment fonctionne le moteur d"une voiture ?Vidéo :
CHP 4 Page 6 sur 6 4ème
III) Les dangers des combustions
1) Des combustions explosives
Vidéo : Minute de vérité : " La catastrophe du tunnel du Mont Blanc »Questions du documentaire
2) Des combustions incomplètes
Observation : On observe toujours la formation de gouttelette d"eau sur la coupelle, par contre cette fois-ci
apparait un dépôt noir sur la coupelle.Interprétation : En privant la combustion de dioxygène, il se forme de nouveau produits en plus du dioxyde de
carbone et de l"eau : il se forme du carbone ainsi que du monoxyde de carbone. Le monoxyde de carbone est un gaz inodore, incolore toxique et mortel. Il agit comme un gaz asphyxiant enprenant la place du dioxygène dans le sang. Il provoque maux de tête, nausée, fatigue et dans
les cas plus grave le coma voir le décès. En moins d"une heure ce gaz peut s"avérer mortel. Tous les appareils qui fonctionnent avec des combustibles come le bois, le charbon, le gaz, l"essence, le fuel, l"éthanol peuvent dégager du monoxyde de carbone s"ils ne sontC"est pour cela que toutes combustions nécessitent de l"oxygène et que les milieux de vie telle
que la cuisine doivent être convenablement aérée. BUTANE + DIOXYGENE → DIOXYDE DE CARBONE + EAU + MONOXYDE DE CARBONE + CARBONE On place une coupelle au dessus d"une flamme jaune d"un bec bunsen (auquel on a diminué l"arrivée d"oxygène en fermant la virole).quotesdbs_dbs29.pdfusesText_35[PDF] la comédie classique définition
[PDF] comedie heroique
[PDF] comédie classique théâtre
[PDF] origine du mot grotesque
[PDF] comédie classique auteurs
[PDF] air caraibes film a bord aout 2017
[PDF] air caraibes programme film aout 2017
[PDF] air caraibes film septembre 2017
[PDF] air caraibes film a bord juillet 2017
[PDF] air caraibes film aout 2017
[PDF] film air caraibes octobre 2017
[PDF] air caraibes film juillet 2017
[PDF] film air caraibe aout 2017
[PDF] aulularia plaute texte latin traduction
