 Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
COURS. ATOMISTIQUE/LIAISON CHIMIQUE. Réalisé par : Pr. Hamid MAGHAT. ANNEE UNIVERSITAIRE : 2017/2018. Page 2. Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU
 Chimie Générale (Chimie 1)
Chimie Générale (Chimie 1)
23 déc. 2020 ... Cours/Physique/S2/Chimie/Cours/liaisonchimique11_compre · sse.pdf. - La chimie. net - Liaisons chimiques. - Liaison chimique — Wikipédia.
 Chapitre III : La liaison chimique(Partie2)
Chapitre III : La liaison chimique(Partie2)
Cours de Chimie I-1ére année. Promotion électronique. 6C : 1s. 2. 2s. 2. 2p. 2. 6C : [He] 2s. 1. 2p. 3. 6C : [He] 2s. 1. 2p. 3. Chapitre III : La liaison
 cour-chimie-organique-S2-2017-2018.pdf
cour-chimie-organique-S2-2017-2018.pdf
Support de cours de chimie organique. Filière : STU-SV (S2). Réalisé par : Pr Une liaison covalente symbolisée par un trait
 Théorie des orbitales moléculaires (Approximation LCAO)
Théorie des orbitales moléculaires (Approximation LCAO)
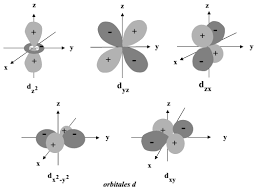
Cours de Liaisons Chimiques. Pr. EL AATIAOUI Abdelmalik. 5) Orbitales Dans le cas où la différence entre les niveaux d'énergie 2s et 2p est grande (17eV).
 Correction TD Liaison chimique –SMPC-S2 Série N°1 Exercice 4 : 1
Correction TD Liaison chimique –SMPC-S2 Série N°1 Exercice 4 : 1
2) Calculer la charge partielle (en coulomb) portée par chaque atome. 3) Calculer le caractère ionique partiel de cette molécule. Réponse (Voir le cours la page
 Les différents types de liaisons chimiques
Les différents types de liaisons chimiques
- intermédiaire entre liaison covalente et liaison ionique. - se produit lorsque Cours V. Fritsch. Page 8. - toutes les interactions vues précédemment ont ...
 LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
En 1916 deux classes de liaisons chimiques ont été décrites : la liaison ionique par Walther. Kossel (Allemagne) et la liaison covalente par G. N. Lewis
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
Pour cela le carbone doit être dans un état excité c-à-d un électron de la sous couche 2s passe à la sous couche 2p. Une liaison covalente π vient du ...
 Cours de chimie organique
Cours de chimie organique
Formation de la liaison : Deux Carbones hybridés Sp liés par une double liaison des liaisons (σ +. ). VI.3. Propriétés chimiques.
 Cours Liaison Chimique.pdf
Cours Liaison Chimique.pdf
Avant propos: Ce cours de La Liaison Chimique est destiné aux étudiants de 1er années des sciences vétérinaires. Cette présentation résulte de la lecture de
 Chapitre 4 :La liaison chimique
Chapitre 4 :La liaison chimique
Une liaison covalente c'est la mise en commun d'une ou plusieurs paires d'électrons par deux atomes. 4.0 International”. https://www.immae.eu/cours/ ...
 LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
En 1916 deux classes de liaisons chimiques ont été décrites : la liaison ionique par Walther. Kossel (Allemagne) et la liaison covalente par G. N. Lewis
 Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
Faculté des Sciences Meknès Cours ATOMISTIQUE SVTU/S1 Pr.H
COURS. ATOMISTIQUE/LIAISON CHIMIQUE. Réalisé par : Pr. Hamid MAGHAT l'orbitale 2s est représentée par la fonction d'onde : ?20
 Chimie Générale (Chimie 1)
Chimie Générale (Chimie 1)
Cours de Chimie Générale. Bendaoud-Boulahlib Yasmina. 2. Le chapitre (VII) est consacré à la liaison chimique (la liaison ionique la liaison covalente
 liaison chimique
liaison chimique
Chapitre III : La liaison chimique (première partie ). I -Définition : Département Tronc Commun. Cours de Chimie I-1ére année. 3. 8O : 1s. 2. 2s.
 COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE Semestre 2 SVI
COURS DE CHIMIE ORGANIQUE II/ NATURE ELECTRONIQUE DES LIAISONS EN CHIMIE ORGANIQUE ... électron de la sous couche 2s passe à la sous couche 2p.
 La chimie des polymères
La chimie des polymères
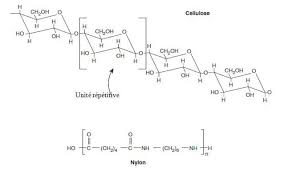
Support de Cours (Version PDF) -. La chimie des polymères La réticulation correspond à la formation de liaisons chimiques suivant les différentes.
 Cours de chimie organique
Cours de chimie organique
Filière : STU-SV (S2) Chapitre II : Nomenclature en chimie organique ... Une liaison covalente symbolisée par un trait
 Cours de Chimie Structure de la matière
Cours de Chimie Structure de la matière
Enfin ; Le sixième chapitre décrit les différents types de la liaison chimique. Page 3. Sommaire. Page 4. Sommaire.
UNIVERSITE CADI AYYAD
Faculté Polydisciplinaire
SafiDépartement de Chimie
COURS DE CHIMIE ORGANIQUE
Semestre 2
SVIPréparé par :
Moulay Rachid LAAMARI
2016-2017
SOMMAIRE
Chapitre I : INTRODUCTION A LA CHIMIE ORGANIQUE
I/ COMPOSES ORGANIQUES
II/ NATURE ELECTRONIQUE DES LIAISONS EN CHIMIE ORGANIQUEII-1- Orbitales atomiques (OA)
II-2- Valence du carbone
II-3- Hybridation du carbone
II-4- Liaisons covalentes
II-5- Comparaison entre sp3, sp2 et sp du carbone
II-6-Chapitre II : ECRITURE DES FORMULES ET FONCTIONS
EN CHIMIE ORGANIQUE
I/ ECRITURE DES FORMULES
I-1- Formule brute
I-2- Formule développée plane (FDP)
I-3- Formule semi-développée (FSD)
I-4- Formule simplifiée (FS)
II/ DIVERSES FONCTIONS ET GROUPEMENT FONCTIONNELS
II-1-II-2- Principales fonctions organiques
II-2-4- Fonctions tétravalentes
Chapitre III : PRINCIPALES REGLES DE NOMENCLATURE
DES COMPOSES ORGANIQUES
I/ NOMENCLATURE DES ALCANES ACYCLIQUES
I-1- Alcanes à chaîne linéaire
I-2- Alcanes à chaîne ramifiée
II/ NOMENCLATURE DES HYDROCARBURES ACYCLIQUES INSATURESII-1- Les alcènes : CnH2n
II-2- les alcynes : CnH2n-2
III/ NOMENCLATURE DES DERIVES HALOGENES (R-X)
IV/ NOMENCLATURE DES COMPOSES CYCLIQUES
IV-1- Les homocycles
IV-2- Les cycles aromatiques
IV-3- Les hétérocycles
V/ NOMENCLATURE DES FONCTIONS SIMPLES ET MULTIPLESV-1- Les alcools : R-OH
V-2- Les éthers (oxydes) : R-O-
V-3- Les amines
V-4- Les cétones : R-COR' avec R et R'
HV-5- Les aldéhydes : R-CHO
V-6- Acides carboxyliques : R-COOH
V-7- Dérivées des acides carboxyliques
VI/ NOMENCLATURE DES COMPOSES A PLUSIEURS FONCTIONSChapitre IV : ISOMERIE PLANE
I/ ISOMERIE DE CONSTITUTION
I-1-I-2- Isomérie de position
I-3- Isomérie de fonction
II/ ISOMERIE TAUTOMERIE
II-1-Tautomérie des aldéhydes et des cétonesII-2-Tautomérie des amides
II-3-Tautomérie des imines
Chapitre V : STEREOCHIMIE ISOMERIE CONFORMATIONNELLEI/ REPRESENTATION DES MOLECULES ACYCLIQUES
I-1- Molécule contenant un carbone sp3
I-2- Molécule contenant deux carbones sp3
I-3- Analyse conformationnelle des chaînes saturées aliphatiques II/ REPRESENTATON DES MOLECULES CYCLIQUES SATUREESII-1- Cyclopropane
II-2- Cyclobutane
II-3- cyclopentane
II-4- Cyclohexane
Chapitre VI : ISOMERIE OPTIQUE
I/ CHIRALITE
II/ MOLECULES CONTENANT UN SEUL CARBONE ASYMETRIQUEIII/ CONFIGURATIONS ABSOLUES R ET S
III-1- Règles de Cahn-Ingold et Prelog
III-2- Examen de la molécule
III-3- Projection de Fischer
IV/ Composés CONTENANT deux carbones asymétriques IV-1- Molécules possédant deux *C différents IV-2- Molécules possédant deux *C identiques CHAPITRE VII : ISOMERIE GEOMETRIQUE CISTRANS OU Z-EI/ ISOMERIE GEOMETRIQUE POUR LES ALCENES
I-1- ISOMERIE CIS-TRANS
I-2- ISOMERIE Z-E
II/ ISOMERIE GEOMETRIQUE CIS-TRANS POUR LES CYCLOALCANESII-1-DIMETHYLCYCLOBUTANE
II-2- DIMETHYLCYCLOHEXANE
CHAPITRE VIII : EFFETS ELECTRONIQUES
I/ EFFET INDUCTIF
I-1- E-I)
I-2-I-3- CONSEQUENCES DES EFFETS INDUCTIFS
II/ CONJUGAISON ET AROMATICITE
II-1- CONJUGAISON
II-2- AROMATICITE
III/ EFET MESOMERE
III-1- EFFET MESOMERE ATTRACTEUR (-M)
III-2- EFFET MESOMERE DONNEUR (+M)
Chapitre I : INTRODUCTION A LA CHIMIE ORGANIQUE
I/ COMPOSES ORGANIQUES
Les composés organiques sont des composés qui contiennent essentiellement du carbone sauf le monoxyde de carbone (CO), le dioxyde de carbone (CO2), les carbonates (K2CO3, Na2CO3, NaHCO3), les cyanures (KCN, NaCN), le dissulfure (CS2) et les carbures (CaC2) qui sont des composés inorganiques. Les composés organiques sont formés de liaisons covalentes. Ils sont rarement soluble dans l'eau et se décomposent facilement par la chaleur.Leurs densités sont voisines de l'unité.
II/ NATURE ELECTRONIQUE DES LIAISONS EN CHIMIE ORGANIQUE Pour décrire la nature des liaisons C-C et/ou C-H, on utilise la notion dépendent des nombres quantiques n, l et m (voir cours de chimie généraleI S1).
n : nombre quantique principale n>0, il détermine la distance moyenne entre l : 0< l < n, nombre quantique secondaire ou azimutal, il définit la sous couche, l = 0 orbitale s l = 1 orbitale p, etc. m : -l < m < l, nombre quantique magnétique, il définit la case quantique, à un niveau l correspond (2l + 1) valeurs (cases) de m.II-1- Orbitales atomiques (OA)
y a une grande proba organique sont s et p.II-1-1-
de la classification périodique des éléments. Il a sa couche externe à moitié remplie. Pour compléter sa couche périphérique, il pourra se lier à lui mêmeH He
Li Be B 6C N O F Ne
Na Mg Al Si P S Cl Ar
Le numéro atomique du carbone est 6 par conséquent sa structureélectroniques est 1s22s22p2.
II-1-2- Formes des OA du carbone
O. s y z x -1, 0, 1) correspond à 3 orbitales px, py et pz. Ces dernières ont chacune deux lobes et leurs axes de symétrie respectifs Ox, Oy et Oz sont perpendiculaires entre eux.Remarque: Le noyau se tr
II-2- Valence du carbone
r avec La configuration électronique externe du carbone à l'état fondamental est 2s22p2.2p22s2
Cette valence (VC = 2) permet la formation des molécules instables car la couche périphérique du carbone est incomplète (6e-, il faut 8e-).Exemple : CCl2
Octet (8e- sur la couche externe), le carbone
doit faire 4 liaisons donc il doit avoir 4 électrons célibataires sur sa couche externe (VC = 4). Pour cela, le carbone doit être dans un état excité c-à-d un électron de la sous couche 2s passe à la sous couche 2p.2p22s22p32s1
Excitation
Etat fondamentalEtat excité
Exemple : CH4 (8e- autour du carbone donc sa couche périphérique est saturée).Cette hypothèse tétravalence du
carbone (VC = 4) mais non pas sa géométrie qui se traduit parII-3- Hybridation du carbone
Une combinaison linéaire des OA conduit aux orbitales dites orbitales hydrides (OH) spatialement et énergétiquement équivalentes entre elles.2px 2py 2pz2s1
Etat excité
Par des différentes combinaisons linéaires des OA du carbone, on peut avoir3, sp2 et sp.
II-3-1- Hybridation sp3
re que les quatre liaisons C-H du méthane (CH4) sont identiques et indiscernables. Chacune forme avec les trois autres le même 2py et 2pz) du carbone subissent une combinaison linéaire pour donner 4 orbitales hybrides (OH). Cette combinaison met en jeu une orbitale s et 3 orbitales p pour conduire à quatre orbitales hybrides sp3 équivalentes.1 s+3 p4 sp3(4 OH)
px y z x pypz109°28'
sp3sp3 sp3 sp3 s Le carbone hybridé sp3 possède une géométrie tétraédrique.Remarque
II-3-2- Hybridation sp2
La combinaison linéaire met en jeu une orbitale s et deux orbitales p pour conduire à trois orbitales hybrides sp2 équivalentes dont leurs axes de inchangée et son axe de symétrie est perpendiculaire au plan des axes des orbitales hybrides sp2.1 s+2 p3 sp2(3 OH)
z pz120°
sp2 sp2 sp2 Le carbone hybridé sp2 possède une géométrie triangulaire.II-3-3- Hybridation sp
Elle met en jeu une orbitale s et une orbitale p pour conduire à deux orbitales hybrides sp dont les axes forment un angle de 180° et sont confondus. Les deux autres orbitales atomiques p (py et pz) restent naturelles et sont perpendiculaires aux deux orbitales hybrides sp.1 s+1 p2 sp(2 OH)
py pz spsp Le carbone hybridé sp possède une géométrie linéaire.II-4- Liaisons covalentes
Le carbone, situé sur la colonne centrale de la classification périodique, peut se lier à peut se lier à lui même, aux éléments de la mê des liaisons covalentes et . Une liaison covalente vient du recouvrement axial de deux orbitales hybrides (sp, sp2, sp3) dans le cas de la liaison C- et une orbitale s dans le cas de la liaison C-H. Une liaison covalente vient du recouvrement latéralII-4-1- Recouvrement axial
par rapport à ce même axe. Il aboutit à la formation de liaison covalente .Exemple 1 : méthane CH4 (4)
sp3sp3 sp3 sp3 s Csp3H HH H109°28'
La géométrie de CH4est tétraédrique
C H H H H +4H Conclusion : Un atome de carbone entouré de 4 liaisons est hybridé en sp3.Exemple 2 : éthane CH3-CH3
Chaque carbone est entouré de 3 liaisons (C-H) et une liaison (C-C). HH HH HHRecouvrement axial
Csp3Csp3
6H Le recouvrement axial C-C ié par rotation de la molécule autour de la liaison C-C; il y a la libre rotation autour de la liaisonII-4-2- Recouvrement latéral
Exemple 1 : éthylène CH2=CH2
pz' sp2sp2 sp2 pz sp2 sp2 sp2Recouvrement axial
Recouvrement latéral
H H H H 4H pour former une orbitale moléculaire (OM) correspondant à une liaison de type lèles. la liaison bloque la rotation autour de la liaison C-C. Conclusion : Un carbone hybridé sp2 est entouré de 3 liaisons et une liaison . Le carbone sp2 se trouve dans les molécules insaturés (doubles liaisons :C=O, C=S, C=N, C=C).
Exemple 2 : acétylène HCCH
conduire respectivement à deux liaisons perpendiculaires entre elles. Les trois liaisons Conclusion Un carbone hybridé sp est entouré de 2 et 2 . Il se trouve dans les molécules avec triple liaison et des molécules du genre C=C=C, C=C=O,C=C=N-, C=C=S.
II-5- Comparaison entre sp3, sp2 et sp du carbone
L'orbitale hybride sp3 est constituée de 25% de caractère s et de 75% de caractère p. Lorsque le caractère s de l'OH augmente on constate : - Aspect énergétiqueOA ns est plus faible que
- Aspect géométrique180°.
II-6-Le tableau ci-dessous rassemble les différe
sp3 sp2 spC 4 3 + 1 2 + 2
N 3 + 1 doublet libre 2 + 1 + 1 doublet libre 1 + 2 + 1 doublet libreO 2 + 2 doublets
libres1 + 1 + 2 doublets
libresChapitre II : ECRITURE DES FORMULES ET FONCTIONS
EN CHIMIE ORGANIQUE
Pour écrire une molécule organique, il faut respecter la valence des atomes qui constitue cette molécule. VC = 4, VN = 3, VO = 2, VH = V(F, Cl, Br, I) = 1.I/ ECRITURE DES FORMULES
En c - Formule brute, - Formule développée plane, - Formule semi-développée, - Formule simplifiée.I-1- Formule brute
que contient la molécule, elle est de la forme CxHyOzNtXw avec X = Cl, Br, I, F.Exemple :
- CH4N2O, elle contient (1C, 4H, 2N, 1O). - C3H6O, elle contient 3C, 6H et 1O. ne indication sur la façon dont les atomes sont disposés entre eux. En fait, il rapport aux autres.I-2- Formule développée plane (FDP)
Tous les atomes et toutes les liaisons sont représentés sur la surface plane d'une feuille. HCC H C H Cl H H H Cl HCN H C H H H H HHCO H H H ces atomes dans une molécule, mais non pas leur orientation réelle dansI-3- Formule semi-développée (FSD)
Dans cette écriture, on élimine les liaisons C-H, N-H et O-H.Exemples: CH3-CH3, CH3CH2-CH2-NH2, CH3-CH2-OH
Si en plus, on élimine les liaisons C-C, C-N, C- deviennent des formules compactes. Exemples: CH3CH2CH2CH3, CH3CH2OH, CH3NHOHI-4- Formule simplifiée (FS)
Du point de vue pratique et de simplification des écritures, on utilise pour les chaînes carbonées et les cycles des formules simplifiées. Dans ces formules, on ne garde que le squelette carboné sans nt porter. Par contre, on représente les hétéroatomes (N, O, S), les hydrogènes liés aux hétéroatomes et les halogènes (Cl, Br, I, F). Chaque extrémité et intersection du squelette correspondent à un carbone. Dans ces représentations, on respecte les angles de valence.CH3CH2CHCH2CH2C
O OHOH OCH2CHCHCHCH2C
NH2 CH ClCl NH2 H2CH2CCH2
CH2 CH2 H2C CH3 FSDFSExemple :
H2C NCH2 N CH H2C CH2CH3H3CNN
quotesdbs_dbs1.pdfusesText_1[PDF] liaison ionique et covalente
[PDF] liaison satellite pdf
[PDF] liaisons sociales classement master rh 2016
[PDF] liasse fiscale marocaine excel
[PDF] liasse fiscale syscohada excel systeme allégé
[PDF] liasse fiscale syscohada excel systeme normal
[PDF] liban 2011 maths s
[PDF] liban 2012 maths corrigé
[PDF] liban 2013 sujet maths
[PDF] liban 2014 physique
[PDF] liban 2016 bac svt corrigé
[PDF] liban 2016 maths es corrigé
[PDF] liban 2016 spé svt
[PDF] liban 2017 physique
