 Rappels chimie seconde
Rappels chimie seconde
RAPPELS DE SECONDE. FORMULAIRE DE CHIMIE. Utilisez les outils de l'analyse dimensionnelle pour mémoriser et contrôler ces relations ! La masse volumique ρ
 Chapitre 0 - Révisions du programme de Seconde
Chapitre 0 - Révisions du programme de Seconde
programme de physique chimie en classe de seconde. Les principaux chapitres concernent la structure de l'atome et de la matière les formules de chimie
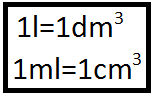 Les grandeurs physiques et leurs unités. (à connaître par cœur) Il ne
Les grandeurs physiques et leurs unités. (à connaître par cœur) Il ne
secondes. Page 3. Les expressions littérales « formules reliant différentes grandeurs physiques » (à connaître et à savoir utiliser). L'emploi de ces formules
 FORMULES DE PHYSIQUE-CHIMIE A CONNAITRE POUR LE
FORMULES DE PHYSIQUE-CHIMIE A CONNAITRE POUR LE
FORMULES DE PHYSIQUE-CHIMIE A CONNAITRE POUR LE BREVET. Formule à connaître : Formules « annexes » : Exemple : Page 1 sur 4
 Exercices de physique-chimie Seconde
Exercices de physique-chimie Seconde
`A partir de cette formule isolez la masse volumique ρ. 7/ Donner la valeur de la masse volumique de l'eau ρeau. Exercice 2. Le cyclohexane est
 Programme de physique-chimie de seconde générale et
Programme de physique-chimie de seconde générale et
Échelle microscopique : molécules atomes et ions
 Chapitre 1 La quantité de matière la concentration molaire et le
Chapitre 1 La quantité de matière la concentration molaire et le
Cette année on va aller encore plus loin en ajoutant des formules ! Je vais C'est une grandeur physique (car mesurable) qui s'exprime en mole de symbole ...
 Niveau : Seconde Type de ressources : Analyse documentaire
Niveau : Seconde Type de ressources : Analyse documentaire
Formules développées et semi-développées. •. Groupes caractéristiques. Capacités travaillées physique-chimie/enseignement/ressources- · documentaires/groupes ...
 Physique-Chimie-PSI-2020.pdf
Physique-Chimie-PSI-2020.pdf
9 juil. 2020 Le sujet comprend deux problèmes indépendants le premier de Physique et le second de. Chimie. • Les données et formules utiles à la résolution ...
 Fiche de révision de 3eme en physique chimie - DNB
Fiche de révision de 3eme en physique chimie - DNB
Formule chimique de l'ion g) Le son : fréquence. Un son est émis par la membrane d'un haut-parleur : Si la membrane vibre 1000 fois par seconde le son émis ...
 Rappels chimie seconde
Rappels chimie seconde
La densité d d'une espèce chimique solide ou liquide s'obtient en divisant sa masse volumique ? par celle de l'eau ?eau (les.
 Chapitre 0 - Révisions du programme de Seconde
Chapitre 0 - Révisions du programme de Seconde
programme de physique chimie en classe de seconde. Les principaux chapitres concernent la structure de l'atome et de la matière les formules de chimie
 FORMULES DE PHYSIQUE-CHIMIE A CONNAITRE POUR LE
FORMULES DE PHYSIQUE-CHIMIE A CONNAITRE POUR LE
FORMULES DE PHYSIQUE-CHIMIE A CONNAITRE POUR LE BREVET. Formule à connaître : Formules « annexes » : Exemple : Page 1 sur 4
 Les grandeurs physiques et leurs unités. (à connaître par cœur) Il ne
Les grandeurs physiques et leurs unités. (à connaître par cœur) Il ne
Il ne faut pas confondre une grandeur physique et son unité. peuvent se calculer en utilisant une expression littérale que l'on appelle formule.
 LIVRET DE REVISION SPECIALITE PHYSIQUE-CHIMIE
LIVRET DE REVISION SPECIALITE PHYSIQUE-CHIMIE
Vous pouvez retrouver des formules que vous allez aborder en 1ere spé qui n'ont pas été vu en seconde grâce aux unités ! À vous de jouer ! Grandeurs à trouver.
 DEVOIR SURVEILLE - SCIENCES PHYSIQUES
DEVOIR SURVEILLE - SCIENCES PHYSIQUES
Formule développée. Formule semi-développée sciences physiques et chimiques - Seconde http://cedric.despax.free.fr/physique.chimie/.
 Exercices de physique-chimie Seconde
Exercices de physique-chimie Seconde
`A partir de cette formule isolez la masse volumique ?. 7/ Donner la valeur de la masse volumique de l'eau ?eau. Exercice 2. Le cyclohexane est un solvant
 Physique Chimie
Physique Chimie
???/???/???? Physique Chimie Nathan pour le Cycle 4 ... Matériaux et propriétés physiques . ... Deuxième méthode :le coefficient de proportionnalité.
 La mole Ce quil faut retenir La mole : Exercices dapplication niveau
La mole Ce quil faut retenir La mole : Exercices dapplication niveau
Les formules suivantes sont à connaître : Chimie soutien seconde seconde. Exercice IV. Un flacon contient 800 mL de chlorododécane liquide de masse ...
 Chimie Premier exercice : Liaisons chimiques (65 points) Deuxième
Chimie Premier exercice : Liaisons chimiques (65 points) Deuxième
Écrire la formule ionique et la formule statistique de ce composé. 4. Expliquer la liaison chimique établie entre le phosphore et le chlore. Donner la formule.
RAPPELS DE SECONDE FORMULAIRE DE CHIMIE
Utilisez les outils de l"analyse dimensionnelle pour mémoriser et contrôler ces relations ! La masse volumique rrrr ( "ro") d"une espèce chimique s"obtient en divisant la masse m d"un échantillon contenant cette espèce par son volume V. La valeur de la masse volumique dépend des unités choisies pour l"exprimer. 1 g g.mLmL m V- r = m mm .V VVr = Û = r Û =r exemples :ρeau = 1g.mL-1 = 1000g.L-1 = 1000kg.m-3
La densité d d"une espèce chimique solide ou liquide s"obtient en divisant sa masse volumique r par celle de l"eau reau (les deux masses volumiques étant exprimées dans la même unité). C"est une grandeur sans unité. La densité de l"eau est égale à 1 par définition. 1 1 g.mL eau g.mL d r=r eau eau d d.r= Û r = rr d : densité de l"espèce chimiqueρ : masse volumique de l"espèce chimique
ρeau : masse volumique de l"eau
Pour dénombrer les atomes ou les molécules contenus dans un échantillon, le chimiste les regroupe par paquets.La mole est un paquet de 6,02.10
23 entités (atomes, molécules,
ions par exemple). Ce nombre d"entités contenus dans une mole porte le nom de constante d"Avogadro. 1 A molmolN n .N
= A ANN n.N nN= Û =
N : nombre d"entités dans l"échantillon (sans unité) n : quantité de matière ("nombre de moles") d"un échantillon NA : constante d"Avogadro ⇒ NA = 6,02.1023mol-1 La masse molaire moléculaire M d"une espèce chimique est la masse d"une mole de molécules de cette espèce chimique. Elle se calcule en effectuant la somme des masses molaires atomiques de tous les atomes constituant la molécule et s"exprime en g.mol -1. exemple : M(H2O) = 2.MH + MO = 18,0g.mol-11g molg.mol
m n . M -= mm n.M nM= Û = m : masse d"un échantillon n : quantité de matière ("nombre de moles") d"un échantillonM : masse molaire ("masse d"une mole")
La concentration molaire C d"une espèce chimique se calcule en divisant la quantité de matière n de soluté (l"espèce dissoute dans la solution) par le volume V de la solution. 1 mol mol.L L nCV-= nC n C.VV= Û =C : concentration molaire
n : quantité de matière de soluté (l"espèce dissoute)V : volume de la solution
La concentration massique t d"une espèce chimique se calcule en divisant la masse m de soluté (l"espèce dissoute dans la solution) par le volume V de la solution. 1 g g.L L mtV-= mt m t.VV= Û = t : concentration massique m : masse de soluté (l"espèce dissoute)V : volume de la solution
Relation entre concentration molaire C d"un soluté et concentration massique t du même soluté dans la même solution ⇒111g.molg.L mol.L
m n.Mt M . CV V---= = = tt M.C CM= Û = Au cours d"une dilution, la quantité de matière nM contenu dans le prélèvement de solution mère est égale à la quantité de matière n F contenu dans l"intégralité de la solution fille. On utilise de la verrerie jaugée pour préparer une solution par dilution car elle est plus précise : Prélever VM de solution mère à l"aide d"une pipette jaugée de V M mL. Les introduire dans une fiole jaugée de V F mL. Ajouter de l"eau distillée jusqu"au trait de jauge et agiter. Remarque : Si le volume à prélever ne correspond pas au volume d"une pipette jaugée, on utilise alors une pipette graduée.Pipettes jaugées :
0,5mL / 1mL / 2mL / 5mL / 10mL / 20mL / 25mL
F F M MC .V C .V= F F
MMC .VVC=
CF : concentration de la solution fille
V F : volume de solution fille que l"on souhaite préparer CM : concentration de la solution mère
VM : volume prélevé dans la solution mère
F : facteur de dilution qui indique de combien de fois la concentration de la solution mère va être divisée lors de la dilution (F>1) M F F MC VFC V= =
F MVVF=quotesdbs_dbs14.pdfusesText_20[PDF] formules ratios commerciaux
[PDF] formules remerciements thèse
[PDF] formules vecteurs seconde
[PDF] fort de loncin
[PDF] fort l'écluse
[PDF] forte personnalité pdf
[PDF] fortrainjobs
[PDF] fortuneo
[PDF] forum accompagnant educatif et social
[PDF] forum bourse de casablanca
[PDF] forum capeps interne
[PDF] forum capes anglais
[PDF] forum capes anglais 2018
[PDF] forum capes maths 2017
