 LES REACTIONS DE COMPLEXATION 1. Les complexes 1.1
LES REACTIONS DE COMPLEXATION 1. Les complexes 1.1
LES REACTIONS DE COMPLEXATION. 1. Les complexes. 1.1 Définition. Un complexe est un édifice polyatomique formé d'un atome ou d'un cation central auquel sont
 REACTIONS DE COMPLEXATION
REACTIONS DE COMPLEXATION
Les réactions de complexation sont d'une Elle permet aussi de complexer certains ions susceptibles d'interférer au cours de la recherche d'autres ions.
 Chapitre II - Réactions de Complexation
Chapitre II - Réactions de Complexation
La réaction qui conduit à la formation du complexe est dite réaction de Complexation. Exemple. 2- Constante de Stabilité ou de formation. La constante d
 Polycope Complexation Tirage 2013 chap2
Polycope Complexation Tirage 2013 chap2
La réaction qui conduit à la formation du complexe est dite réactions de Complexation. Exemple. 2- Constante de Stabilité ou de formation. La constante d
 COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
RÉACTIONS DE COMPLEXATION. COURS DE CHIMIE-PCSI/MPSI/TSI-. ◇ Un ligand est dit polydentate s'il possède plusieurs doublets libres. Exemple. Ion
 Chapitre SA2_PSI Seconde période Plan du cours Complexation
Chapitre SA2_PSI Seconde période Plan du cours Complexation
Pour répondre à cette question écrire la réaction de dissociation du complexe
 Chapitre 2 : Réactions de complexation et de précipitation I
Chapitre 2 : Réactions de complexation et de précipitation I
logKfi. On définit aussi les constantes successives de dissociation Kdi = 1/Kfi. Complexation et précipitation. 1/3. Y Elmokhtari. Page 2. Cours de chimie
 COURS DE CHIMIE MPSI CHIMIE DES SOLUTIONS EL FILALI SAID
COURS DE CHIMIE MPSI CHIMIE DES SOLUTIONS EL FILALI SAID
1 - Calcul des constantes des réactions : ◮ Réaction de précipitation :Aℓ3+ + 3OH−. ⇋. Aℓ(OH)3. K1. K1 = 1. Ks. = 10−32. ◮ Réaction de Complexation :Aℓ(OH)
 Chimie analytique : Réaction de Complexation- 2ème année
Chimie analytique : Réaction de Complexation- 2ème année
Exemple : Noir d'ériochrome T. On utilise un indicateur de fin de réaction. On choisit le noir ériochrome T ou NET au cours du dosage des ions chlorure Ca2+
 COURS-Equilibre-complexe.pdf
COURS-Equilibre-complexe.pdf
III – EQUILIBRE DE COMPLEXATION CONSTANTES ASSOCIEES. 3-1 Couple accepteur On dit que la réaction de formation des complexes est quantitative
 LES REACTIONS DE COMPLEXATION 1. Les complexes 1.1
LES REACTIONS DE COMPLEXATION 1. Les complexes 1.1
LES REACTIONS DE COMPLEXATION. 1. Les complexes. 1.1 Définition. Un complexe est un édifice polyatomique formé d'un atome ou d'un cation central.
 Equilibres De Complexation
Equilibres De Complexation
Chimie analytique : Réaction de Complexation- 2ème année pharmacie Batna2- Pr. La réaction de complexation qui se produit au cours du dosage (R.P. avant ...
 Chapitre SA2_PSI Seconde période Plan du cours Complexation
Chapitre SA2_PSI Seconde période Plan du cours Complexation
Pour répondre à cette question écrire la réaction de dissociation du complexe
 Polycope Complexation Tirage 2013 chap2
Polycope Complexation Tirage 2013 chap2
La réaction qui conduit à la formation du complexe est dite réactions de Complexation. Exemple. 2- Constante de Stabilité ou de formation.
 Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
CHAPITRE IV : REACTIONS DE COMPLEXATION. 1. Définitions. 2. Coordinence et géométrie. 3. Nomenclature des complexes : 4. Constante globale de formation du
 COURS-Equilibre-complexe.pdf
COURS-Equilibre-complexe.pdf
III – EQUILIBRE DE COMPLEXATION CONSTANTES ASSOCIEES. 3-1 Couple accepteur/donneur. On écrit de la façon suivante la réaction de formation d'un complexe de
 complexes.pdf
complexes.pdf
réaction de complexation : utilisation d'agents chelatants (EDTA) pour doser les il faut trouver un indicateur coloré pour voir la fin de réaction.
 COURS DE CHIMIE MPSI CHIMIE DES SOLUTIONS EL FILALI SAID
COURS DE CHIMIE MPSI CHIMIE DES SOLUTIONS EL FILALI SAID
2.4 Aspet quantitatif d'une réaction chimique acide base A/B . . . . . . 12. 3 RÉACTIONS DE COMPLEXATION. 14. 3.1 Couple donneur/Accepteur .
 COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
Transformation chimique : C'est une transformation aux cours de laquelle il y On peut décomposer une réaction de complexation en une série de réactions.
 2020 Chimie organométallique des éléments de transition
2020 Chimie organométallique des éléments de transition
Intervenants : Vincent Gandon (cours) Sophie Bezzenine (TD)
 [PDF] LES REACTIONS DE COMPLEXATION 1 Les complexes - PC-STL
[PDF] LES REACTIONS DE COMPLEXATION 1 Les complexes - PC-STL
LES REACTIONS DE COMPLEXATION 1 Les complexes 1 1 Définition Un complexe est un édifice polyatomique formé d'un atome ou d'un cation central
 [PDF] Chapitre II - Réactions de Complexation - F2School
[PDF] Chapitre II - Réactions de Complexation - F2School
La réaction qui conduit à la formation du complexe est dite réaction de Complexation Exemple 2- Constante de Stabilité ou de formation
 [PDF] COURS-Equilibre-complexepdf
[PDF] COURS-Equilibre-complexepdf
III – EQUILIBRE DE COMPLEXATION CONSTANTES ASSOCIEES 3-1 Couple accepteur/donneur On écrit de la façon suivante la réaction de formation d'un complexe de
 [PDF] Polycope Complexation Tirage 2013 chap2
[PDF] Polycope Complexation Tirage 2013 chap2
La réaction qui conduit à la formation du complexe est dite réactions de Complexation Exemple 2- Constante de Stabilité ou de formation La constante d'
 [PDF] Equilibres De Complexation - opsuniv-batna2dz
[PDF] Equilibres De Complexation - opsuniv-batna2dz
Chimie analytique : Réaction de Complexation- 2ème année pharmacie Batna2- Pr La réaction de complexation qui se produit au cours du dosage (R P avant
 [PDF] Chapitre 2 : Réactions de complexation et de précipitation
[PDF] Chapitre 2 : Réactions de complexation et de précipitation
Cours de chimie des solutions Sup TSI Chapitre 2 : Réactions de complexation et de précipitation I Réactions de complexation 1 Définition
 [PDF] Plan du cours Complexation - Chimie en PCSI
[PDF] Plan du cours Complexation - Chimie en PCSI
Pour répondre à cette question écrire la réaction de dissociation du complexe calculer sa constante et calculer la concentration des ions [CN-] La limite
 [PDF] Chapitre 2 Équilibres de complexation
[PDF] Chapitre 2 Équilibres de complexation
? La réaction de complexation mise en jeu pour le titrage doit être unique c'est la raison pour laquelle les systèmes où ne peuvent se former qu'un seul
 [PDF] 2 – Equilibres de complexation
[PDF] 2 – Equilibres de complexation
2 – Equilibres de complexation 1 – Rappels : constantes caractéristiques Définitions : Constante de formation globale ?n du complexe MLn
 [PDF] Les réactions de complexation - Ressources STL et BTS
[PDF] Les réactions de complexation - Ressources STL et BTS
LES RÉACTIONS DE COMPLEXATION 1 LES COMPLEXES 2 NOMENCLATURE DES COMPLEXES 3 GÉOMÉTRIE DES COMPLEXES 4 LES CONSTANTES DE DISSOCIATION ET DE FORMATION
Lycée Jean DautetPCSI D.Lecorgne
Dé#inition:
coétalement,n.m. !Domaine : Chimie/Chimie physique. ! Définition : Action de déposer ensemble et simultanément, à la surface d'un liquide, deux espèces chimiques, l'une amphiphile et l'autre non amph iphile. ! Voir aussi : amphiphile, composé semi-amphiphile, cuve de Langmuir, sous-phase. ! Équivalent étranger : co-spreading.Source: Journal officieldu 15 juin 2003.
complexe,n.m. !Domaine : Chimie. ! Définition : Entité moléculaire f ormée par l'association de deux ou de plusieurs entités moléculaires, ioniques ou neutres; l'espèce chimique correspondante. ! Voir aussi : adduit, liaison de coordination. ! Équivalent étranger : complex.Source: Journal officieldu 18 avril 2001.
composé d'inclusion !Domaine : Chimie.! Définition : Composé dont l'un des composants forme une cavité de taille limitée ou un réseau cristallin dans lesquels sont logées la ou les entités moléculaires d'une seconde espèce chimique. ! Note : L'attraction entre l'hôte et la ou l es molécules incluses étant due à des forces de Van der Waals, il n'y a pas de liaisons chimiques fortes entre ces espèces. ! Voir aussi : clathrate, entité 24estuneliai sonacido-ba siqueausensdeLewis, d'intensitétrèsvariable, ainsidescomplexe strèsstabl esetd'autresbeaucoupmoi ns,cequ'onp eut ci-dessous. liaison axiale !Domaine : Chimie/Stéréochimie. ! Définition : Liaison perpendiculaire au plan contenant (ou passant au plus près de) la majorité des atomes du cycle. ! Note :1. Dans le cyclohexane en conformation en chaise, les liaisons axiales sont alternées et parallèles à l'axe de symétrie C 3 .2. Dans les cycles analogues mono-insaturés, les liaisons correspondant es issues d'atomes contigus à un at ome doublement lié sont dites "quasi-axiales » ou "pseudo-axiales». ! Voir aussi : conformation en chaise, liaison équatoriale. ! Équivalent étranger :axial bond.
Source: Journal officieldu 18 avril 2001.
liaison covalente !Domaine : Chimie. ! Définition : Liaison entre deux atomes résultant de la mise en commun de deux électrons provenant séparément de chacun d'eux. ! Équivalent étranger : covalentbond.Source: Journal officieldu 18 avril 2001.
liaison de coordination !Domaine : Chimie. ! Définition : Liaison entre deux atomes dans laquelle le doublet d'électrons commun ne provient que de l'un des deux atomes liés. ! Note :1. L'expression "liaison dative », considérée comme équivalente, n'est pas recommandée.2. On peut citer comme 84liaison équatoriale !Domaine :Chimie/Stéréochimie. ! Définition :Liaison parallèle au plan contenant (ou passant au plus près de) la majorité des atomes du cycle. ! Note :1. Dans le cyclohexane en conformation en chaise, les liaisons équatoriales sont parallèles à deux des liaisons du cycle.2. Dans les cycles analogues mono-insaturés, les liaisons cor respondantes issues d'atomes contigus à un atome doublement lié sont dites "quasi- équatoriales» ou " pseudo-équatoriales». ! Voir aussi :conformation en chaise, liaison axiale. ! Équivalent étranger :equatorial bond.
Source: Journal officieldu 18 avril 2001.
ligand,n.m. !Domaine : Chimie. !Synonyme: coordinat, n.m. ! Définition : Atome ou groupe d'atomes lié à un atome central, génér alement métallique, dans une entité molécul aire polyatomiq ue. ! Équivalentétranger : ligand.
Source: Journal officieldu 18 avril 2001.
ligne de contact !Domaine : Chimie/Chimie physique. ! Définition : Ligne correspondant à l'intersection apparente de deux interfaces contiguës. ! Note :1. Dans le cas d'un film liquide, la ligne de contact le sépare de son bord de Plateau.2. L'expression "ligne de raccordement» 86[Cu(NH 3 4 2+
Tétraamminecuivre(II)4
[Al(H 2 O) 6 3+Hexaaquaaluminium(III)6
[Fe(SCN)] 2+Thiocyanatofer(III)1
[Fe(CN) 6 3-Hexacyanoferrate(III)6
[Fe(CN) 6 4-Hexacyanoferrate(II)6
SiO 3 4-Trioxosilicate(IV)4
-OHH 2 O NH 3SCNCl-
1 doublet pour se lier à l'atome central2 doublets pour se lier à l'atome central
H 2 NCH 2 CH 2 NH 26 doublets pour se lier à l'atome central
NCH 2 CH 2 N CH 2 CH 2 -OOCH 2 CCOO- H 2CCOO--OOC
IILesconstante sd'équilibres associéesauxréac 5onsde complexa5on1.Constantedeformation
1.1.Constanteglobaledeformation
Constanteglobaledeformationducomplexe:
M+nL=MLn
n ML n .c° n M .L nConstantesuccessivedeformationK
fn du complexe: constanted'équilibrede laréactionde formationducomplexeML n-1 etd'unligandL: ML n-1 +L=ML n K fn n n-1ML.c°
ML.L2.Constantedeformationsuccessive
[1]Cu 2+ +NH3=[Cu(NH3)] 2+Kf1=1,0.10
4,2 [2][Cu(NH3)] 2+ +NH3=[Cu(NH3)2] 2+Kf2=1,0.10
3,4 [3][Cu(NH3)2] 2+ +NH3=[Cu(NH3)3] 2+Kf3=1,0.10
3 [4][Cu(NH3)3] 2+ +NH3=[Cu(NH3)4] 2+Kf4=1,0.10
2 [1]Cu 2+ +NH3=[Cu(NH3)] 2+Kf1=1,0.10
4,2 [2][Cu(NH3)] 2+ +NH3=[Cu(NH3)2] 2+Kf2=1,0.10
3,4 [3][Cu(NH3)2] 2+ +NH3=[Cu(NH3)3] 2+Kf3=1,0.10
3 [4][Cu(NH3)3] 2+ +NH3=[Cu(NH3)4] 2+Kf4=1,0.10
2 [5] Cu 2+ + 4 NH3 = [Cu(NH3)4] 2+ b4 On remarque que : [5] = [1] + [2] + [3] + [4], relation de laquelle on en déduit :K°5 = K°1.K°2.K°3.K°4
Soit, en utilisant les notations précédemment introduites : b4 = Kf1. Kf2. Kf3. Kf4ConstantesuccessivededissociationK
dn du complexe: constanted'équilibrede laréactionde dissociationducomplexeenlecomplexeML n-1 et unligandL: ML n =ML n-1 +LK dn1.Diagrammedeprédominance
Onpeutd éfinirun coupleDonneur/Accepteurde
AH+ A HDonneur Accepteur Particule
ÈchangÈe
ML n ML n-1 LDonneur Accepteur Particule
ÈchangÈe
-n1 n dn [ML] pL=pK+Log() [ML]2.Diagrammededistribution
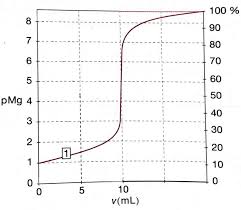
2.Diagrammededistribution
4,36,28,0
1.Exempl e1:étudedeladissociationd'uncomplexe
A une concentration d e 1,0.10
-2 mol .L -1 , une solution de [Fe(CN) 6 4- est -elle dangereuse pour la santé dans la mesure où elle peut libérer des ions CN ? Pour répondre à cette question, écrire la réaction de dissociation du complexe, calculer sa constante, et calculer la concentration des ions [CNLa limite légale admissible est de 1,0
g.L -1 de CNDonnéesà25°C:
Constantededissociationducomplexe[Fe(CN)
6 4- [Fe(CN) 6 4- =Fe 2+ +6CN K d =10 -35Massesmolairesatomiqueseng.mol
-1 :H:1C:12N:14Pb:2071.Exemple2: complexationcompétitive
L'ionfer(III)donneaveclesionssulfateSO
4 2- uncomplexe[Fe(SO 4 2 deconstanteglobalede formaBon 2 tel lequeLog 2 = 7,4; ildonneave cles ionscyan ureuncomplexe hexacoordiné[Fe(CN) 6 3- deconstanteglobaledeformaBon' 6 tellequeLog' 6 =31.1.Nommerlecomplexe[Fe(SO
4 22.OnconsidèreunesoluBondenitratedef er(III)Fe(NO
3 3 -cesoli deesttotalement -2 mol.L -1 danslaquelleonadissouségalement dusulfatedesodiumNa 2 (SO 4 c'=5,0.10 -2 mol.L -1 .Montr erquelasoluBon Sainsiobten ueconBen tlesionsfer(III)6,0.10
-3 moledecyanuredesodium.3.1.Ecrirel'é quaBon-bilandelaréacBonquiseproduit;idenBfierl'accepteur,ledonneur
3.2.Faire l'inventairedes concentraBonsdesréacBfsiniBalement. Rechercher la
présentes.IV-Titragescomplexométriques:voirTP
quotesdbs_dbs45.pdfusesText_45[PDF] complexe cuivre ammoniaque
[PDF] prologue antigone sophocle analyse
[PDF] reaction de complexation definition
[PDF] soprano ferme les yeux et imagine toi mp3
[PDF] tp réaction de complexation
[PDF] ferme les yeux et imagine toi année de sortie
[PDF] complexation définition
[PDF] soprano blacko ferme les yeux et imagine toi mp3
[PDF] sulfate de cuivre + ammoniaque
[PDF] ferme les yeux et imagine toi wikipedia
[PDF] soprano ferme les yeux et imagine toi paroles
[PDF] soprano feat blacko mp3
[PDF] ferme les yeux et imagine toi date de sortie
[PDF] ferme les yeux citation
