 Réactivité de la Fonction Acide Carboxylique
Réactivité de la Fonction Acide Carboxylique
Ainsi à coté des alcools
 1.1. Oxydation dun alcool primaire ou dun aldéhyde 1.2
1.1. Oxydation dun alcool primaire ou dun aldéhyde 1.2
Divers réactifs permettent d'oxyder les alcools primaires et les aldéhydes en acides carboxyliques. Dans ce cas le nombre d'atomes de carbone.
 ACIDES CARBOXYLIQUES ET DÉRIVÉS Introduction
ACIDES CARBOXYLIQUES ET DÉRIVÉS Introduction
12 janv. 2016 L'hydroxyde de sodium (base minérale) convertit complètement un acide carboxylique en carboxylate correspondant. Le contre-ion sodium ne fait.
 2. Synthèse des dérivés dacides R C O O + R C O O NaOH H + NaH
2. Synthèse des dérivés dacides R C O O + R C O O NaOH H + NaH
Comment prépareriez-vous les acides carboxyliques suivants via un réactif de c) Réaction d'un acide carboxylique avec un chlorure d'acide en présence de.
 Chimie Chapitre 10 Terminale Sx
Chimie Chapitre 10 Terminale Sx
produire avec un acide carboxylique les phénols ne réagissant pas avec les acides. Les acides gras sont des acides carboxyliques comprenant de 12 à 20 ...
 THÈME: CHIMIE ORGANIQUE TITRE DE LA LEÇON : ACIDES
THÈME: CHIMIE ORGANIQUE TITRE DE LA LEÇON : ACIDES
Un élève en classe de Terminale C au Lycée Municipal de Williamsville a appris que le vinaigre contient un acide carboxylique et que les acides carboxyliques
 Oxyder les alcools en phase aqueuse
Oxyder les alcools en phase aqueuse
(acide carboxylique) et H2O côté droit. 2) Couple aldéhyde / alcool primaire. R - CHO / R – CH2OH. R - CHO + 2 H+ + 2 e- = R – CH2OH. 3) Couple acide ...
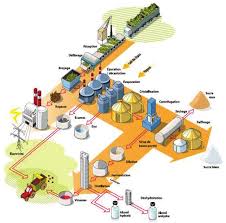 Valorisation catalytique dun acide carboxylique issu de lindustrie
Valorisation catalytique dun acide carboxylique issu de lindustrie
20 août 2020 GHB Acide gamma-hydroxybutyrique. Le GHB est un acide carboxylique naturel qui est produit dans le cerveau de l'organisme humain suite à l ...
 Procédé de distillation catalytique pour la récupération dun acide
Procédé de distillation catalytique pour la récupération dun acide
3 juin 2022 Dans cette optique des acides carboxyliques alpha hydroxylés tels que les acides glycérique
 Réactivité de la Fonction Acide Carboxylique
Réactivité de la Fonction Acide Carboxylique
à coté des alcools les acides carboxyliques ont un pKa beaucoup Dans une solution aqueuse à pH neutre (pH = 7)
 ACIDES CARBOXYLIQUES ET DÉRIVÉS Introduction
ACIDES CARBOXYLIQUES ET DÉRIVÉS Introduction
12 janv. 2016 Chimie organique II. Nomenclature des acides carboxyliques (suite). OH. O. HO. O acide éthanedioïque acide oxalique acide glutarique.
 Chapitre 23
Chapitre 23
acide carboxylique si l'oxydant est en excès. Remarque : l'aldéhyde formé lors de la première étape est facilement oxydable. Pour le conserver.
 NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
NOMENCLATURE EN CHIMIE ORGANIQUE 1. Hydrocarbures (HC
acide carboxylique acide ... oïque. Acides sulfoniques. -SO3H. Sulfo- acide ... sulfonique. Anhydrides d'acides. R-COOOC-R. - anhydride d'acide .
 Chimie Chapitre 10 Terminale Sx
Chimie Chapitre 10 Terminale Sx
Un anhydride d'acide est obtenu par déshydratation intramoléculaire de l'acide correspondant. Deux molécules d'acide carboxylique sont chauffées à 700°C
 Valorisation catalytique dun acide carboxylique issu de lindustrie
Valorisation catalytique dun acide carboxylique issu de lindustrie
20 août 2020 Hydrogénation catalytique des acides carboxyliques par des métaux ... Le GHB est un acide carboxylique naturel qui est produit dans le ...
 2. Synthèse des dérivés dacides R C O O + R C O O NaOH H + NaH
2. Synthèse des dérivés dacides R C O O + R C O O NaOH H + NaH
Avec tous les réactifs mentionnés il faut au préalable activer l'acide carboxylique en un intermédiaire plus réactif (RCOL). Après une réaction.
 Réaction destérification
Réaction destérification
acide carboxylique + alcool ? ester + eau. ? L'équation générale de la réaction associée à cette transformation chi- mique s'écrit : Exemple :.
 1.1. Oxydation dun alcool primaire ou dun aldéhyde 1.2
1.1. Oxydation dun alcool primaire ou dun aldéhyde 1.2
Hydrolyse d'un nitrile. En résumé pour : Divers réactifs permettent d'oxyder les alcools primaires et les aldéhydes en acides carboxyliques. Dans ce cas
NOMENCLATURE EN CHIMIE ORGANIQUE
La nomenclature permet de :
a) Trouver le nom d'une molécule connaissant la structure. b) Trouver la structure d'une molécule connaissant le nom.1. Hydrocarbures (HC) saturés acycliques : les alcanes
Les hydrocarbures saturés ne sont formés que de carbone et d'hydrogène. Nom : préfixe correspondant au nombre de carbones de la chaîne + terminaison aneNombre de C Préfixe Nombre de C Préfixe
1 méth 8 oct
2 éth 9 non
3 prop 10 déc
4 but 11 undéc
5 pent 12 dodéc
6 hex 13 tridéc
7 hept
Ex. CH 3 -CH 2 -CH 2 -CH 31) 4C but
4 carbones : préfixe but, HC saturé : terminaison ane butane
2. Hydrocarbures saturés ramifiés acycliques
chaîne principale ramification La ramification est un substituant (ou un radical) qui est accroché à la chaîne principale.Un radical prend une terminaison en yle.
Ex. CH 3 -CH 2 - éthyle 22.1. Numérotation de la chaîne
La chaîne principale est celle qui possède le plus grand nombre de carbone. Les indices indiquant l'emplacement des radicaux doivent être les plus petits possibles.1 2 3 4 5 6
6 5 4 3 2 1
Numérotation correcte
CH 3 CH 2 CH 2 CH CH 3 CH 2 CH 33-méthylhexane
Dans le nom, les substituants ne prennent pas de e ; terminaison yl Les substituants sont placés avant le groupe principal.S'il y a plusieurs groupes substituants, ils sont placés par ordre alphabétique (sans les préfixes
multiplicateurs). S'il y a plusieurs fois le même groupe dans la molécule, on utilise un préfixe : nb de substituants identiques Préfixe 2 di 3 tri4 tétra
2.2. Indices et signes
Règles générales (valables pour tous les composés) :- Les indices de position sont placés immédiatement avant la partie du nom à laquelle ils se
réfèrent. - Les indices sont reliés à la fonction par un tiret.- S'il y a plusieurs indices qui se rapportent à la même partie, ils sont séparés par une
virgule. CH 3 CH 2 CH 2 CH 2 CH CH 2 CH 3 CH 31234567
3-méthylheptane
CH 3 CH 2 CH 2 CH CH 3 CCH 2 CH 2 CH 3 CH 2 CH 3 CH 2 CH 3123456789
5-éthyl-4,5-diméthylnonane
32.3. Ramifications multiples
CH 3 CH 2 CH 2 CH 2 CH CH CH 2 CH 3 CH 3 CH 2 CH 2 CH 2 CH 2 CH 312345678910
2 1 3 toujours n°1- Les chaînes latérales sont numérotées à partir du carbone lié à la chaîne principale.
- Si nécessaire, le nom de la chaîne secondaire est mise entre parenthèses.1) Chaîne principale : décane
2) Indice de substitution principal : 5
3) Nom du radical ramifié : 5-propyl
4) Nom de la ramification secondaire : 1-méthyl
5-(1-Méthylpropyl)décane
3. Hydrocarbures insaturés acycliques
3.1. Hydrocarbures à doubles liaisons : les alcènes
Le nom d'un HC insaturé avec double liaison est formé par le préfixe de l'HC saturé correspondant. La terminaison ane devient ène Ex.1 2 3 4 5 6
CH 3 -CH=CH-CH 2 -CH 2 -CH 31) 6C hex
2) 1 double liaison en position 2
hex-2-èneS'il y a plusieurs doubles liaisons :
Nb de doubles liaisons Terminaison
2 diène
3 triène
6 5 4 3 2 1
CH 3 -CH=CH-CH 2 -CH=CH 21) 6C hex
2) 2 doubles liaisons en position 1et 4
hex-1,4-dièneDénomination non systématique :
CH 2 =CH 2éthylène (et non éthène)
43.1.1. Substituant à doubles liaisons
ATTENTION :
dans le cas des composés insaturés, la chaîne principale n'est pas forcément la plus longue mais celle qui contient le plus d'insaturations. - Terminaison : ényle (ényl dans le nom)Dénomination non-systématique :
CH 2 =CH- vinyle (et non éthényle) CH 2 =CH-CH 2 - allyle (et non prop-2-ényle) Ex. 1234 56
7
3-propylhept-1-ène
3.2. Hydrocarbures à triples liaisons : les alcynes
Le nom d'un HC insaturé avec triple liaison est formé par le préfixe de l'HC saturé correspondant. La terminaison ane devient yne.CHC CH
2 CH 2 CH 3 12345pent-1-yne
Avec plusieurs triples liaisons :
CHC CCCH
3 12345pent-1,3-diyne
CHC CCCCH
hexatriyneDénomination non-systématique :
HC CH acétylène (et non éthyne)3.2.1. Substituant à triples liaisons
-Terminaison : ynyle (ynyl dans le nom) 5 H 3 CCCCH 2 but-2-ynyle3.3. HC avec doubles et triples liaisons
On utilise le préfixe de l'HC saturé et une terminaisonényne.
Les liaisons multiples ont les indices les plus bas possibles. S'il subsiste un choix, la double liaison a l'indice le plus bas. CCH 2CHCHCH
2 12345pent-1-ène-4-yne
4. Hydrocarbures monocycliques saturés et insaturés
4.1. Hydrocarbures monocycliques saturés
Le nom d'un HC monocyclique saturé se forme en accolant le préfixe cyclo- au nom de l'HC acyclique saturé. Hquotesdbs_dbs7.pdfusesText_13[PDF] acide chlorhydrique danger
[PDF] acide chlorhydrique en anglais
[PDF] acide chlorhydrique et fer
[PDF] acide chlorhydrique francais
[PDF] acide chlorhydrique piscine
[PDF] acide éthanoïque
[PDF] acide formique
[PDF] acide fort def
[PDF] acide fort définition
[PDF] acide fort faible
[PDF] acide fort ou acide faible
[PDF] acide fort pka
[PDF] acide fumarique alimentation
[PDF] acide fumarique bac
