3 : Représentation des isothermes et adiabatiques réversibles : la transformation adiabatique Q
| Previous PDF | Next PDF |
 Transformation adiabatique dun gaz parfait
Transformation adiabatique dun gaz parfait
isotherme) Au cours d'une compression adiabatique, du travail s'effec- tue sur le gaz si bien que
 THERMODYNAMIQUE
THERMODYNAMIQUE
RMATION ISOTHERME : elle se fait à température constante T = Cte • TRANSFORMATION ADIABATIQUE : elle se fait sans échange de chaleur avec l' extérieur Q = 0 1 3
 Chapitre 13 : Transformations réversibles dun gaz parfait
Chapitre 13 : Transformations réversibles dun gaz parfait
rmation adiabatique réversible en partant de l'état initial TVp ,, La pression extérieure est 3 – Transformations isothermes réversibles d'un gaz parfait a) Transformation
 Le premier principe de la thermodynamique
Le premier principe de la thermodynamique
e isotherme d'un gaz parfait 13 Enthalpie en fonction de T à V constant 14 Détente adiabatique
 Chapitre VIII Les diagrammes thermodynamiques
Chapitre VIII Les diagrammes thermodynamiques
3 : Représentation des isothermes et adiabatiques réversibles : la transformation adiabatique Q
 Thermodynamique
Thermodynamique
rmation réversibles gaz parfait ∆S Adiabatique 0 Isocore Isobare Isotherme nR −1 ln T f
 ELEMENTS DE THERMODYNAMIQUE ET THERMIQUE I
ELEMENTS DE THERMODYNAMIQUE ET THERMIQUE I
Cité 12 fois — pour une transformation isotherme et Cpoly→0 pour un transformation adiabatique) En pratique, la
 Le Son et la Thermodynamique
Le Son et la Thermodynamique
rmnPDF
 TD4 – Premier principe de la thermodynamique - Sayede Adlane
TD4 – Premier principe de la thermodynamique - Sayede Adlane
lise la compression isotherme d'une mole de gaz parfait contenu dans un cylindre de section S Or Q = 0 car les parois sont athermanes, la transformation est donc adiabatique
[PDF] adres beyanı nasıl yapılır
[PDF] adresse mail france bleu lorraine nord
[PDF] adresse mairie 20 arrondissement paris
[PDF] advanced excel training ppt free download
[PDF] advanced french grammar exercises pdf
[PDF] advanced html tags list with examples pdf
[PDF] advanced inorganic chemistry by huheey pdf
[PDF] advanced java tutorial pdf tutorialspoint
[PDF] advanced javascript syllabus pdf
[PDF] advanced node.js development pdf
[PDF] advanced r programming pdf download
[PDF] advanced unix commands tutorial pdf
[PDF] advantages and disadvantages of flexible working hours
[PDF] advantages and disadvantages of international trade
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 80
Chapitre VIII. Les diagrammes thermodynamiques
Introduction.
Tout fluide (liquide ou gaz) à son état d'équilibre est caractérisé par des
grandeurs thermodynamiques (variables d'état ou fonctions d'état) (P, V, T, U, H, S).Equation caractéristique d'un fluide.
Soit f(x, y, z) = 0 avec x, y, z variables d'état. On peut mettre sous la forme z=f(x, y). Donc dans le plan (x, y), on peut tracer des courbes d'équation z = cte.VIII.1 : Diagramme de Clapyron (P, V).
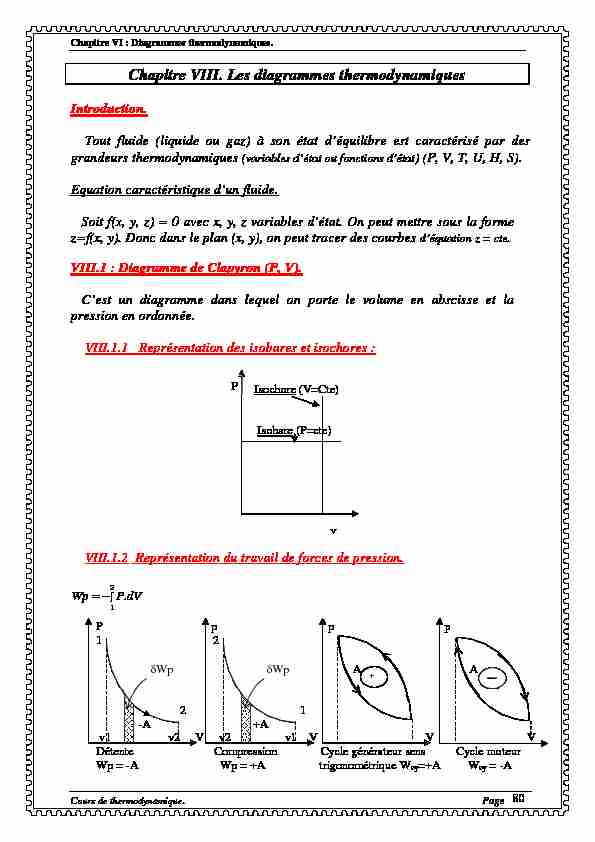
C'est un diagramme dans lequel on porte le volume en abscisse et la pression en ordonnée. VIII.1.1 Représentation des isobares et isochores : VIII.1.2 Représentation du travail de forces de pression. 21.dVPWp
Isochore (V=Cte)
Isobare (P=cte)
P vP p p p
1 2
Wp Wp A A 2 1 -A +Av1 v2 V v2 v1 V V V
Détente Compression Cycle générateur sens Cycle moteurWp = -A Wp = +A trigonométrique Wcy=+A Wcy = -A
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 81
VIII.1.3 : Représentation des isothermes et adiabatiques réversibles : Les isothermes sont représentées par des courbes d'équation P.V = cte ouP = Cte /V.
Ce sont des hyperboles équilatères. Les adiabatiques sont représentées par des courbes d'équation P .V = cte (voir chapitre gaz parfait). TV P : Pente au point M de la courbe qui représente la transformation isotherme. QV P : Pente au point M de la courbe qui représente la transformation adiabatique QV P TV P avec > 1 QV P TV P : Fluide monophasique.Remarque :
Les adiabatiques réversibles ont une forme compliquée à tracer, particulièrement pour des grandes variations de pression et de volume. Exemple : Turbine à vapeur ( Pression à l'admission 20 Bars, Pression à l'échappement 0,02 Bars. VIII.1.4 : Cas de la vapeur d'eau (fluide diphasique (Liq + Vap)Permet de calculer le titre
en vapeurConclusion :
Le diagramme de ClapyRon est commode à utiliser pour des considérations etétudes théoriques.
Pour lire des valeurs numériques et faire des calculs on utilisera les diagrammes Entropique et EnthalpiqueP Adiabatique (Q = 0)
QV P TV PIsotherme
VP C : point critique
Isotherme
C critique (Tc)
liq+ vapLiq Vap
Courbe de saturation
VIsotherme T Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 82
VIII.2 : Diagramme entropique (T, S)
Abscisse Entropie
Ordonnée température.
VIII.2.1 : Représentation des isothermes et isentropiques (adiabatiques et réversibles) VIII.2.2 : Quantité de chaleur échangée
A A dSTQ dSTQ iST QdS B A rev rev rev Q Q A B B A A B de réversibletion Transforma
BA de réversibletion Transforma
0 Remarque :
Analogie entre
2 1 .dvPWdans le diagramme (p, v) et B A revdSTQ. dans le diagramme (T,S). Cas d'un cycle :
Qrev = + A si le cycle est
parcouru dans le sens d'une aiguille d'une montre. Qrev = - A si le cycle est parcouru
dans le sens trigonométrique. T T
Isotherme T=cte T1 B C Cycle de Carnot
T2 A D
0 S S1 S2 S
Isentropique
S= cte T B TB TA A S T T
B B
+A -A A A
S S
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 83
W +Q = E = (U +Ec +Ep)
Pour un cycle réversible E = 0 Wrev +Qrev = 0 Wrev = - Qrev = -(We)rev Pour un cycle réversible, il y a donc équivalence entre l'aire mesurée sur le diagramme de Clapeyron et celle mesurée sur le diagramme entropique. VIII.2.3 : - Isochore et isobare d'un fluide à Cv et Cp constantes Isobare réversible Qrev = Cp.dT (dp = 0) dS = Qrev /T iS = 0 dS = Cp(dT /T) S = Cp Ln(T)+Cte Ln(T) = (S - Cte)/Cp ee
Cp S Cp CteS kT. Isochore réversible QREV = CvdT (dV = 0) dS =CteLnTCST dTCT Q vv rev V S ekT Les transformations isobares et isothermes réversibles sont représentées dans le diagramme (T.S) par des exponentielles. VIII.2.4 : Représentation de l'isobare et de l'isochore sur le diagramme (T, S) Plaçons nous en un point M du diagramme (T, S) et cherchons à situer l'isobare (l'isochore) en ce point. Soient
PVdS dTetdS dT les pentes des tanjentes à l'isobare et à l'isochore du point M arbitraire du diagramme (T, S).
Mpoint ceen isobar)l' tangnte(àla à supèrieure rsest toujou isochore)l' (à tangenteLa 1 PV v p P V v Cv Squotesdbs_dbs2.pdfusesText_3
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 82
VIII.2 : Diagramme entropique (T, S)
Abscisse Entropie
Ordonnée température.
VIII.2.1 : Représentation des isothermes et isentropiques (adiabatiques et réversibles)VIII.2.2 : Quantité de chaleur échangée
A A dSTQ dSTQ iST QdS B A rev rev rev Q Q A B B AA B de réversibletion Transforma
BA de réversibletion Transforma
0Remarque :
Analogie entre
2 1 .dvPWdans le diagramme (p, v) et B A revdSTQ. dans le diagramme (T,S).Cas d'un cycle :
Qrev = + A si le cycle est
parcouru dans le sens d'une aiguille d'une montre.Qrev = - A si le cycle est parcouru
dans le sens trigonométrique.T T
Isotherme T=cte T1 B CCycle de Carnot
T2A D
0 S S1 S2 S
Isentropique
S= cte T B TB TA A ST T
B B
+A -AA A
S S
Chapitre VI : Diagrammes thermodynamiques.
Cours de thermodynamique. Page 83