 Métropole 09/2008 EXERCICE III SIROP DE MENTHE (4 points
Métropole 09/2008 EXERCICE III SIROP DE MENTHE (4 points
Pour déterminer la concentration en colorant jaune et en colorant bleu dans le sirop, on réalise les expériences suivantes à partir du sirop de menthe dilué dix fois, d’une solution de tartrazine à 2,00 × 10 – 2 g L – 1 et d’une solution de bleu patenté V à 1,00 × 10 – 2 g L – 1
 Exercice - La physique cest sympathique
Exercice - La physique cest sympathique
b Justifier la présence d'un colo- rant bleu dans le sirop c À I 'aide des connaissances sur la synthèse soustractive des couleurs, donner la couleur du deuxième colorant présent dans le sirop d Proposer et décrire une expérience qui permettrait de confir- mer la présence des deux colorants dans le sirop Densité de l'acétone par
 Goût et couleur du sirop de menthe (10 points)
Goût et couleur du sirop de menthe (10 points)
méthode de dosage d’un colorant présent dans le sirop, le bleu patenté V, afin d’estimer la quantité maximale de sirop qui peut être consommé sans risque pour la santé 1 Goût de menthe : le menthol et ses dérivés Le menthol tire son nom de l’essence de menthe C’est un composé qui est utilisé
 Quels#colorants#sont#présents#dans#lesiropdementhe#?# Quelle#
Quels#colorants#sont#présents#dans#lesiropdementhe#?# Quelle#
La# lecture# de# l’étiquette# de# la# bouteille# d’un# sirop# de# menthe# indique#la#présence#de#deux#colorants#synthétiques#(n’existant#pas# dans#la#nature)#:E102##et#E131 # (Les#colorantsalimentairessont#desadditifsrepéréspar#un#code# défini#auniveaueuropéen#:lettre#E#suivie#d’un#nombre#de#100#à# 180 )#
 TP n°6 Dosage spectrophotométrique des colorants d’un sirop
TP n°6 Dosage spectrophotométrique des colorants d’un sirop
jaune D’où le nom de ce colorant Le bleu patenté E 131 a une absorbance maximale lorsqu’il est traversé par une longueur d’onde de 630 nm, ce qui correspond à la couleur orange Ce colorant est donc bleu Le sirop de menthe : En analysant le spectre d’absorption du sirop de menthe, on remarque qu’il possède deux
 Activité 1 : Séparation et identification des colorant d’un
Activité 1 : Séparation et identification des colorant d’un
Colorant : espèe solu le dans un milieu u’elle olo e Activité 1 : Séparation et identification des colorant d’un sirop de menthe On cherche à vérifier que le sirop de menthe vendu en France contient bien les 2 colorants indiqués su l’éti uette : tartrazine et bleu patenté V
 1 Observations préliminaires et identification
1 Observations préliminaires et identification
La couleur du sirop est le résultat d'une synthèse soustractive, le sirop absorbant dans le bleu et le jaune orangé, il transmet le vert 2 5 Donner la concentration du colorant E131 dans le sirop de menthe compte tenu de la dilution réalisée Rappeler la méthode L'utilisation de la courbe d'étalonnage (ou calcul du coefficient de
 Couleur menthe à leau Consignes Thème I - Observer
Couleur menthe à leau Consignes Thème I - Observer
Justifier à partir du spectre représenté, la couleur verte du sirop Quel type de synthèse de couleurs permet d'obtenir la couleur du sirop ? 2 5 Donner la concentration du colorant E131 dans le sirop de menthe Rappeler la méthode 2 6 Préciser pourquoi avec une courbe d'étalonnage pour le colorant E102, il n'aurait pas été possible de
 s780911a423139a5fjimcontentcom
s780911a423139a5fjimcontentcom
a En s'aidant de la courbe d'étalonnage, déterminer la concen- tration massique cm en colorant bleu du sirop dilué b En déduire la concentration massique c'm en bleu patenté V du sirop de menthe 4 La dose maximale admissible de bleu patenté V ingérab'ž par un être humain est de 2,50 mg par kg de masse corpore5e
[PDF] classification des roches magmatiques
[PDF] comment se forme une roche sédimentaire
[PDF] tableau de classification des roches sédimentaires
[PDF] caractéristiques des roches sédimentaires
[PDF] exercices les roches sedimentaires
[PDF] les différents types de roches sédimentaires
[PDF] classification des roches sédimentaires pdf
[PDF] formation des roches sédimentaires 5ème
[PDF] roches sédimentaires liste
[PDF] l'union de l'ame et du corps
[PDF] séparation du corps et de l âme
[PDF] ame et corps philosophie
[PDF] sujet d'examen hydrologie
[PDF] l'âme philosophie
 Métropole 09/2008 EXERCICE III. SIROP DE MENTHE (4 points) C alculatrice interdite Sur l'étiquette d'une bouteille de sirop de menthe, on peut lire les indications suivantes : Sucre, eau, sirop de glucose-fructose, arôme naturel de menthe, colorants :
Métropole 09/2008 EXERCICE III. SIROP DE MENTHE (4 points) C alculatrice interdite Sur l'étiquette d'une bouteille de sirop de menthe, on peut lire les indications suivantes : Sucre, eau, sirop de glucose-fructose, arôme naturel de menthe, colorants : E102- E131.
L'objectif de cet exercice est d'étudier une méthode d'extraction d'un arôme naturel de menthe puis
d'analyser les colorants contenus de ce sirop.Les parties 1 et 2 sont indépendantes.
1. Extraction de l'arôme naturel de menthe
L'arôme naturel de menthe est principalement dû à deux molécules : le menthol et la menthone que
l'on trouve dans l'huile essentielle de menthe. Cette dernière est extraite à partir des feuilles de
menthe.On donne quelques caractéristiques physiques :
Huile essentielle de
menthe Dichlorométhane Eau salée saturéeDensité par rapport à l'eau 0,9 1,3 1,1
Solubilité dans l'eau faible quasi nulle -
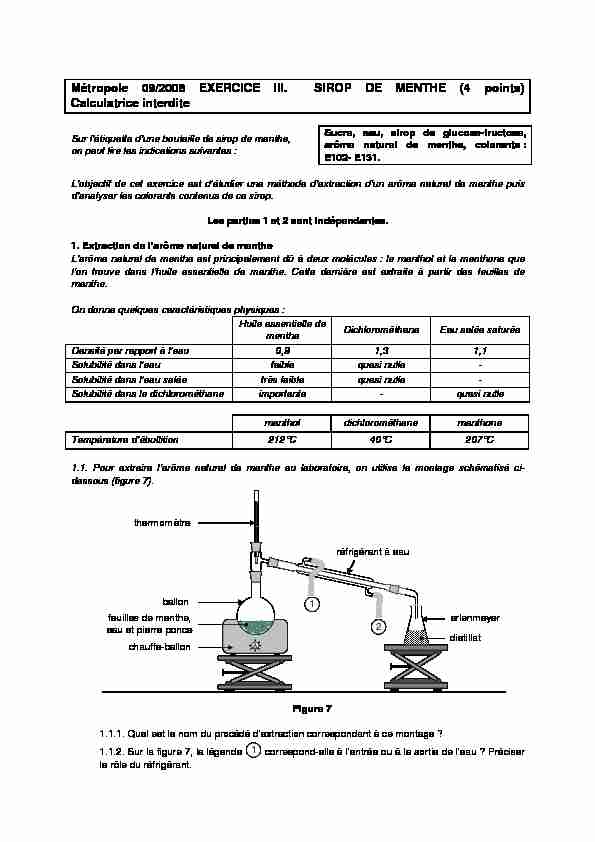
Solubilité dans l'eau salée très faible quasi nulle - Solubilité dans le dichlorométhane importante - quasi nulle menthol dichlorométhane menthone Température d'ébullition 212°C 40°C 207°C1.1. Pour extraire l'arôme naturel de menthe au laboratoire, on utilise le montage schématisé ci-
dessous (figure 7).Figure 7
1.1.1. Quel est le nom du procédé d'extraction correspondant à ce montage ?
1.1.2. Sur la figure 7, la légende
1 correspond-elle à l'entrée ou à la sortie de l'eau ? Préciser
le rôle du réfrigérant. réfrigérant à eau chauffe-ballon feuilles de menthe, eau et pierre ponce ballon distillat erlenmeyer thermomètre 1 21.2. Le distillat obtenu est trouble car il contient deux phases mal séparées : l'huile essentielle de
menthe et l'eau. Afin de faciliter leur séparation, on ajoute une solution aqueuse saturée de chlorure
de sodium dans le distillat recueilli. On place ensuite le contenu de l'erlenmeyer dans une ampoule à
décanter. On verse du dichlorométhane dans l'ampoule puis après agitation et décantation, on
recueille la phase organique. On ajoute du sulfate de magnésium anhydre à la phase organique afin
de la sécher. Après filtration, on procède à l'évaporation du solvant à l'aide d'un évaporateur rotatif
afin d'isoler l'huile essentielle de menthe.1.2.1. À l'aide du tableau des caractéristiques physiques, justifier l'ajout de chlorure de sodium
dans le distillat.1.2.2. Citer deux raisons qui justifient le choix du dichlorométhane comme solvant extracteur.
1.2.3. Faire un schéma de l'ampoule à décanter en indiquant la position des phases aqueuse et
organique obtenues. Justifier.2. Analyses qualitative et quantitative des colorants contenus dans le sirop
2.1. Chromatographie des colorants
On ne peut pas réaliser directement la chromatographie du sirop de menthe à cause de la présence
des sucres. On procède alors en deux étapes.Étape 1 : extraction des colorants.
Des brins de laine écrue (c'est-à-dire non teintée) sont trempés dans une solution d'ammoniac
pendant quelques minutes puis ils sont rincés et séchés. Ils sont ensuite placés dans un bécher
contenant du sirop de menthe. Les colorants contenus dans le sirop se fixent, à chaud et en présence
d'acide éthanoïque, sur les brins de laine. Après rinçage et essorage, les brins de laine teints en vert
sont placés dans une solution d'ammoniac où ils se décolorent. La solution verte obtenue est portée à
ébullition afin de la concentrer par évaporation d'eau. Cette solution est ensuite analysée par
chromatographie.Étape 2 : chromatographie.
Sur un papier filtre, on réalise les trois dépôts suivants : - colorant alimentaire E102 (tartrazine) - colorant alimentaire E131 (bleu patenté V) - solution verte obtenue S L'éluant utilisé est une solution de chlorure de sodium de concentration égale à 20 g.L - 1 . Le chromatogramme obtenu est schématisé ci-contre (figure 8).Figure 8
Données :
E102 E131
Solubilité dans une solution de
chlorure de sodium faible importante2.1.1. Une révélation du chromatogramme est-elle nécessaire ? Pourquoi ?
2.1.2. Le chromatogramme est-il en accord avec les indications portées sur la bouteille de
sirop ? Justifier la réponse.2.1.3. À partir des données, proposer une interprétation de la disposition relative des taches sur
le chromatogramme.E102 E131 S
tache bleue tache jaune2.2. Détermination de la concentration de chaque colorant dans le sirop par spectrophotométrie
Pour déterminer la concentration en colorant jaune et en colorant bleu dans le sirop, on réalise les
expériences suivantes à partir du sirop de menthe dilué dix fois, d'une solution de tartrazine à
2,00 × 10 - 2 g.L - 1 et d'une solution de bleu patenté V à 1,00 × 10 - 2 g.L - 1 .À l'aide d'un spectrophotomètre, on obtient les courbes donnant l'absorbance A en fonction de la
longueur d'onde λ pour les trois solutions. Les courbes obtenues pour les colorants sont représentéessur la figure 9 ci-dessous et celle obtenue pour le sirop de menthe dilué est représentée sur la
figure 10 DE L'ANNEXE. longueur d'onde λλλλ en nmabsorbance A00,10,20,30,40,50,60,70,80,9
360 400
440 480 520 560 600 640 680 720
Colorant jaune (tartrazine)
00,20,40,60,81,01
,21,41,6360 400 440 480 520 560 600 640 680 720
absorbance A longueur d 'ondeλλλλ en nm
Colorant bleu (bleu patenté V)
Figure 9
On réalise ensuite une échelle de teintes à partir des solutions de colorants. On mesure l'absorbance
de chaque solution à l'aide du spectrophotomètre en se plaçant à la longueur d'ondeλ1 = 450 nm
pour la tartrazine et à la longueur d'ondeλ2 = 640 nm pour le bleu patenté V.
On obtient (figure 11 DE L'ANNEXE) les graphiques A = f(c) pour chaque colorant alimentaire, cétant exprimée en mg.L
- 12.2.1. Pourquoi choisit-on de se placer à la longueur d'onde
λ = 450 nm plutôt que 420 nm pour
réaliser le dosage par étalonnage de la tartrazine dans le mélange?2.2.2. À partir des figures 10 et 11, déterminer graphiquement la concentration massique en
colorants jaune et bleu dans le sirop dilué. On fera apparaître clairement les constructions sur
les figures 10 et 11 DE L'ANNEXE.