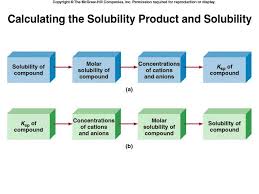
 Les solutions tampons
Les solutions tampons
solution tampon ne change pas appréciablement lorsqu'on ajoute des acides et des bases. • le pouvoir tampon est la capacité de la solution tampon à.
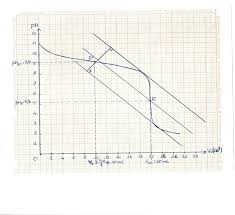 chimie générale réactions acide – base. solution tampon
chimie générale réactions acide – base. solution tampon
3.4 Pourquoi la solution est acide à l'équivalence. IV. Solutions tampons. 1. Composition d'une solution tampon. Au cours de la réaction entre un acide faible
 Une solution tampon est constituée par le mélange dun acide faible
Une solution tampon est constituée par le mélange dun acide faible
Conclusion : Le pH de la solution tampon ne varie pas par dilution. III-Limites de l'effet tampon : Si on continue de verser l'acide fort ou la base forte à
 Solutions tampons
Solutions tampons
Définition : Une solution tampon est une solution dont la composition est telle que son pH varie peu soit par addition de petites quantités d'acide ou de base
 MAEC et SIE : une solution en bordure de cours deau ?
MAEC et SIE : une solution en bordure de cours deau ?
25 janv. 2016 Zones tampons vis-à-vis des produits phytopharmaceutiques. Page 14. • Bordure d'une eau de surface : Zone tampon minimale de 6 mètres.
 Solution Tampon
Solution Tampon
Solution Tampon. • Ajout de base ou d'acide et dilution: impacts sur le PH. Page 2. Dosages. Page 3. Dosages (II). Page 4. Acide + Base. Page 5. Récapitulatif
 Fiche de Données de Sécurité: Solution tampon
Fiche de Données de Sécurité: Solution tampon
Solution tampon pH 1000 ±0
 Fiche de Données de Sécurité: Solution tampon pH 688 ±0
Fiche de Données de Sécurité: Solution tampon pH 688 ±0
https://www.carlroth.com/medias/SDB-T185-CH-FR.pdf?context=bWFzdGVyfHNlY3VyaXR5RGF0YXNoZWV0c3wyNDg0MjR8YXBwbGljYXRpb24vcGRmfHNlY3VyaXR5RGF0YXNoZWV0cy9oZTAvaGIyLzkwNTU0Mjk2NTY2MDYucGRmfDk5ZWY2ZGE4NDg4ZDVhYmUyYjQ2MWM4ZjZkODQ2N2Q0NGU2YzdjNTIxODQxN2UyNDJjOGE2NTVlYTc4OWZlZjc
 La chimie
La chimie
Les solutions tampons. • une solution tampon est une solution constituée. • d'un acide faible ou d'une base faible. • d'un sel de cet acide ou de cette base.
 Solutions tampons
Solutions tampons
(tampon à la dilution). Ainsi les solutions d'acide fort ou de base forte ne constituent pas de bonnes solutions tampons car si ce sont des tampons
 COURS DE CHIMIE GENERALE Semestre 1 SVI
COURS DE CHIMIE GENERALE Semestre 1 SVI
Solutions tampon. 3.1. Définition de la ST. 3.2. Propriété de la ST. 3.3. Préparation de la ST. 3.4. Calcul du pH de ST. 4. Titrages acide-base.
 Transformations chimiques en solution aqueuse
Transformations chimiques en solution aqueuse
Cours de chimie de seconde période de PCSI PSI UNE SOLUTION TAMPON EST UNE SOLUTION DONT LE PH VARIE PEU PAR UN APPORT MODERE D'ACIDE OU.
 Chapitre 1 Acides et bases
Chapitre 1 Acides et bases
Le pH (“potentiel hydrogène”) d'une solution défini par Søren Sørensen en 1909
 Chimie Chapitre 1 Terminale S
Chimie Chapitre 1 Terminale S
Pour les solutions aqueuses diluées le pH est égal à l'opposé du Une solution tampon est une solution dont le pH varie peu lorsqu'on y ajoute une ...
 reactions-acido-basiques.pdf
reactions-acido-basiques.pdf
TS – PHYSIQUE-CHIMIE – REACTIONS ACIDO-BASIQUES – COURS. 3. Echelle de p.H. Solution acide. p.H < 7. H3O+ > HO?. Solution neutre. p.H = 7. H3O+ = HO?.
 Solution Tampon
Solution Tampon
Solution Tampon. • Ajout de base ou d'acide et dilution: impacts sur le PH. Page 2. Dosages. Page 3. Dosages (II). Page 4. Acide + Base. Page 5
 Les Acides Aminés
Les Acides Aminés
Une solution tampon est une solution dont le pH varie peu soit pas addition d'acide soit par addition de base ou par dilution dans de l'eau. Le pouvoir tampn
 Solutions tampon Nancy
Solutions tampon Nancy
Une solution tampon est souvent un mélange d'acide faible et de sa base conjuguée Mobiliser les connaissances acquises au cours de l'activité 1 pour.
 [PDF] Solutions tampons
[PDF] Solutions tampons
Définition : Une solution tampon est une solution dont la composition est telle que son pH varie peu soit par addition de petites quantités d'acide ou de base
 [PDF] Les solutions tampons - La chimie
[PDF] Les solutions tampons - La chimie
Les solutions tampons • une solution tampon est une solution constituée • d'un acide faible ou d'une base faible • d'un sel de cet acide ou de cette base
 [PDF] Solutions tampon Nancy
[PDF] Solutions tampon Nancy
Une solution tampon peut être constituée d'un mélange d'acide faible et de sa base conjuguée Elle a un pH qui ne varie pas par ajout limité d'acide ou de base
 [PDF] Equilibre acidobasique
[PDF] Equilibre acidobasique
instantanés » automatiques : systèmes tampons Produit ionique de l'eau (toute solution aqueuse) : Appliquée au système tampon « bicarbonates /
 [PDF] Solution Tampon
[PDF] Solution Tampon
Solution Tampon • Ajout de base ou d'acide et dilution: impacts sur le PH Page 2 Dosages Page 3 Dosages (II) Page 4 Acide + Base Page 5
 [PDF] grenoble_première_CBSV_thème 1_Solutions tampon
[PDF] grenoble_première_CBSV_thème 1_Solutions tampon
L'objectif de cette activité est de préparer une solution tampon de pH donné et de montrer l'effet tampon Mots clés de recherche : tampon solution tampon
 [PDF] SOLUTIONS TAMPONS
[PDF] SOLUTIONS TAMPONS
SOLUTIONS TAMPONS 1) Définition Une solution tampon est une solution dont le pH varie peu par addition modérée d'un acide d'une base ou d'eau
 [PDF] Étude de solutions tampons (Manipulation de TCE ou TD)
[PDF] Étude de solutions tampons (Manipulation de TCE ou TD)
Nous allons ici étudier les variations de pH d'une solution tampon lors d'un ajout d'acide fort ou de base forte 2 ÉTUDE EXPÉRIMENTALE 2 1 Préparation des
 62 – Solutions tampons – La Chimie Générale pour les Gee-Gees
62 – Solutions tampons – La Chimie Générale pour les Gee-Gees
6 2 – Solutions tampons · 1 Un bon mélange tampon doit avoir des concentrations à peu près égales de ses deux composants · 2 Une solution tampon a généralement
 [PDF] Filière Sciences de la Matière Chimie Cours Chimie des Solutions
[PDF] Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Solutions tampon 3 1 Définition de la ST 3 2 Propriété de la ST 3 3 Préparation de la ST 3 4 Calcul du pH de ST 4 Titrages acide-base
Quel est le principe d'une solution tampon ?
Une solution tampon est un mélange d'acide faible et de sa base conjuguée ou d'une base faible et de son acide conjugué. On utilise des solutions tampons pour maintenir stable la valeur du pH d'une autre solution mélangée avec le tampon.Comment préparer une solution tampon PDF ?
Dissoudre les solides dans environ 100 mL d'eau distillée. Agiter. Quand tout est dissous, ajuster au trait de jauge avec de l'eau distillée; homogénéiser. Cette solution constitue la solution tampon.Quel est le rôle du tampon ?
Définition de tampon ??? nom masculin. Petite masse dure ou d'une matière souple pressée, qui sert à boucher un trou, à emp?her l'écoulement d'un liquide.- Préparation d'une solution tampon
Lorsque l'on est en présence d'un mélange équimolaire [A-] = [AH] , la relation pH = pKa + log[A-]/[AH] devient pH = pKa. La solution tampon a donc un pH égal au pKa du couple acide base mis en jeu. En chimie des solutions, elles sont notamment utilisées pour étalonner le pH-mètre.