 BPF PARTIE III : SYSTEME QUALITE PHARMACEUTIQUE (ICH Q10)
BPF PARTIE III : SYSTEME QUALITE PHARMACEUTIQUE (ICH Q10)
Ce document établit une nouvelle ligne directrice tripartite ICH qui décrit un modèle de système de management de la qualité efficace pour l'industrie
 Q3D : Directive concernant les impuretés élémentaires
Q3D : Directive concernant les impuretés élémentaires
29 janv. 2016 ... ICH. Ce processus aboutira à la modification ou si les révisions à ... Getting to the bottom of arsenic standards and guidelines. Environ ...
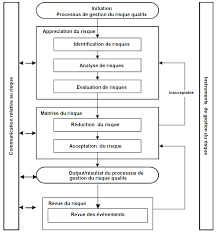 PARTIE III : GESTION DU RISQUE QUALITÉ (ICH Q9)
PARTIE III : GESTION DU RISQUE QUALITÉ (ICH Q9)
ICH Q8 Développement pharmaceutique. ISO/IEC Guide 73:2002 – Gestion du Guidelines for Failure Modes and Effects Analysis (FMEA) for Medical Devices ...
 Ladoption pour lICH ligne directrice: Q3A(R2): Présence d
Ladoption pour lICH ligne directrice: Q3A(R2): Présence d
5 juin 2015 also available in English under the following Title: Guidance Document: International ... Human Use (ICH) Impurities in New Drug Substances; ICH ...
 LES ICH ET LA RÉGLEMENTATION PHARMACEUTIQUE LA
LES ICH ET LA RÉGLEMENTATION PHARMACEUTIQUE LA
13 mai 2017 L'application des guidelines ICH pour toutes les évaluations techniques. ... la SFSTP (Société Française des Sciences et des Techniques ...
 Implémentation de la guideline ICH Q3D au sein dun site de
Implémentation de la guideline ICH Q3D au sein dun site de
10 janv. 2019 The documents may come from teaching and research institutions in France or abroad or from public or private research centers. L'archive ...
 ICH Topic Q 6 B Specifications: Test Procedures and Acceptance
ICH Topic Q 6 B Specifications: Test Procedures and Acceptance
TEST PROCEDURES AND ACCEPTANCE CRITERIA FOR. BIOTECHNOLOGICAL/BIOLOGICAL PRODUCTS. ICH Harmonised Tripartite Guideline. Table of Contents. Page.
 GUIDE RELATIF A LA BIOEQUIVALENCE DES MEDICAMENTS A
GUIDE RELATIF A LA BIOEQUIVALENCE DES MEDICAMENTS A
12 janv. 2018 - Les guidelines CPMP : 'Guideline On The Investigation Of Bioequivalence'. - Les guidelines ICH M4 intitulées 'Organisation Of The Common ...
 ICH Topic Q 1 A (R2) Stability Testing of new Drug Substances and
ICH Topic Q 1 A (R2) Stability Testing of new Drug Substances and
The texts on test procedures etc. have been brought in line with the Q6A guideline. Relevant cross-references to other ICH guidelines have been introduced. •
 Guide bonnes pratiques de fabrication
Guide bonnes pratiques de fabrication
6 mai 2019 ... Guidelines for Failure Modes and Effects Analysis (FMEA) for Medical ... ICH Q9. Les outils de gestion du risque de la qualité tels que ceux ...
 BPF PARTIE III : SYSTEME QUALITE PHARMACEUTIQUE (ICH Q10)
BPF PARTIE III : SYSTEME QUALITE PHARMACEUTIQUE (ICH Q10)
Ce document établit une nouvelle ligne directrice tripartite ICH qui décrit un modèle de système de management de la qualité efficace pour l'industrie
 DICH Q8 à Q10: la maîtrise des changements dans un système de
DICH Q8 à Q10: la maîtrise des changements dans un système de
19 jan. 2015 recherche français ou étrangers des laboratoires ... Les GMP Guidelines
 addenda intégré de le6(r1) de lich : ligne directrice pour de bonnes
addenda intégré de le6(r1) de lich : ligne directrice pour de bonnes
Ces lignes directrices devraient être lues en parallèle avec d'autres directives de l'ICH concernant la réalisation d'essais cliniques [par exemple E2A (
 LES ICH ET LA RÉGLEMENTATION PHARMACEUTIQUE LA
LES ICH ET LA RÉGLEMENTATION PHARMACEUTIQUE LA
13 mai 2017 L'application des guidelines ICH pour toutes les évaluations techniques. ... la SFSTP (Société Française des Sciences et des Techniques ...
 ICH Topic Q 1 A (R2) Stability Testing of new Drug Substances and
ICH Topic Q 1 A (R2) Stability Testing of new Drug Substances and
The texts on test procedures etc. have been brought in line with the Q6A guideline. Relevant cross-references to other ICH guidelines have been introduced. •
 PARTIE III : GESTION DU RISQUE QUALITÉ (ICH Q9)
PARTIE III : GESTION DU RISQUE QUALITÉ (ICH Q9)
Guidelines for Failure Modes and Effects Analysis (FMEA) for Medical Devices 2003 Dyadem. Press
 ICH Topic Q 6 B Specifications: Test Procedures and Acceptance
ICH Topic Q 6 B Specifications: Test Procedures and Acceptance
SPECIFICATIONS: TEST PROCEDURES AND ACCEPTANCE CRITERIA FOR. BIOTECHNOLOGICAL/BIOLOGICAL PRODUCTS. ICH Harmonised Tripartite Guideline. Table of Contents.
 Q3C (R8) Step 5 - impurities: guideline for residual solvents
Q3C (R8) Step 5 - impurities: guideline for residual solvents
20 mai 2021 ICH Guideline Residual Solvents. Pharmeuropa. 1997;Suppl 9:57. 2. Tyl RW France KA
 Ladoption pour lICH ligne directrice: Q3A(R2): Présence d
Ladoption pour lICH ligne directrice: Q3A(R2): Présence d
5 jui. 2015 Requirements for the Registration of Pharmaceuticals for. Human Use (l'ICH): Présence d'impuretés dans les nouvelles.
 La réglementation pharmaceutique et les dossiers dautorisation de
La réglementation pharmaceutique et les dossiers dautorisation de
14 mar. 2018 recherche français ou étrangers des laboratoires ... parties ainsi que les références aux guidelines ICH ou ASEAN qui doivent être suivies.
 E6(R2): Addenda intégré de bonnes pratiques cliniques - ICH GCP
E6(R2): Addenda intégré de bonnes pratiques cliniques - ICH GCP
En adoptant cette ligne directrice de l’ICH Santé Canada fait siens les principes et les pratiques qui y sont énoncés Ce document doit être lu en parallèle avec la lettre d’accompagnement et les sections pertinentes des autres lignes directrices applicables à Santé Canada
 PARTIE III : GESTION DU RISQUE QUALITÉ (ICH Q9) - AFMPS
PARTIE III : GESTION DU RISQUE QUALITÉ (ICH Q9) - AFMPS
Il sert de base ou de document ressource indépendamment des autres documents qualité ICH tout en les étayant et complète les pratiques exigences normes et lignes directrices qualité en vigueur dans l’industrie pharmaceutique et dans le domaine réglementaire
 BPF PARTIE III : SYSTEME QUALITE PHARMACEUTIQUE (ICH Q10) - AFMPS
BPF PARTIE III : SYSTEME QUALITE PHARMACEUTIQUE (ICH Q10) - AFMPS
de mettre en œuvre l’ICH Q10 avec succès et de manière efficace Ces facilitateurs favoriseront la réalisation des objectifs décrits en section 1 5 en apportant les moyens nécessaires aux décisions basées sur les risques et les sciences et qui concernent la qualité des produits
 Q12 Annexes - ICH
Q12 Annexes - ICH
ICH HARMONISED GUIDELINE TECHNICAL AND REGULATORY CONSIDERATIONS FOR PHARMACEUTICAL PRODUCT LIFECYCLE MANAGEMENT Q12 Annexes Final version Adopted on 20 November 2019 This document has been developed by the appropriate ICH Expert Working Group and has been subject to consultation by the regulatory parties in accordance with the ICH Process
 IMPURITIES GUIDELINE FOR RESIDUAL S Q3C(R8) - ICH
IMPURITIES GUIDELINE FOR RESIDUAL S Q3C(R8) - ICH
ICH HARMONISED GUIDELINE IMPURITIES: GUIDELINE FORRESIDUAL SOLVENTS Q3C(R8) Current Step 4 version dated 22 April 2021 This Guideline has been developed by the appropriate ICH Expert Working Group and has been subject to consultation by the regulatory parties in accordance with the ICH Process
 E6: Les bonnes pratiques cliniques: Directives consolidées
E6: Les bonnes pratiques cliniques: Directives consolidées
Ligne directrice de l’ICH1 E6: Les bonnes pratiques cliniques: directives consolidées ERRATUM en Anglais et Français Les versions finales anglaise et française de la ligne directrice de l’ ICH adopté par Santé Canada: Les bonnes pratiques cliniques ont été revisées dûs à des corrections éditoriales post-étape 4 par le comité
 Q12 - ICH
Q12 - ICH
The concepts outlined in prior ICH Quality Guidelines (ICH Q8 Q9 Q10 and Q11) provide opportunities for science and risk-based approaches for drug development and risk-based regulatory decisions These guidelines are valuable in the assessment of Chemistry Manufacturing and Controls (CMC) changes across the product lifecycle
 Q8(R2) - ICH
Q8(R2) - ICH
ICH HARMONISED TRIPARTITE GUIDELINE PHARMACEUTICAL DEVELOPMENT Q8(R2) Current Step 4version dated August 2009 This Guideline has been developed by the appropriate ICH Expert Working Group and has been subject to consultation by the regulatory parties in accordance with the ICH Process
 Q1A(R2) - ICH
Q1A(R2) - ICH
This Guideline has been developed by the appropriate ICH Expert Working Group and has been subject to consultation by the regulatory parties in accordance with the ICH Process At Step 4 of the Process the final draft is recommended for adoption to the regulatory bodies of the European Union Japan and USA Q1A(R2) Document History
 Q3D(R1) - ICH
Q3D(R1) - ICH
ICH HARMONISED GUIDELINE GUIDELINE FOR ELEMENTAL IMPURITIES Q3D(R1) Finalversion Adopted on 22 March 2019 This Guideline has been developed by the appropriate ICH Expert Working Group and has been subject to consultation by the regulatory parties in accordance with the ICH Process
 ICH guideline Q2(R2) on validation of analytical procedures
ICH guideline Q2(R2) on validation of analytical procedures
ICH Q2(R2) Guideline 1 1 1 INTRODUCTION 2 This guideline presents a discussion of elements for consideration during the validation of 3 analytical procedures included as part of registration applications submitted within the ICH 4 member regulatory authorities Q2(R2) provides guidance and recommendations on how to 5
 ICH guideline Q9 (R1) on quality risk management
ICH guideline Q9 (R1) on quality risk management
At Step 2 of the ICH Process a consensus draft text or guideline agreed by the appropriate ICH Expert Working Group is transmitted by the ICH Assembly to the regulatory authorities of the ICH regions for internal and external consultation according to national or regional procedures
 Searches related to guidelines ich en français filetype:pdf
Searches related to guidelines ich en français filetype:pdf
Past regular attendance in ICH meetings Past appointment of experts in WGs Application of ICH Guidelines Have implemented at least the following ICH Guidelines (“Tier 1”): Q1: Stability Testing Guidelines Q7: Good Manufacturing Practice Guide for Active Pharmaceutical Ingredients E6: Good Clinical Practice Guideline