|
Chlorure dhydrogène (ou acide chlorhydrique) et solutions aqueuses
Le chlorure d'hydrogène en solution aqueuse (ou solution aqueuse d'acide chlor hydrique) est utilisé principalement dans les opérations de nettoyage et |
|
Chlorure dhydrogène (ou acide chlorhydrique) et solutions - INRS
Chlorure d'hydrogène (ou acide chlorhydrique) et solutions aqueuses Fiche toxicologique synthétique n° 13 - Edition Février 2019 Pour plus d'information se |
|
Fiche de données de sécurité Chlorure d´hydrogène 30 - PanGas
28 avr 2020 · chlorure d'hydrogene Mention d'Avertissement: Danger Déclaration(s) de risque : H280: Contient un gaz sous pression; peut exploser sous |
|
Chlorure dhydrogène et solutions aqueuses - Aix - Marseille
Préparation des chlorures et sels métalliques divers PROPRIÉTÉS PHYSIQUES [1 à 6] Le chlorure d'hydrogène est un gaz suffocant, à saveur acide, facilement |
|
CHIMIE Premier problème : Le chlorure dhydrogène
Premier problème : Le chlorure d'hydrogène Tous les gaz sont considérés comme parfaits, on donne R = 8,314 J K mol –1 On note p° la pression standard ( |
|
Chap3 Réaction entre le fer et lacide chlorhydrique
Les ions hydrogène et chlorure sont présents dans une solution d'acide chlorhydrique Le fer réagit avec l'acide chlorhydrique, avec formation de dihydrogène |
Chlorure dhydrogène (ou acide chlorhydrique) et solutions
Le chlorure d’hydrogène anhydre est un gaz incolore, d'odeur âcre et irritante, facilement liquéfiable (sous pres sion atmosphérique, il se liquéfie entre - 94 et - 85 °C) Il est très soluble dans l'eau : pour 100 g d'eau, 82,3 g de chlorure d'hydrogène à 0 °C, 67,3 g HCl à 30 °C ou 56,1 g HCl à 60 °C
Fiche de données de sécurité Chlorure d´hydrogène 3
Nom commercial: Chlorure d'hydrogène 2 8; Chlorure d'hydrogène 3 0; Chlorure d'hydrogène 4 5; Chlorure d'hydrogène 5 0; Chlorure d'hydrogène 5 5 Désignation chim ique Formule chimique Concentration N° CAS N° d’enregistreme nt REACH facteurs M: Notes chlorure d'hydrogene HCl 100 7647-01-0 01-2119484862-27 - #
Chlorure dhydrogène (ou acide chlorhydrique) et solutions
Le chlorure d’hydrogène, ou ses solutions aqueuses, sont corrosifs ou irritants selon la concentration ; ils induisent des effets locaux sur la peau, les yeux et le tractus gastro -intestinal, après exposition directe à une dose suffisam ment élevée
Les acides et les bases Corrigés des exercices
Le chlorure d'hydrogène est un composé moléculaire (il possède une liaison covalente) C'est un gaz dans les conditions normales de température et de pression 2 Ecrivez l'équation de la réaction qui accompagne la mise en solution du chlorure d'hydrogène dans l'eau Réponse : HCl + H 2O H 3O + + Cl– 3
Tests didentification de Collège quelques ions
Solution de chlorure d'hydrogène + (acide chloridrique) (H + Cl ) Solution d’hydroxyde de sodium (soude) (Na+ + HO ) Nitrate d’argent ( + ) I Test d'identification des ions chlorure 1 Expérience : On verse quelques gouttes de nitrate d’argent de formule chimique ( + ) dans des tubes à essai Contenant chlorure de sodium (Na+ + Cl ): 2
I) ACTION DE L’ACIDE CHLORHYDRIQUE SUR LES METAUX
C’est la solution de chlorure d’aluminium e) Conclusion : Le réagit avec la solution d’acide chlorhydrique Au cour de cette réaction les réactifs sont l’aluminium Al et les ions d’hydrogène H+, et les produits sont le gaz dihydrogène H2 et la solution de chlorure d’aluminium (Al3+ + 3Cl-) dont : Le bilan littéral est :
SÉRIE C3 ALCENES ET ALCYNES
2 L’addition de chlorure d’hydrogène sur A conduit de façon prépondérante au 2-chloro-2,3-diméthylbutane mais pas exclusivement Montrer que cela permet de déterminer la formule semi-développée de A 3 A présente-t-il l’isomérie Z, E ? 4 Donner les produits majoritaires et minoritaires lors de l’addition d’eau sur A
France - Brenntag
Chlorure d’aluminium (NF EN 881) Aluminate de sodium (NF EN 882) Polymères anioniques et cationiques en poudre (NF EN 1407) DIVERS Produits de nettoyage et désinfection des membranes d’osmose et d’ultra-filtration Antitartres
|
REACTION TOTALE ET EQUILIBRE CHIMIQUE (CORRECTION
[PDF] REACTION TOTALE ET EQUILIBRE CHIMIQUE (CORRECTION lerepairedessciences S TPa equilibre correction pdf |
|
Les acides et bases en solution aqueuse - Groupe Transition
[PDF] Les acides et bases en solution aqueuse Groupe Transition grptrans ulg ac be modules ac bas i pdf |
|
pH et équilibres acido-basiques en solution - Groupe Transition
[PDF] pH et équilibres acido basiques en solution Groupe Transition grptrans ulg ac be modules ph equab pdf |
|
Note relative au peroxyde d hydrogène en solution aqueuse - Ineris
[PDF] Note relative au peroxyde d 'hydrogène en solution aqueuse Ineris ineris dra peroxyde hydrogene repro pdf |
|
Acides et Bases en solution aqueuse Acides Exercice 1 - Eduscol
[PDF] Acides et Bases en solution aqueuse Acides Exercice Eduscoleduscol education rnchimie chi gen dossiers acides bases pdf |
|
chap 1 : définition et mesure du pH I Solutions d acide
[PDF] chap définition et mesure du pH I Solutions d 'acide dfglfa dfg info lib exe fetch php?media ph |
|
pH d une solution aqueuse
[PDF] pH d 'une solution aqueuseww ac poitiers math sp IMG pdf PH pdf |
|
Chapitre 4: Ions et pH
[PDF] Chapitre Ions et pHetab ac poitiers coll sauze vaussais Chap Ions et pH pdf |
|
Réactions de neutralisation
[PDF] Réactions de neutralisation meine mathe de Chimie eModules b bc acidebaseph pdf |
|
LA LIAISON CHIMIQUE
plus ou moins importante d 'ion hydrogène (H+) en solution Les indicateurs colorés sont des substances dont la teinte dépend du pH de la solution dans Exemple acide chlorhydrique +ammoniaque chlorure d 'ammonium + eau |
- tp chimie ph et equilibre chimique
- exercices corrigés ph des solutions aqueuses
- acides et bases en solution aqueuse exercices corrigés
- chimie des solutions aqueuses pdf
- chimie des solutions aqueuses exercices corrigés pdf
- tp chimie equilibre chimique
- solution aqueuse exercices corrigés pdf
- solution aqueuse cours
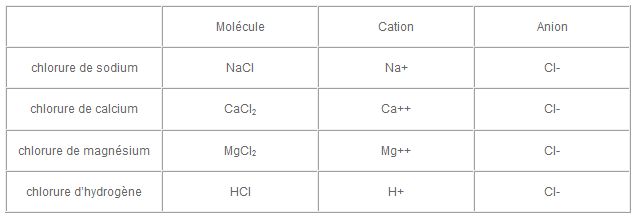
Chlorure d'hydrogène — Wikipédia
Source:http://doc.lerm.fr/wp-content/gallery/lerm-infos-23/tableau-chlorures.jpg

Présentation du chlore aux chlorures
Source:https://docplayer.fr/docs-images/43/7123413/images/page_14.jpg

Chapitre 7 : Acides bases et sels - PDF Téléchargement Gratuit
Source:https://www.fichier-pdf.fr/2016/11/09/tputilisation-des-modeles-moleculaires/preview-tputilisation-des-modeles-moleculaires-1.jpg

TPUtilisation des modéles moléculaires par nafti - Fichier PDF
Source:http://sciencesphysiques.e-monsite.com/medias/images/test-identification-ions.png?fx\u003dr_800_315

Test des ions
Source:https://upload.wikimedia.org/wikipedia/commons/4/4b/Cobalt%28II%29_chloride.jpg

Chlorure — Wikipédia
Source:https://kronos-images.schoolmouv.fr/2-fnx-spc-c06-img01.png
hcl hopital
Etablissement public d 'excellence, les Hospices Civils de Lyon sont
- parking gratuit croix rousse
- hopital lyon sud
- tarif parking hopital croix rousse
- centre anti douleur lyon croix rousse
- hôpital de la croix rousse hcl lyon
- tcl itinéraire
- hopital de la croix rousse
composé ionique dans l'eau
L 'eau solvant I La molécule d 'eau - Rappels
ph de début de précipitation
CHIM105B #8211 DS2 - Corrigé
- produit de solubilité du chlorure de plomb
- relation entre s et ks
- nitrate de plomb + chlorure de potassium
- exercice solubilité et précipitation
- équation de dissolution du chlorure de plomb dans l'eau
- exercices corrigés de solubilité pdf
- chlorure de plomb 2
- hydroxyde de plomb
hydroxyde de plomb
CHIM105B #8211 DS2 - Corrigé
- produit de solubilité du chlorure de plomb
- relation entre s et ks
- nitrate de plomb + chlorure de potassium
- ph de début de précipitation
- équation de dissolution du chlorure de plomb dans l'eau
- pb(oh)2
- chlorure de plomb 2
- exercice solubilité et précipitation