 La chimie
La chimie
• chaque colonne (groupe) du tableau périodique moderne partage la même • le rayon ionique est le rayon d'un cation ou d'un anion. • lorsqu'un atome ...
 Untitled
Untitled
tableau périodique. 4. Energie de la première ionisation. * L'énergie de lère ionisation diminue lorsque le rayon atomique augmente: plus l'électron de.
 Architecture de la matière
Architecture de la matière
Figure 2 : évolution du rayon atomique pour les 3 premières périodes. Figure 3 : évolution du rayon atomique dans la classification. Source : CHIMIE 3ème
 Chapitre III LES CRISTAUX IONIQUES
Chapitre III LES CRISTAUX IONIQUES
Les rayons ioniques de tous les éléments du tableau périodique déterminés rayons cristallins (meilleure approche que le rayon ionique). Coordinence. 4. 6. 8.
 Le tableau périodique
Le tableau périodique
• Le rayon atomique. • Le rayon ionique. • L'énergie d'ionisation. • L'électronégativité. • Le point de fusion. Page 15. 15. Le rayon atomique. • En théorie le
 LES ELEMENTS DU GROUPE 2 - LES METAUX ALCALINO
LES ELEMENTS DU GROUPE 2 - LES METAUX ALCALINO
Rayon atomique et rayon ionique / C. Densité point de fusion et point d Les métaux alcalino-terreux sont les éléments du 2e groupe du tableau périodique.
 CRISTALLOGRAPHIE
CRISTALLOGRAPHIE
6). À partir du rayon atomique (Ti) du titane dans le tableau de données ci-dessous déterminer quel serait le paramètre de maille ′ si l'empilement du
 Tableau périodique et périodicité
Tableau périodique et périodicité
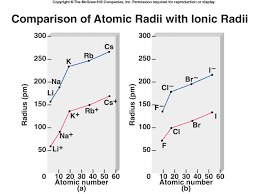
Rayon ionique: Rayons des ions (en Armstroeng) en fonction du numéro atomique. Rayon atomique: Rayons des atomes isolés (en.
 Cours 3. Classification géochimique des éléments
Cours 3. Classification géochimique des éléments
Classification des éléments en traces selon leur position dans le tableau périodique Les éléments à fort rayon ionique et à faible charge sont appelés : LILE ...
 REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET POPULAIRE
REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET POPULAIRE
%20%20V%20.pdf
 Architecture de la matière
Architecture de la matière
A – DEFINITION DU RAYON IONIQUE le tableau périodique est la meilleure des ... éléments chimiques tous regroupés dans un tableau périodique ...
 I. Propriétés des éléments dans un groupe et dans une période
I. Propriétés des éléments dans un groupe et dans une période
I. Tableau périodique des éléments Cette propriété périodique est directement reliée à ... Chez les ions positifs le rayon ionique est plus petit.
 La chimie
La chimie
chaque colonne (groupe) du tableau périodique moderne partage la même le rayon ionique est le rayon d'un cation ou d'un anion.
 Le tableau périodique
Le tableau périodique
Périodicité des propriétés physiques. • Le rayon atomique. • Le rayon ionique. • L'énergie d'ionisation. • L'électronégativité. • Le point de fusion
 Présentation PowerPoint
Présentation PowerPoint
V : Propriétés physiques et chimiques et tableau périodique. V.1. Propriétés physiques. V.1.b. Le rayon ionique. Ion : atome ou groupe d'atome dont la
 Untitled
Untitled
Le tableau périodique reste le moyen le plus important de comparaison Le rayon atomique diminue en traversant une période de gauche à.
 Architecture de la matière
Architecture de la matière
A – DEFINITION DU RAYON IONIQUE éléments chimiques tous regroupés dans un tableau périodique parfaitement ordonné. Le Plan du cours ...
 Chapitre 3: Classification périodique des éléments
Chapitre 3: Classification périodique des éléments
ces ions sont appelés rayons ioniques. Pour des ions ayant la même charge le rayon ionique ri varie dans le tableau périodique comme le rayon atomique.
 Après latome dhydrogène Les atomes polyélectronique
Après latome dhydrogène Les atomes polyélectronique
Le tableau périodique Le rayon covalent (1/2 de la distance entre 2 atomes dans une molécule ou dans une solide) ... Rayon atomique versus rayon ionique.
 CRISTALLOGRAPHIE
CRISTALLOGRAPHIE
Relier le rayon métallique covalent
 Tendances du rayon ionique dans le tableau périodique
Tendances du rayon ionique dans le tableau périodique
Le rayon atomique • en allant de gauche à droite les rayons atomiques des éléments tendent à devenir plus petits • le plus petit rayon atomique est dû à l’augmentation de la charge nucléaire effective en allant de gauche à droite • les électrons de valence sont retenus plus près du noyau par sa plus grande
 Chapitre 3: Classification périodique des éléments
Chapitre 3: Classification périodique des éléments
L a première classification périodique a été établie bien avant que la structure électronique des éléments ne soit connue Mendeleïev a disposé (1869) dans un tableau les 68 éléments connus à l’époque en se basant sur la relation entre le poids atomique et les propriétés chimiques
 Chap V : Propriétés physiques et chimiques et tableau périodique
Chap V : Propriétés physiques et chimiques et tableau périodique
Chap V : Propriétés physiques et chimiques et tableau périodique V 1 Propriétés physiques V 1 b Le rayon ionique Ion : atome ou groupe d’atome dont la charge est devenue positive (ou négative) à la suite de la perte (ou de la capture) d’un ou de plusieurs électrons
 Searches related to rayon ionique tableau périodique PDF
Searches related to rayon ionique tableau périodique PDF
Le rayon ionique augmente le long d'une colonne du tableau périodique Pour des ions isoélectroniques c'est-à-dire qui possèdent la même con guration électronique il diminue de gauche à droite du tableau comme le rayon atomique En n pour un même élément le rayon ionique d'un anion est généralement plus grand que le rayon atomique
Qu'est-ce que le rayon ionique dans le tableau périodique ?
Le rayon ionique des éléments présente des tendances dans le tableau périodique. En général: Le rayon ionique augmente à mesure que vous vous déplacez de haut en bas sur le tableau périodique. Le rayon ionique diminue à mesure que vous vous déplacez dans le tableau périodique, de gauche à droite.
Comment calculer le rayon ionique ?
Mesuré à partir de la distance entres cations et anions d'un cristal ionique. Le rayon est exprimé en pm (pico mètre = 10 -12 m). Le rayon ionique caractérise, comme tout rayon, le volume occupé par les électrons du nuage électronique, sauf que pour les ions, le nombre d'électron diffère de la forme neutre, ce qui explique deux phénomènes inverses:
Quelle est la différence entre rayon ionique et rayon atomique ?
Bien que rayon ionique et rayon atomique ne signifient pas exactement la même chose, la tendance s'applique au rayon atomique ainsi qu'au rayon ionique. Le rayon ionique est la moitié de la distance entre les ions atomiques dans un réseau cristallin. Pour trouver la valeur, les ions sont traités comme s'ils étaient des sphères dures.
Comment les rayons atomiques varient-ils ?
Les rayons atomiques varient de manière prévisible lorsqu'on se déplace dans le tableau périodique. Par exemple, les rayons diminuent en général le long d'une période (rangée) de la table depuis les alcalins jusqu'aux gaz nobles; et augmentent lorsqu'on descend une colonne.
I. Tableau périodique des éléments
7 I. Propriétés des éléments dans un groupe et dans une période1.1. Rayon atomique
et la frontière du - Dans une même période, le rayon atomique diminue de gauche à droite. Cette propriété périodique est directement reliée àCette croissance traduit une augmenta
noyau et les électrons de valence et donc à une diminution du rayon atomique. Exemple : le rayon atomique des éléments de la deuxième période diminue de gauche à droite.Li Be B C N
pm (picomètre) 152 pm 118 pm 80 pm 77 pm 75 pm - Dans un même groupe, le rayon atomique augmente de haut en électrons périphériques sont moins fortement liés au noyau dans le bas du tableau. Exemple : le rayon atomique des éléments du groupe IA augmente de haut en bas.Li 152 pm
Na 186 pm
K 227 pm
Rb 248 pm
1.2. Rayon ionique
(ion négatif). a) Ions positifs électrons. Chez les ions positifs, le rayon ionique est plus petit que le rayon atomique, par exemple :I. Tableau périodique des éléments
8Na 186 pm Na+ 99 pm
Mg 160 pm Mg2+ 65 pm
b) Ions négatifs électrons. Chez les ions négatifs, le rayon ionique est plus grand que le rayon atomique, par exemple :N 75 pm N3 171 pm
O 73 pm O2 140 pm
F 71 pm F 133 pm
1.3. Rayon ionique dans un même groupe
Dans un groupe, le rayon ionique augmente de haut en bas, par exemple :Groupe IA Groupe VIIA
Li+ 59 pm F 133 pm
K+ 138 pm Br 196 pm
Rb+ 148 pm I 220 pm
1.4. Rayon ionique dans une même période
Dans une période, le rayon ionique des ions positifs diminue de gauche à droite augmente brusquement et ré-diminue de gauche à droite. Exemple : Rayon ionique des éléments de la troisième période99 pm 65 pm 50 pm 212 pm 184 pm 181 pm
À titre de comparaison des éléments qui ne sont pas dans les mêmes groupes et périodes, par exemple : p = 18 p = 17 p = 21 p = 19 p = 38 e = 18 e = 18 e = 18 e = 18 e = 36I. Tableau périodique des éléments
9 éléments ayant le moins de protons aura la plus grande taille, ainsi on peut classer ces éléments par ordre décroissant de la taille :1.5. Tendance
sont généralement plus élevées chez les métaux que chez les non- métaux.Dans une période
augmentent du groupe IA à IVA, tandis que les éléments du groupeChez les métaux
fu à diminuer du haut en bas leChez les non-métaux
tendance à augmenter en allant du haut en basII. Place d dans le tableau périodique
élément dans la classification périodique se détermine à partir de la configuration électronique.électrons
sur leur couche externe. Le numéro des groupes principaux (IA àVIIIA) indique , par exemple,
les éléments des groupes IA et IIA ont respectivement 1 et 2 électrons sur leur couche externe. pas aussi évidente que celle des éléments des groupes A. Connaissant ne suffit pas du tableau périodique car la plupart des métaux de transition ont 1 ou 2 électrons périphériques comme les éléments des groupes IA et IIA. Il faut donc encore -dernière, par exemple : - si la couche externe possède 1 électron et -dernière 8I. Tableau périodique des éléments
10 - si -dernière 8 - mais si -dernière e transition. électroniques. Les chiffres placés devant les sous-couches dans la configuration électronique indiquent le numéro de la période. Tableau 2.1 Position des éléments dans le tableau périodique sachant leur distribution des électrons. Élément Distribution des électrons Numéro du périodeNuméro du groupe
37 Rb 2 8 18 8 1 5 1
38Sr 2 8 18 8 2 5 2
21Sc 2 8 9 2 4 Métal de transition
26Fe 2 8 14 2 4 Métal de transition
47Ag 2 8 18 18 1 5 Métal de transition
29Cu 2 8 18 1 4 Métal de transition
34Se 2 8 18 6 4 6
53I 2 8 18 18 7 5 7
83Bi 2 8 18 32 18 5 6 5
I. Tableau périodique des éléments
111. Indiquer les numéros du période, du groupe ou du métal de transition des
éléments dans le tableau ci-dessous :
Élément Distribution des électrons Numéro du périodeNuméro du
groupeA 2 8 18 7
B 2 8 8 1
C 2 8 8 2
D 2 8 18 2
E 2 8 18 32 17 1
F 2 8 18 32 18 8 1
G 2 8 3
H 2 8 18 32 18 4
I 2 8 18 32 12 2
J 2 8 18 18 9 2
K 2 8 7
2. Dans chacun des groupes suivants, placer les éléments par ordre
décroissant de rayon atomique et justifier. a) 12A ; 17B ; 16C ; 14D b) 30Zn ; 26Fe ; 19K ; 23V ; 21Sc ; 28Ni ; 33AS c) 20Ca ; 4Be ; 56Ba ; 12Mg ; 88Ra3. Dans chacun des groupes suivants, placer les atomes ou ions par ordre
décroissant de la taille et justifier. a) 16S2 ; 16S ; 16S ; 16S3 b) 8O2 ; 11Na+ ; 10Ne ; 12Mg2+4. Laquelle est correcte pour le classement par ordre décroissant de la taille
des particules suivantes ?quotesdbs_dbs35.pdfusesText_40[PDF] énergie de première ionisation calcul
[PDF] l'ancien régime et la révolution résumé
[PDF] la morphologie en linguistique
[PDF] énergie d'ionisation calcul
[PDF] morphologie flexionnelle et dérivationnelle
[PDF] morphologie des mots exercices
[PDF] cours de morphologie linguistique pdf
[PDF] analyse morphologique des mots exercices
[PDF] fin de l'ancien régime
[PDF] morphologie flexionnelle et dérivationnelle pdf
[PDF] la morphologie lexicale
[PDF] morphologie des insectes pdf
[PDF] classification des insectes pdf
[PDF] biologie des insectes pdf
