 I. SITUATION DAPPRENTISSAGE II. CONTENU DE LA LEÇON
I. SITUATION DAPPRENTISSAGE II. CONTENU DE LA LEÇON
Au cours des réactions chimiques les atomes réagissent pour obtenir une structure électronique plus Cite les ions polyatomiques parmi les ions suivants : SO4.
 Spectrométrie démission dions secondaires. Secondary Ions Mass
Spectrométrie démission dions secondaires. Secondary Ions Mass
.ions polyatomiques hétéronucléaires (composés): (AmBn). +. . (AmBn). -. (< 1 .Canons à ions (émission thermo-ionique) - Ions de gaz rares. Ar. +.
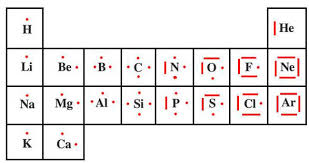 Fiche 2: Représentation de Lewis des espèces chimiques
Fiche 2: Représentation de Lewis des espèces chimiques
Représentation de Lewis des ions. • Un atome faisant partie d'un ion polyatomique va porter une charge formelle s'il n'est pas entouré du même nombre d
 Atome molécule et ion - Guillotine et tsunami
Atome molécule et ion - Guillotine et tsunami
Il existe aussi des ions polyatomiques : c'est une molécule qui a gagné ou perdu un ou plusieurs électrons. Voici quelques exemples : Nom ion nitrate ion
 Les matériaux et lélectricité
Les matériaux et lélectricité
Un ion monoatomique est constitué d'un seul atome. ○ Un ion polyatomique est constitué par un ensemble d'atomes. * Exemples : Les cations.
 Untitled
Untitled
- un ion polyatomique est un groupe d'atome ayant perdu ou capturé un ou plusieurs électrons. - Les ions monoatomiques. - Les cations. Un cation est un ion
 cours : Atomes et molécules
cours : Atomes et molécules
On ne regarde que la géométrie de l'atome considéré avec ses liaisons. Une double liaison compte comme une simple liaison. V- ions poly-atomiques. Pour
 Grandeurs physiques pour caractériser un système initial
Grandeurs physiques pour caractériser un système initial
Pour un ion polyatomique la masse molaire est égale à la somme des masses molaires des atomes qui composent l'ion. Exemple : M(H+) = 1 g.mol-1 ; M(S2-) 32
 Chapitre 4 : Structure et polarité des espèces chimiques
Chapitre 4 : Structure et polarité des espèces chimiques
ion polyatomique . . . . . . . . . . . 33. 4.2 Géométrie des molécules et ions polyatomiques . . . . . . . . . . . . . . . 33. 4.3 Polarité d'une molécule ...
 Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques. Formules. Constantes et conversions. Solubilité des composés ioniques dans l'eau à 25 °C. Ions -. 1. Ions -. 2. Ions
 Chapitre 4 : Structure et polarité des espèces chimiques
Chapitre 4 : Structure et polarité des espèces chimiques
4.1.3 Schéma de Lewis d'une molécule ou d'un ion polyatomique . . . . . . . . . . . 33. 4.2 Géométrie des molécules et ions polyatomiques .
 Fiche de synthèse n°3.a Nombres doxydation
Fiche de synthèse n°3.a Nombres doxydation
Page 2. ? Pour les ions polyatomiques la somme des nombres d'oxydation est égale à la charge portée par cet ion. Exemple : ion hydroxyde HO-. n.o(H) = +I.
 MÉCANISME DE FORMATION DIONS POLYATOMIQUES
MÉCANISME DE FORMATION DIONS POLYATOMIQUES
01?/01?/1984 MÉCANISME DE FORMATION D'IONS POLYATOMIQUES SECONDAIRES. ... (1) On suppose qu'il existp tout au cours du phénomène un centre de nucléation ...
 CH III) Constitution de la matière : les ions
CH III) Constitution de la matière : les ions
D. GENELLE Cours Constitution de la matière Les ions Page 1/3 Un ion polyatomique est un édifice chimique électriquement chargé formé de plusieurs.
 QCM relatif au « Cours 16 Lénergie »
QCM relatif au « Cours 16 Lénergie »
QCM relatif au cours « STRUCTURE ELECTRONIQUE DES IONS » Dans un ion il existe autant de charge positive que négative : ... d - un cation polyatomique.
 Structure de Lewis II
Structure de Lewis II
tridimensionnelles des molécules ou des ions polyatomiques dont on a d'abord construit les diagrammes de Lewis. Au cours d'une séance de travail on peut.
 1ére Année de lenseignement secondaire
1ére Année de lenseignement secondaire
un cours illustré de nombreux documents (schémas
 02.schema-de-lewis.pdf
02.schema-de-lewis.pdf
Représentation de Lewis des ions. B : Mésomérie Un atome faisant partie d'un ion polyatomique va porter une charge formelle s'il n'est pas entouré.
 Chapitre 4 : le modèle de latome
Chapitre 4 : le modèle de latome
2) les ions polyatomiques Un ion monoatomique est un atome qui a perdu ou ... Au cours du XX° siècle les scientifiques ont élaboré.
Solubilité des composés ioniques
dans l'eau à 25 °C Ions 1 Ions 2 Ions 3 Formule Nom Formule Nom Formule Nom H 2 PO 4- H 2 PO 3- HCO 3- HSO 4- HSO 3- BrO 3- CH 3 COO C 6 H 5 COO ClO ClO 2- ClO 3- ClO 4- CN IO 3- OH NO 3- NO 2- MnO 4- SCN dihydrogénophosphate dihydrogénophosphite hydrogénocarbonate hydrogénosulfate hydrogénosulfite bromate acétate benzoate hypochlorite chlorite chlorate perchlorate cyanure iodate hydroxyde nitrate nitrite permanganate thiocyanate HPO 42-HPO 32-
CO 32-
SO 42-
SO 32-
C 2 O 42-
CrO 42-
Cr 2 O 72-
S 2 O 32-
SiO 32-
hydrogénophosphate hydrogénophosphite carbonate sulfate sulfite oxalate chromate dichromate thiosulfate silicate PO 43-
PO 33-
BO 33-
phosphate phosphite borate Ions 1
Formule Nom
NH 4+ H 3 O ammonium hydronium qmcT qCT r qnH 3 pH log H O pOH log OH QIt e QnF produitsréactifsrffHnH nH
produitsréactifs EL EL r H 2 42bb acxa
Quantité Symbole Valeur
nombre d'Avogadro N A 23602 10
température et pression normales TPN 0,00 ºC et 100 kPa volume molaire d'un gaz à TPN TPN V22,7 L/mol
constante d'auto-ionisation de l'eau à 25 CK e 14
100 10
enthalpie de fusion de l'eau à 0 C fus H6,02 kJ/mol
enthalpie de vaporisation de l'eau à100,0 C
vap H40,7 kJ/mol
chaleur massique de l'eau à25,0 C
C eau 4 184 chaleur massique de la glace C glace 203chaleur massique de la vapeur C vapeur 201
constante de Faraday F 96 500 C/mol
Ions Group IA,
NH 4+ H (H 3 O ) ClO 3- NO 3- ClO4- Cl Br I CH 3 COO SO 42 -S 2 - OH PO 43 -
SO 32 -
CO 32 -
(aq) solubilité élevée (> 0,1 mol/L) tous tous la plupart la plupart la plupart
Group IA,
Group IIA,
NH 4+Group IA ,
NH 4+ , Sr 2+ Ba 2+ , TlGroup IA,
NH 4+ (s) solubilité faible (< 0,1 mol/L) aucun aucun A g , Tl Hg 22+, Hg Cu , Pb 2+ Ag , Hg Ca 2+ , Sr 2+ Ba 2+ , Ra 2+ Pb 2+ , Ag la plupart la plupart la plupartquotesdbs_dbs12.pdfusesText_18
[PDF] Les ions probleme 3eme
[PDF] Les ions, pour les pro
[PDF] les ions-interactions fondamentale
[PDF] les isitopes ; element chimique
[PDF] Les isomères d'une molécules
[PDF] Les isotopes d'hydrogene
[PDF] Les isotopes de l'hydrogène
[PDF] les isotopes de l'uranium
[PDF] les isotopes de l'hydrogène exercice
[PDF] les italiens a new york
[PDF] les italiens victimes de la xenophobie caricature
[PDF] les jardins d'agadir club marmara
[PDF] les jardins d'agadir contact
[PDF] les jardins d'agadir immobilier
