 Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques. Formules. Constantes et conversions. Solubilité des composés ioniques dans l'eau à 25 °C. Ions -. 1. Ions -. 2. Ions -.
 I. SITUATION DAPPRENTISSAGE II. CONTENU DE LA LEÇON
I. SITUATION DAPPRENTISSAGE II. CONTENU DE LA LEÇON
Au cours des réactions chimiques les atomes réagissent pour obtenir une structure électronique plus Cite les ions polyatomiques parmi les ions suivants : SO4.
 Spectrométrie démission dions secondaires. Secondary Ions Mass
Spectrométrie démission dions secondaires. Secondary Ions Mass
.ions polyatomiques hétéronucléaires (composés): (AmBn). +. . (AmBn). -. (< 1 .Canons à ions (émission thermo-ionique) - Ions de gaz rares. Ar. +.
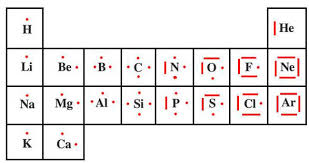 Fiche 2: Représentation de Lewis des espèces chimiques
Fiche 2: Représentation de Lewis des espèces chimiques
Représentation de Lewis des ions. • Un atome faisant partie d'un ion polyatomique va porter une charge formelle s'il n'est pas entouré du même nombre d
 Atome molécule et ion - Guillotine et tsunami
Atome molécule et ion - Guillotine et tsunami
Il existe aussi des ions polyatomiques : c'est une molécule qui a gagné ou perdu un ou plusieurs électrons. Voici quelques exemples : Nom ion nitrate ion
 Les matériaux et lélectricité
Les matériaux et lélectricité
Un ion monoatomique est constitué d'un seul atome. ○ Un ion polyatomique est constitué par un ensemble d'atomes. * Exemples : Les cations.
 Untitled
Untitled
- un ion polyatomique est un groupe d'atome ayant perdu ou capturé un ou plusieurs électrons. - Les ions monoatomiques. - Les cations. Un cation est un ion
 cours : Atomes et molécules
cours : Atomes et molécules
On ne regarde que la géométrie de l'atome considéré avec ses liaisons. Une double liaison compte comme une simple liaison. V- ions poly-atomiques. Pour
 Grandeurs physiques pour caractériser un système initial
Grandeurs physiques pour caractériser un système initial
Pour un ion polyatomique la masse molaire est égale à la somme des masses molaires des atomes qui composent l'ion. Exemple : M(H+) = 1 g.mol-1 ; M(S2-) 32
 Chapitre 4 : Structure et polarité des espèces chimiques
Chapitre 4 : Structure et polarité des espèces chimiques
ion polyatomique . . . . . . . . . . . 33. 4.2 Géométrie des molécules et ions polyatomiques . . . . . . . . . . . . . . . 33. 4.3 Polarité d'une molécule ...
 Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques. Formules. Constantes et conversions. Solubilité des composés ioniques dans l'eau à 25 °C. Ions -. 1. Ions -. 2. Ions
 Chapitre 4 : Structure et polarité des espèces chimiques
Chapitre 4 : Structure et polarité des espèces chimiques
4.1.3 Schéma de Lewis d'une molécule ou d'un ion polyatomique . . . . . . . . . . . 33. 4.2 Géométrie des molécules et ions polyatomiques .
 Fiche de synthèse n°3.a Nombres doxydation
Fiche de synthèse n°3.a Nombres doxydation
Page 2. ? Pour les ions polyatomiques la somme des nombres d'oxydation est égale à la charge portée par cet ion. Exemple : ion hydroxyde HO-. n.o(H) = +I.
 MÉCANISME DE FORMATION DIONS POLYATOMIQUES
MÉCANISME DE FORMATION DIONS POLYATOMIQUES
01?/01?/1984 MÉCANISME DE FORMATION D'IONS POLYATOMIQUES SECONDAIRES. ... (1) On suppose qu'il existp tout au cours du phénomène un centre de nucléation ...
 CH III) Constitution de la matière : les ions
CH III) Constitution de la matière : les ions
D. GENELLE Cours Constitution de la matière Les ions Page 1/3 Un ion polyatomique est un édifice chimique électriquement chargé formé de plusieurs.
 QCM relatif au « Cours 16 Lénergie »
QCM relatif au « Cours 16 Lénergie »
QCM relatif au cours « STRUCTURE ELECTRONIQUE DES IONS » Dans un ion il existe autant de charge positive que négative : ... d - un cation polyatomique.
 Structure de Lewis II
Structure de Lewis II
tridimensionnelles des molécules ou des ions polyatomiques dont on a d'abord construit les diagrammes de Lewis. Au cours d'une séance de travail on peut.
 1ére Année de lenseignement secondaire
1ére Année de lenseignement secondaire
un cours illustré de nombreux documents (schémas
 02.schema-de-lewis.pdf
02.schema-de-lewis.pdf
Représentation de Lewis des ions. B : Mésomérie Un atome faisant partie d'un ion polyatomique va porter une charge formelle s'il n'est pas entouré.
 Chapitre 4 : le modèle de latome
Chapitre 4 : le modèle de latome
2) les ions polyatomiques Un ion monoatomique est un atome qui a perdu ou ... Au cours du XX° siècle les scientifiques ont élaboré.
JOURNAL DE PHYSIQUE
Colloqu
e C2 supplémen t a u n°2 Tom e *5 févrie r 1984 pag e C2-12 9
MÉCANISM
E D EFORMATIO
N D'iON SPOLYATOMIQUE
SSECONDAIRE
SAPPLICATION
S AU X ION S Cu E T Cu P Joye sLaboratoire
dePhysique
desSolides,
Bât.
510,Université
Paris-Sud,
91405Orsay,
France
Résum
L a formatio n d'ion s secondaire s polyatoraique s es t décrit e comme due à "la capture par un ion secondaire monoatomique d'atomes émis à la suite du même impact primaire.
Abstrac
t Th e formatio n o f secondar y polyatomi c ion s i s describe d as resulting from the nucleation on a monoatomic secondary ion of atoms emitted after same primary impact.
IINTRODUCTIO
N L a productio n d'ion s moléculaire s M n o u M n lor s d u bombardemen t d'un e cibl e [M par un faisceau d'ions A+ ayant une énergie de l'ordre de 10 keV est un phénomène qui a fait l'objet ces dernières années de nombreuses études expérimentales ou théoriques /l/. Souvent les intensités I(M±) ou I(Mp) enregistrées dans le spectre de masse présentent un comportement en dent de scie extrêmement marqué avec renforcement systématique pour une parité donnée de n.
C e phénomèn e a ét utilis d'abor d comm e un e sourc e d'informatio n su r le s amas. Dans ces études /2/ on postulait une règle de correspondance "intensité •» stabilité" selon laquelle les amas les plus abondants dans le spectre de masse étaient aussi les plus stables, puis on effectuait des calculs sur la structure électronique des amas concernés qui, en général, permettaient de comprendre ce point.
Plu s récemment o n s'es t orient ver s un e meilleur e compréhensio n d u mécanisme d'émission lui-même, ceci pour tenter de relier par une formule ou une formulation mathématique les deux grandeurs physiques (intensité et stabilité) citées plus haut. Nous avons dans un travail précédent /3/ proposé un mécanisme de formation d'agrégats secondaires appliqué à l'émission d'ions Aïg émis à partir de cibles d'aluminium. Nous nous proposons ici d'étendre ce travail à 1'émission secondaire d'ions Cu£ et CuJ à partir de cibles de cuivre. Ce système est choisi parce que, d'une part, l'intensité de Cu| est très élevée (c'est l'amorce d'un phénomène d'alternance pair-impair avec ions de rang impair plus abondants); d'autre part, les courbes de potentiel du système Cu-Cu+ sont connues.
Dan s l e chapitr e suivan t nou s exposeron s notr e modèl e dan s se s grande s lignes nou s donneron s ensuit e e t discuteron s no s résultats I IFORMATIO
N D EDIMERE
S E T D ETRIMERE
SAprè
s l'impac t d'u n io n incidentï lémerg
e d'un e région ayan t approximativement quelques dizaines d'angstrbms de rayon, un nombre np d'atomes neutres (nQ ^ 6 pour le cuivre) et des ions monoatomiques des deux charges (10~1 à 10"2 par ion Article published online by
C2-130 JOURNAL DE PHYSIQUE
incident). Toutes ces particules sortant presque simultanément (1 'ensemble du phé- nomène se déroule en 'approximativement10-13s); le problème est de savoir avec quel-
le probabilité un ion Mt peut d'abord capter un atome M (formation d'un dimère M;) puis, éventuel lement un deuxième atome M (formation d' un trimère M;, destruction d'un dimère M$). On doit aussi tenir compte de l'accrochage direct d'un M2 sur M+. Le principe du calcul (lorsqu'on exclut la formation de trimères) est exposé en /3/ : pour une vitesse de M' donnée (énergie cinétique correspondante e) on éva- lue le nombre d'atomes secondairesM qui, au moment de leur émission (appelons p
la distance Mt - M à cet instant) sont tels que l'énergie cinétique du système Mt - M dans le centre de masse soit inférieure à l'énergie potentielle d'attractionEd2) (p). Notons que 1 'on se restreint au cas des vitesses perpendiculaires à la surface de la cible. Le modèle nécessite la connaissance de la distribution énergé-
tique et angulaire des M : on a pris pour le cuivre la même forme que pour 1 'alumi- nium (voir /3/, avec Eb = 0,5 eV). L'énergie E (p)est aussi fixée comme en /3/ à partir des courbes de potentiels calculée par 6" ne méthode ab-initia : (~62) en eV, p en A). Pour que le calcul de la formation de trimères (par accrochage d'un M sur M;) reste simple tout en correspondant le mieux possible au phénomène physique réel, nous avons effectué deux hypothèses (1) On suppose qu'il existp tout au cours du phénomène un centre de nucléation ponc- tuel de vitesse constante V. On ne tient donc pas compte de la délocalisation de la charge. De plus, cette hypothèse revientà calculer la probabilité d'accrochage
M + M; comme si tous les M$ avaient la vitesse ? de M'. Pour juger dans une certai- ne mesure de la validité de ce dernier point, nous avons calculé1 'énergie cinéti-
que moyenne des Mt perpendiculairement à la surface et vérifié qu'elle est bien le plus souvent procÂe de la valeur 2e qu'implique notre hypothèse (le plus grandécart est pour e
c 3,3 eV où l'on obtient 1,35 e)., (2) On n'introduit pour décrire 1 'accrochage M + M2 qu'une seule énergie potentiel- le é3) (p). En l'absence de données sur les "surfaces du potentiel" du système nous avong uti 1 isé 1 'hypothèse où a est fixé par des arguments sur la stabilité des amas CU; et CU;. On sait en effet que, dans une théorie "à un électron", l'énergie gagnée dans la réaction Cu + Cut -+ CU$ est @ (6: intégrale de transfert) alors qu'elle vaut 2,4~ dans la réaction Cu + CU; -+ Cu3 (on a pris pour Cu; la moyenne entre les formes linéaire et équilatérale). Ceci nous conduità prendre a = 2,4.
Le calcul de la probabilité d'obtenir un M: par l'autre mode de formation (accro- chage M2 -+ Mt) est du même type que celui exposé en /3/ pour les dimères. On a pris pour distribution angulaire et énergétique des M le carré de la diçtribution des M (avec comme nombre total de M2 . 1 -1). Le potenSiel d'attraction ~~(3) (p) est aussi choisi du type E?'(P) = aiE$(p) où al est le rapport de l'énergie gagnée dans la réaction Cu2 + Cut -. CU^ à l'énergie gagnée dans la réaction Cu + Cut -t Cu?, soit a' = 1,4. Comme les deux modes de formation d'un Cu; sont en général peu pro- bables, on peut les supposer indépendants et ajouter les probabilités obtenues dans les deux calculs.III - RESULTATS et DISCUSSION
Nous avons porté dans le tableau
1 les valeurs obtenues pour les probabilités de
former un Cu3 ou un Cu$ , respectivement: et P(2' . NOUS avons placé dans une même col onne les probabi 1 i tés correspondant à des parti cules qui ont approximativement la même énergie d'émission E. Pour ceci nous supposons, comme dans l'hypothèse (1) développée plus haut, que les probabilités pl3) et @) calculées lorsque le centre de nucléation originel a l'énergie e correspondentà des trimères d'énergies E valant
approximativement 3e et 2e. Tableau 1 - Probabilités de formation d'un dimère ou d'un trimère On peut ainsi estimer le rapport r31(c) des courants de trimères et d'ions simples pour différentes énergies d'émission e. On aura : où le facteur entre crochet provient de la distribution énergétique des ions simples (voir131). En tenant compte de ce qu'une partie des ions simples disparaît par
formation de dimères ou de trimères, on obtient : (1 eV) 2. 0,36 et F(li (5 eV) %0,95, ce qui conduit à r31 (1 eV) 2. 0,34 et r3~ (5 eV) 2. 2,54. Ces résultats mon-
trent qu'à basse énergie d'émission on peut s attendreà un courant en Cu+ plus im-
portant qu'en Cu', mais que cet effet disparaît à plus haute énergie; cetSe tendance est observée expérimentalement 141.REFERENCES
/1/ YU M.L., Phys. Rev., 824, (1981), 5625. /2/ JOYES P., J. Phys.CheE Sol ., 32, (1971), 1269.
/3/ JOYES P.,J. Phys., 44, (1983),721.
/4/ BLAISE G., Thèse d'EGt (1972) Orsay.quotesdbs_dbs46.pdfusesText_46[PDF] Les ions probleme 3eme
[PDF] Les ions, pour les pro
[PDF] les ions-interactions fondamentale
[PDF] les isitopes ; element chimique
[PDF] Les isomères d'une molécules
[PDF] Les isotopes d'hydrogene
[PDF] Les isotopes de l'hydrogène
[PDF] les isotopes de l'uranium
[PDF] les isotopes de l'hydrogène exercice
[PDF] les italiens a new york
[PDF] les italiens victimes de la xenophobie caricature
[PDF] les jardins d'agadir club marmara
[PDF] les jardins d'agadir contact
[PDF] les jardins d'agadir immobilier
