 Chapitre 12 : La réaction chimique - AlloSchool
Chapitre 12 : La réaction chimique - AlloSchool
▫ On appelle transformation chimique une transformation (réaction) au cours de laquelle des réactifs. (substances présentes au départ) sont consommés pour
 Chimie Générale (Chimie 1)
Chimie Générale (Chimie 1)
23 déc. 2020 ✓ Loi de conservation de la masse au cours d'une réaction (Lavoisier « lors d'une réaction chimique la masse totale des réactifs est égale à ...
 Les réactions chimiques
Les réactions chimiques
G L'annexe 18 présente une activité de laboratoire au cours de laquelle les élèves peuvent calculer avec un bon degré de précision la masse molaire du butane.
 Les transformations chimiques
Les transformations chimiques
Exemple : l'eau est une espèce chimique. b) Transformation physique. Au cours d'une transformation physique les espèces chimiques restent les mêmes : il ne.
 Chapitre Chimie N°8 La Réaction Chimique Objectifs du cours
Chapitre Chimie N°8 La Réaction Chimique Objectifs du cours
→. E.F = (Cu2+; Ag; NO3- ; Ag+ (?); Cu (?)) c) Réactifs et produits. Au cours d'une transformation chimique : → Les espèces chimiques qui disparaissent sont
 Cours de chimie g´en´erale Pr´eparation au concours B des ´ecoles
Cours de chimie g´en´erale Pr´eparation au concours B des ´ecoles
La cinétique chimique est l'étude de la cinétique des réactions chimiques. En d'autres termes elle permet d'étudier l'évolution temporelle des quantités de
 Réactions chimiques 1 :
Réactions chimiques 1 :
Le présent guide d'apprentissage constitue votre principal instrument de travail pour le cours Réactions chimiques 1 : énergie et cinétique chimique. Il a été
 Dangers chimiques liés à la présence de substances néoformées
Dangers chimiques liés à la présence de substances néoformées
En effet au cours du processus de transformation technologique et/ou de préparations culinaires industrielles ou ménagères des denrées alimentaires
 Chapitre 8 : Le tableau davancement
Chapitre 8 : Le tableau davancement
Au cours d'une transformation chimique des espèces chimiques sont modifiées : réactifs et des produits au cours de la réaction chimique. Il s'exprime en ...
 obS.2 avancement dune réaction chimique – cours
obS.2 avancement dune réaction chimique – cours
b) Transformation chimique : Les espèces chimiques qui constituent un système peuvent réagir entre elles. Le système peut donc évoluer au cours du temps. Cette
 Reaction chimique - Thermodynamique - Cinétique
Reaction chimique - Thermodynamique - Cinétique
La réaction chimique. Définition. Il s'agit d'une transformation au cours de laquelle un certain nombre de constituants initiaux appelés réactifs.
 Chimie Générale (Chimie 1)
Chimie Générale (Chimie 1)
Loi de conservation de la masse au cours d'une réaction (Lavoisier « lors d'une réaction chimique la masse totale des réactifs est égale à la masse totale
 Réactions chimiques 1 :
Réactions chimiques 1 :
Réactions chimiques 1 : énergie et cinétique chimique est le deuxième des trois guides d'apprentissage correspondant aux trois cours du programme Chimie 5e
 Chapitre 12 : La réaction chimique - AlloSchool
Chapitre 12 : La réaction chimique - AlloSchool
On appelle transformation chimique une transformation (réaction) au cours de laquelle des réactifs. (substances présentes au départ) sont consommés pour
 Cours de chimie g´en´erale Pr´eparation au concours B des ´ecoles
Cours de chimie g´en´erale Pr´eparation au concours B des ´ecoles
La cinétique chimique est l'étude de la cinétique des réactions chimiques. En d'autres termes elle permet d'étudier l'évolution temporelle des quantités de
 2. Réactions chimiques Stœchiométrie
2. Réactions chimiques Stœchiométrie
Equation chimique. Une réaction chimique est un processus par lequel des éléments ou des composés (les réactifs) interagissent en brisant et/ou en créant
 La réaction chimique
La réaction chimique
On peut considérer que l'élimination est une réaction au cours de laquelle une double liaison carbone : C=C est formée tandis qu'une petite molécule est libérée
 Chapitre VI: Lévolution des réactions chimiques
Chapitre VI: Lévolution des réactions chimiques
La transformation chimique est le passage d'un système chimique de l'état initial à l'état final. exemple: les ions iodure I - avec les ions peroxodisulfate
 Les transformations chimiques
Les transformations chimiques
Exemple : l'eau est une espèce chimique. b) Transformation physique. Au cours d'une transformation physique les espèces chimiques restent les mêmes : il ne.
 COURS DE CHIMIE GENERALE Semestre 1 SVI
COURS DE CHIMIE GENERALE Semestre 1 SVI
Titrage d'un acide faible par une base forte. CHAPITRE III : REACTIONS D'OXYDO-REDUCTION. 1. Généralités. 1.1. Oxydant réducteur

Chapitre 12 : La réaction chimique 1. La transformation chimique (Voir TP n°11) Définitions : On appelle système chimique lensemble des espces chimiues prsentes dans un milieu ; On appelle transformation chimique, une transformation (réaction) au cours de laquelle des réactifs (substances présentes au départ) sont consommés pour former des produits nouveaux (substances formées après la transformation). ÉTAT INITIAL ÉTAT FINAL L'état d'un système chimique est caractérisé par : - Les grandeurs physiques P (pression du ou des gaz) et T (température) ; - L'état physique des espèces présentes : liquide (), solide (s), gazeux (g) ou aqueux (aq) ; - Les quantités de matière des espèces chimiques présentes. Lolution dun systme est caractrise par : - Des substances chimiques qui disparaissent, on les appelle les REACTIFS ; - Des substances chimiques apparaissent, on les appelle les PRODUITS. Ltat final est atteint lorsue lun au moins des ractifs est totalement consomm : la transformation chimique sarrte. A RETENIR : - Ltat du systme aant la transformation chimiue sappelle ltat initial ; - Ltat du systme aprs la transformation chimiue sappelle ltat final ; - La transformation chimique est le passage dun systme de l'état initial à l'état final. 2. Lquation de réaction 2.1. Définitions Définitions : On associe à la transformation chimique dun systme un modle ui rend compte, lchelle macroscopiue, de lolution du systme cest la réaction chimique ; L'équation d'une réaction est l'écriture symbolique d'une réaction chimique : REACTIFS PRODUIT(S) symboles des réactifs séparés par des signes " + » La flèche indique le sens de la transformation chimique symboles des produits de la transformation, séparés par des signes " + » A RETENIR : - Lors dune transformation chimiue, les lments chimiues sont consers ; - La réaction chimique modélise une transformation chimique ; - Luation dune raction symbolise une réaction chimique aussi bien au niveau moléculaire que molaire ; aA + bB cC + dD Exemple : C + O2 CO2 - Lorsque des ions interviennent, la charge globale des réactifs doit être égale à la charge globale des produits.
2.2. criture dune uation de raction
Définitions :
Les coefficients stƈchiomtriƋues sont des nombre positifs qui indiquent les proportions dans lesquelles les
espèces chimiques réagissent ou sont produites au cours dune raction chimiue. Ils traduisent la
conservation de la matière : aA + bB cC + dD (a, b, c, d sont les coefficients stƈchiomtriues)Équilibrer une uation de raction consiste dterminer les coefficients stƈchiomtriques de léquation de
la réaction. Méthode pour équilibrer une équation de réaction : n Identifier les réactifs et les produits de la réaction chimique ;o Écrire les formules brute des différents constituants à gauche (réactifs) et à droite (produits) de la flèche
symbolisant la transformation en précisant leur état physique ; p Compter le nombre datomes pour chaue lment chimiue de part et dautre de la flèche : - Sil y a le mme nombre datomes des deudž cots pour tous les lments prsents alors les nombres stƈchiomtriues sont ajusts : la loi de conservation de la matière est vérifiée ;- Sinon, il faut faire précéder les formules brutes du nombre stƈchiomtriue adapt pour rifier la
conservation des éléments. q Complter luation de la raction en rajoutant les coefficients stƈchiomtriues adapts ; r Vérifier la loi de conservation des charges (sil y a lieu).2.3. Conservation de la masse au cours dune transformation chimiue
Observations :
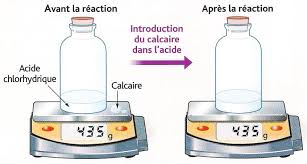
- Lorsque la craie (calcaire) entre en contact aec lacide (acide chlorhydriue ou le vinaigre) il se produit une effervescence. - Au cours de cette transformation chimique, la masse est la même avant et après la disparition de la craie.Interprétation :
Lacide ragit aec le calcaire pour former du diodžyde de carbone et dautres produits.A RETENIR :
Au cours dune transformation chimiue, la masse des ractifs ui disparaissent est gale la masse des produits ui
se forment : il y a conservation de la masse (ou de la matière).3. La transformation physique
Définition :
Une transformation physique est une transformation au cours de laquelle la nature et les propriétés de la
matière ne sont pas modifiées : les atomes et les molécules ne changent pas. Exemples : changement dtat, dissolution, edžtraction͙4. Les effets thermiues dune transformation
Lors dune raction chimiue, un systme peut absorber ou céder de lnergie sous forme de chaleur (appelée
énergie thermique).
Définitions :
Lorsue uune transformation chimiue saccompagne dune augmentation de la température, la transformation est dite exothermique ;Lorsue uune transformation chimiue saccompagne dune diminution de la température, la transformation
est dite endothermique ;Si aucun effet thermique napparait lors dune transformation chimiue, la transformation est dite athermique.
Chapitre 12 : La réaction chimique
Les objectifs de connaissance :
- Dfinir ltat initial et ltat final dun systme chimiue ; - Faire la distinction entre une transformation chimique et une transformation physique ; - Définir luation dune raction chimiue ; - Connaître les effets thermiues dune transformation physique ou chimique.Les objectifs de savoir-faire :
- Décrire un système chimique et son évolution ; - crire luation dune réaction chimique ;- Ajuster les nombres stƈchiomtriues dans (équilibrer) une équation de réaction chimique.
Je suis capable de Oui Non
- Définir les mots : système chimique, transformation chimique, réactif, produit, réaction
chimique, équation de réaction, coefficient stƈchiomtriƋue transformation physique, exothermique, endothermique, et athermique. - Identifier les ractifs et les produits dune transformation chimique. (cf. §1) - crire et uilibrer luation dune raction chimiue. (cf. §2.1 & 2.2) - De montrer uil y a conseration de la masse (ou de la matire) au cours dune transformation chimique. (cf. §2.1 & 2.3) - Dedžpliuer uun effet thermique accompagne une transformation (physique ou chimique). (cf. §4)quotesdbs_dbs2.pdfusesText_2[PDF] cours de langage de programmation c++
[PDF] cours de langage de programmation java
[PDF] cours de langage de programmation pascal
[PDF] cours de langage de programmation visual basic
[PDF] cours de linguistique générale english
[PDF] cours de linguistique générale english pdf
[PDF] cours de linguistique générale explication pdf
[PDF] cours de linguistique générale ferdinand de saussure pdf
[PDF] cours de linguistique générale pdf
[PDF] cours de linguistique générale saussure
[PDF] cours de maths trigonométrie première s
[PDF] cours de philosophie sur l'etat
[PDF] cours de philosophie sur l'etat pdf
[PDF] cours de philosophie sur l'existence et la mort
