 Chapitre 3 :Oxydoréduction
Chapitre 3 :Oxydoréduction
• Oxydation : réaction au cours de laquelle une espèce perd un ou plusieurs On considère une réaction d'oxydoréduction qui se produit dans une cellule.
 Les réactions doxydo-réduction
Les réactions doxydo-réduction
➔ Le réducteur d'un couple (noté 1) peut participer à une réaction chimique avec l'oxydant d'un autre couple. (noté 2). ➔ Au cours de cette réaction le
 Fiche de synthèse n° 3.c Réactions doxydo-réduction
Fiche de synthèse n° 3.c Réactions doxydo-réduction
1.1. Définitions : Une oxydation est une réaction chimique où il y a perte d'un ou plusieurs électrons. Au cours d'
 Leçon 11 : RÉDUCTION DES OXYDES
Leçon 11 : RÉDUCTION DES OXYDES
-Une réaction d'oxydoréduction est une réaction chimique au cours de laquelle l'oxydation et la réduction se font simultanément. Activité d'application a-Ecris
 Réactions doxydo-réduction
Réactions doxydo-réduction
Interprétation : Au cours de cette transformation. • Le dépôt rouge est du cuivre métallique constitué d'atomes de cuivre de formule Cu
 Chimie analytique 2éme année pharmacie -Les réactions d
Chimie analytique 2éme année pharmacie -Les réactions d
1.2. Définition d'une réaction d'oxydo-réduction : Une réaction d'oxydoréduction est une réaction chimique au cours de laquelle se produit un transfert.
 CHAPITRE 3 : Réactions doxydo-réduction
CHAPITRE 3 : Réactions doxydo-réduction
Au cours de cette oxydation le réducteur se transforme en sa forme conjuguée qui est un oxydant : β Red = α Ox + ne−. • Réduction : gain d'électron(s) par un
 Chimie analytique 2éme année pharmacie -Les réactions d
Chimie analytique 2éme année pharmacie -Les réactions d
1.2. Définition d'une réaction d'oxydo-réduction : Une réaction d'oxydoréduction est une réaction chimique au cours de laquelle se produit un transfert.
 Les réactions doxydoréduction
Les réactions doxydoréduction
>>Une oxydation est une réaction au cours de laquelle des électrons sont produits. >>Une espèce capable de former des électrons au cours d'une réaction d'
 TROISIEME ANNEE CHIMIE : OXYDOREDUCTION COMMENT
TROISIEME ANNEE CHIMIE : OXYDOREDUCTION COMMENT
4) Les couples mis en jeu Au cours de cette réaction sont S FeS. ⁄ et FeS Fe. ⁄ . II. REACTION ENTRE LE CARBONE (C) ET L'OXYDE DE CUIVRE (CuO) : ENONCE : On
 Chapitre 3 :Oxydoréduction
Chapitre 3 :Oxydoréduction
I Réactions d'oxydoréduction. A) En solution aqueuse. 1) Définition. • Oxydation : réaction au cours de laquelle une espèce perd un ou plusieurs électrons.
 Les réactions doxydo-réduction
Les réactions doxydo-réduction
? Le réducteur d'un couple (noté 1) peut participer à une réaction chimique avec l'oxydant d'un autre couple. (noté 2). ? Au cours de cette réaction le
 Cours de chimie en solution Oxydoréduction
Cours de chimie en solution Oxydoréduction
- Equilibrer la charge (électro neutralité de demi-réaction) avec des électrons e - . Fe3+ + 1.e-. Fe2+. Couple (Fe3+/ Fe2+). (+III). (+II).
 Chimie analytique 2éme année pharmacie -Les réactions d
Chimie analytique 2éme année pharmacie -Les réactions d
1.2. Définition d'une réaction d'oxydo-réduction : Une réaction d'oxydoréduction est une réaction chimique au cours de laquelle se produit un transfert.
 Chapitre 6 : Les réactions doxydoréduction
Chapitre 6 : Les réactions doxydoréduction
Nous allons voir dans ce chapitre les réactions d'oxydoréduction est trouver une grande 1) Réaction entre les ions cuivre II et le métal zinc :.
 Chapitre SA-PC&PSI. Seconde période Plan du cours
Chapitre SA-PC&PSI. Seconde période Plan du cours
26 Mar 2017 Dans une réaction d'oxydoréduction un élément chimique perd (oxydation) ou gagne (réduction) des électrons. Le nombre d'oxydation d'un élément ...
 Chapitre 2 : Réactions doxydoréduction
Chapitre 2 : Réactions doxydoréduction
2.4 Equilibre d'oxydoreduction en milieu basique . Les réactions d'oxydoréduction sont des réactions chimiques au cours desquelles il y a un échange d' ...
 Chapitre 4 Oxydo-réduction
Chapitre 4 Oxydo-réduction
Dans une réaction d'oxydoréduction les réactifs sont un oxydant et un réducteur de Au cours de cette réaction
 GÉNÉRALITÉS SUR LOXYDORÉDUCTION
GÉNÉRALITÉS SUR LOXYDORÉDUCTION
22 Feb 2016 Réaction chimique d'oxydoréduction. Réactions d'oxydoréduction
 CHAPITRE 2 : LES REACTIONS DOXYDO-REDUCTION
CHAPITRE 2 : LES REACTIONS DOXYDO-REDUCTION
Une réaction d'oxydo-réduction est une transformation chimique au cours de laquelle il y a un échange d'électrons entre l'oxydant d'un couple
 [PDF] Chapitre 3 :Oxydoréduction - Melusine
[PDF] Chapitre 3 :Oxydoréduction - Melusine
I Réactions d'oxydoréduction A) En solution aqueuse 1) Définition • Oxydation : réaction au cours de laquelle une espèce perd un ou plusieurs électrons
 [PDF] Les réactions doxydo-réduction - Physique - Chimie
[PDF] Les réactions doxydo-réduction - Physique - Chimie
? Au cours de cette réaction le réducteur 1 va libérer 1 ou plusieurs électrons qui seront ensuite captés par l'oxydant 2 exemple : réaction entre le
 [PDF] Chimie - Chapitre 9 : Réactions doxydoréduction Ce quil faut retenir
[PDF] Chimie - Chapitre 9 : Réactions doxydoréduction Ce quil faut retenir
La réaction susceptible de se produire à l'interface met en jeu un couple redox : ? Ox + n e- + x H+ = ? Red + y H2O Potentiel de Nernst d'un couple redox : Le
 [PDF] Chapitre 4 Oxydo-réduction
[PDF] Chapitre 4 Oxydo-réduction
2 Les réactions d'oxydoréduction 2 1 Définition Dans une réaction d'oxydoréduction les réactifs sont un oxydant et un réducteur de deux couples oxydant
 [PDF] COURS-Oxydoreductionpdf
[PDF] COURS-Oxydoreductionpdf
I – REACTIONS D'OXYDOREDUCTION 1-1 Introduction Les réactions d'oxydoréduction sont des réactions dans lesquelles des électrons sont transférés
 [PDF] Cours-Réaction-redoxpdf
[PDF] Cours-Réaction-redoxpdf
? couple d'oxydo-réduction ou couple redox est un couple formé par un oxydant et son réducteur conjugué Oxydant + ne- Réducteur ? Par convention on écrit
 [PDF] Chapitre 6 : Les réactions doxydoréduction - Physagreg
[PDF] Chapitre 6 : Les réactions doxydoréduction - Physagreg
Nous allons voir dans ce chapitre les réactions d'oxydoréduction est trouver une grande 1) Réaction entre les ions cuivre II et le métal zinc :
 [PDF] Chimie analytique 2éme année pharmacie -Les réactions d
[PDF] Chimie analytique 2éme année pharmacie -Les réactions d
1 2 Définition d'une réaction d'oxydo-réduction : Une réaction d'oxydoréduction est une réaction chimique au cours de laquelle se produit un transfert
 [PDF] GÉNÉRALITÉS SUR LOXYDORÉDUCTION
[PDF] GÉNÉRALITÉS SUR LOXYDORÉDUCTION
22 fév 2016 · Réaction chimique d'oxydoréduction Réactions d'oxydoréduction Potentiel d'électrode et oxydoréduction Titrages par oxydoréduction COURS
 [PDF] [PDF] 1 Généralités sur loxydo-réduction
[PDF] [PDF] 1 Généralités sur loxydo-réduction
2 2 Loi de Nernst et sens d'évolution d'une réaction d'oxydo-réduction Ce cours fait partie du programme de préparation aux 51me Olympiades
Comment définir une réaction d'oxydoréduction ?
Une réaction d'oxydoréduction est une réaction qui implique un échange d'électrons entre des réactifs. De nombreuses transformations chimiques impliquent le transfert d'un ou de plusieurs électrons d'un atome à un autre.Comment savoir qui est l'oxydant et qui est le réducteur ?
Pour savoir qui est l'oxydant et le réducteur , en utilise cette définition : La substance qui perd des électrons est oxydée et est le réducteur. La substance qui gagne des électrons est réduite et est l'oxydant .- Pour écrire une équation d'oxydo-réduction il faut donc commencer par écrire les deux demi équations puis de les combiner pour former l'équation complète en vérifiant que le nombre d'électrons perdus lors de l'oxydation corresponde au nombre d'électrons gagnés lors de la réduction.
Chapitre 2
Réactions d"oxydoréduction2.1 Couple Oxydant/Réducteur . . . . . . . . . . . . . . . . . . . . . . . . . . .22
2.2 Equilibrer une demi équation électronique . . . . . . . . . . . . . . . . . .
222.3 Réaction d"oxydoréduction . . . . . . . . . . . . . . . . . . . . . . . . . . . .
222.4 Equilibre d"oxydoreduction en milieu basique . . . . . . . . . . . . . . . .
2324Chapitre 2.Réactions d"oxydoréductionA
prèsavoir étudié la notion de transformation chimique et le suivi des transformations à l"aide
d"un tableau d"avancement, nous allons étudier ici un type bien particulier de réaction chimique :
la réaction d"oxydoréduction.Les réactions d"oxydoréduction sont des réactions chimiques au cours desquelles il y a un échange d"un
ou plusieurs électrons entre deux espèces chimiques.2.1 Couple Oxydant/RéducteurCouple oxydant/réducteur
Unoxydantest une espèce capable decapter(ougagner) un ou plusieurs électrons. Unréducteurest une espèce capable decéder(ouperdre) un ou plusieurs électrons. Un couple oxydant/réducteur, notéOx/Redest l"ensemble formé par deux espèces chimiques qui se transforment l"une en l"autre lorsque l"une ou l"autre perd ou gagne un ou plusieursélectrons. Le passage de l"un à l"autre se modélise alors par unedemi équation électronique:
Ox+ne-=Red
oùnreprésente le nombre d"électrons échangés.2.2 Equilibrer une demi équation électronique
Tout comme on équilibre l"équation bilan d"une réaction chimique, il faut équilibre une demi-équation
électronique de sorte à assurer laconservation de la matière et de la charge.Equilibrer une demi-équation Redox
Voici, dans l"ordre, ce qu"il faut équilibrer dans une demi équation électronique : 1. Les atomes autres que l"o xygèneet l"h ydrogène 2. Les o xygènesen a joutantdes molécules d"eau H2O du bon côté
3.Les h ydrogènesen a joutantdes ions H
+du bon côté 4. En dernier la c hargeen a joutantle nom bred"électrons e -nécessaireExemples: 1. Ag +(aq)+e-=Ag(s) 2. MnO4-(aq)+ 8H+(aq)+ 5e-=Mn2+(aq)+ 4H2O(l)
3. S4O62-(aq)+ 2e-= 2S2O32-(aq)
2.3 Réaction d"oxydoréduction
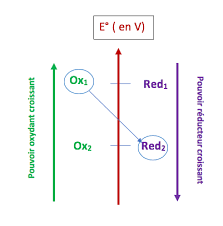
Une réaction d"oxydoréduction a lieu lorsque l"oxydantOx1d"un coupleOx1/Red1réagit avec leréducteurRed2d"un coupleOx2/Red2pour former les réducteurRed1et oxydantOx2conjuguésPoisson Florian Spécialité Physique-Chimie 1
ère
2.4.Equilibre d"oxydoreduction en milieu basique25des couples. Il faut alors équilibrer successivement les deux demi équations électroniques des deux
couples, puis lescombinerpour équilibrer l"équation bilan de la réaction. (N.B :combiner ici prend
exactement le même sens que lorsqu"on combine des équations en maths dans un système de deux
équations à deux inconnues. Le but étant ici d""éliminer" les électrons, qui ne doivent pas apparaître
dans l"équation bilan).Réaction d"oxydoréduction Ox1+n1e-=Red1(×n2)
Red2=Ox2+n2e-(×n1)n
2Ox1+n1Red2=n1Ox2+n2Red1Exemple:On considère les couples suivants : Fe3+(aq)/Fe2+(aq)et MnO4-(aq)/Mn2+(aq).
MnO4-(aq)+ 8H+(aq)+ 5e-=Mn2+(aq)+ 4H2O(l)
Fe2+(aq)=Fe3+(aq)+e-(×5)
On multiplie la deuxième demi-équation par 5 et on somme les deux demi-équations pour obtenir
l"équation bilan suivante : 5Fe2+(aq)+ MnO4-(aq)+ 8H+(aq)5Fe
3+(aq)+ Mn2+(aq)+ 4H2O(l)
2.4 Equilibre d"oxydoreduction en milieu basique
Dans ce qui précède, les demi équations électroniques, et donc les équations bilan aussi, ont été
équilibrées en utilisant des ions H
+. Il s"agit de la méthode à employer lorsque la réaction a lieu enmilieu acide. Lorsqu"elle a lieu en milieu basique, il faut équilibrer cette fois ci avec des ions hydroxyde
HO -à la place des ions H+.Pour ce faire, le plus simple est de commencer par équilibrer en milieu acide, puis de passer en milieu
basique grâce au fait que : H ++HO-H 2O.Exemple:On reprend l"équation bilan de l"exemple précédent en milieu acide, et on passe en milieu
basique : 5Fe2+(aq)+ MnO4-(aq)+ 8H+(aq)5Fe
3+(aq)+ Mn2+(aq)+ 4H2O(l)
5Fe2+(aq)+ MnO4-(aq)+ 8H+(aq)+ 8HO-(aq)5Fe
3+(aq)+ Mn2+(aq)+ 4H2O(l)+ 8HO-(aq)
5Fe2+(aq)+ MnO4-(aq)+ 8H2O(l)5Fe
3+(aq)+ Mn2+(aq)+ 4H2O(l)+ 8HO-(aq)
5Fe2+(aq)+ MnO4-(aq)+ 4H2O(l)5Fe
3+(aq)+ Mn2+(aq)+ 8HO-(aq)Spécialité Physique-Chimie 1
èrePoisson Florian
quotesdbs_dbs14.pdfusesText_20[PDF] réaction d'oxydoréduction exemple
[PDF] réaction d'oxydoréduction exercices corrigés
[PDF] réaction d'oxydoréduction exercices corrigés pdf
[PDF] réaction d'oxydoréduction fe2+/fe3+
[PDF] réaction d'oxydoréduction pdf
[PDF] réaction de fission def
[PDF] réaction de fission du plutonium 239
[PDF] réaction de fission exemple
[PDF] réaction de fission nucléaire définition
[PDF] réaction de fission uranium 235
[PDF] réaction de la fermentation alcoolique
[PDF] réaction de la fermentation lactique
[PDF] réaction de la glycolyse
[PDF] réaction de la peau au soleil
